
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика проведения работы по определению равновесной концентрации железо-салицилового комплексаСодержание книги
Поиск на нашем сайте
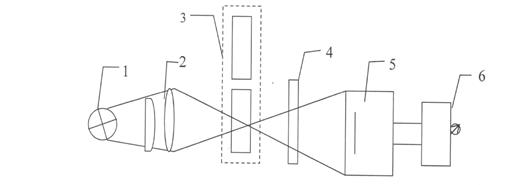
Равновесную концентрацию железо-салицилового комплекса определяют колориметрическим (спектрофотометрическим) методом. Колориметрические определения основаны на сравнении поглощения при пропускании света стандартным и исследуемым окрашенным раствором. В основе метода лежит объединенный закон Бугера-Ламберта-Бера, который можно выразить уравнением А= e ∙ c ∙ l, (3.13) где А – оптическая плотность, Io – интенсивность падающего света; I – интенсивность светового потока после прохождения света через раствор; c – концентрация растворенного вещества, моль/л; l – толщина поглощающего слоя, см; e – молярный коэффициент поглощения света (коэффициент экстинкции). Молярный коэффициент поглощения света представляет собой оптическую плотность 1М раствора, помещенного в кювету с толщиной слоя 1 см. Он зависит от длины волны падающего света, температуры раствора и природы растворенного вещества и растворителя. Для измерения оптической плотности используются спектрофотометры различных конструкций. Оптическая схема фотоэлектроколориметра (самого простого прибора для определения оптической плотности) приведена на рисунке 3.1. Световой поток от источника света 1 фокусируется системой линз 2 на кювете с раствором 3. Затем свет проходит через светофильтр 4 для выделения определенной длины волны и попадает на фотоэлемент 5, где преобразуется в электрический сигнал. Фототок после его усиления регистрируется на гальванометре 6. Принцип работы фотоэлектроколориметра: установка на ноль регистрирующей стрелки прибора при прохождении монохроматического излучения через раствор сравнения («холостой» раствор), чаще всего воду или другой растворитель, и измерение оптической плотности исследуемого раствора после перемещения кюветодержателя в световой поток.
Рисунок 3.1 – Оптическая схема фотоколориметра
Порядок проведения работы
1. Приготовление стандартных растворов. В качестве основных реагентов используют растворы FeCl3 в 5 . 10–2 М растворе HCl и водные растворы салициловой кислоты. Для определения концентрации железо-салицилового комплекса в реакционной смеси предварительно устанавливают зависимость оптической плотности раствора от его концентрации и строят градуировочный график. Для этого готовят серию стандартных растворов FeCl3 в 5,0∙10–2М растворе HCl в избытке салициловой кислоты. Концентрации смешиваемых растворов приведены в таблице 3.1.
Для приготовления реакционной смеси растворы FeCl3 заданной концентрации сливают с равным объемом салициловой кислоты (например, 2,5 мл раствора FeCl3 и 2,5 мл салициловой кислоты, общий объем каждой смеси должен составлять 5 мл). Смешение растворов проводят, начиная с меньшей концентрации. Концентрацию FeCl3 в реакционной смеси рассчитывают по формуле
где С i – концентрация с поправкой на разбавление раствора при смешении; С о – концентрация исходного раствора FeCl3; V 1 – объем раствора FeCl3, мл; V 2 – объем раствора салициловой кислоты, мл.
Таблица 3.1 – Данные для построения градуировочного гррафика
2. Построение градуировочного графика зависимости оптической плотности А от концентрации раствора С i. Измеряют оптическую плотность серии приготовленных стандартных растворов (концентрации указаны в графе 4 таблицы 3.1) при длине волны λ = 480 нм в кюветах толщиной 1 см. Раствор сравнения – дистиллированная вода. Результаты измерения оптической плотности А растворов заносят в графу 5 таблицы 3.1. Полученные результаты представляют в виде графика А = f (C i). Для этого по экспериментальным данным рассчитывают уравнение градуировочного графика. Учитывая, что используется избыток салициловой кислоты, можно принять, что концентрация железо-салицилового комплекса в реакционной смеси равна концентрации С i раствора FeCl3; поэтому на оси абсцисс графика откладывается концентрация комплекса. Правила построения градуировочного графика приведены на стр. 7.
|
||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 137; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.8.172 (0.009 с.) |
|||||||||||||||||||||||

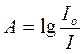 ;
;
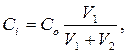 (3.14)
(3.14)


