Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема 3. Кровь. Лимфа. Кроветворение (гемопоэз)
КРОВЬ – своеобразная жидкая ткань, которая циркулирует в сосудах благодаря ритмическим сокращениям сердца. В организме взрослого человека содержится около 4-6 л крови. Потеря более 30 % крови приводит к смерти. Ни одна ткань нашего организма не исследуется в диагностических целях так часто, как кровь. Анализ крови благодаря простоте получения ее проб у больного и высокой диагностической ценности результатов получил широкое распространение в клинической медицине. Кровь находится в непрерывном движении, она, доставляет всем тканям питательные вещества и кислород и удаляет из них продукты обмена, переносит гормоны, участвует в регулировании содержания кислот, оснований и воды в клетках, играет важную роль в регуляции температуры тела. Следовательно, кровь является той средой, при посредстве которой обеспечивается внутренний обмен, нормальное течение жизненного процесса. Но, помимо перечисленных функций, кровь имеет огромное защитное значение. Некоторые формы лейкоцитов обладают способностью захватывать и переваривать чужеродные тела – вредные микроорганизмы, отмершие клетки, очищая, таким образом, внутреннюю среду организма. Все это определяет важнейшую роль крови в организме. Кровь, вытекающая из раны, имеет вид однородной красной жидкости; однако на самом деле она состоит из желтоватой жидкости, называемой плазмой, и плавающих в ней форменных элементов: красных кровяных телец – эритроцитов, сообщающих крови ее цвет, белых кровяных телец – лейкоцитов и кровяных пластинок – тромбоцитов. Все клетки крови имеют микроскопические размеры, поэтому рассмотреть их можно только с помощью микроскопа. Форменные элементы составляют около 45 % объема крови, а остальные 55 % приходятся на долю плазмы. Потеря воды при обильном потоотделении может уменьшить объем плазмы до 50 % объема крови, а употребление большого количества воды или пива может увеличить его до 60 %. Циркулируя по кровеносным сосудам, кровь непрерывно перемешивается, поэтому плазма и клетки крови не отделяются друг от друга. Плазма крови – это жидкое межклеточное вещество, в котором взвешены форменные элементы. Химический анализ показывает, что в плазме содержится 90 % воды, 9 % органических веществ и 1 % неорганических. Главные органические компоненты плазмы – белки, которые обеспечивают ее вязкость, давление, свертываемость, переносят различные вещества и выполняют защитные функции.
Основные белки плазмы: - альбумины - количественно преобладающие белки плазмы крови, переносят ряд метаболитов, гормонов, ионов, поддерживают осмотическое давление крови; - глобулины (α- и β -) – переносят ионы металлов и липиды в форме липопротеинов; γ-глобулины представляют собой фракцию антител (иммуноглобулинов); - фибриноген – обеспечивает свертывание крови, превращаясь в нерастворимый белок фибрин под действием тромбина; - компоненты комплемента – участвуют в неспецифических защитных реакциях. Выработка белков плазмы осуществляется клетками печени, за исключением γ-глобулинов, которые продуцируются плазматическими клетками. Сыворотка крови – жидкость, остающаяся после свертывания крови. По своему составу она сходна с плазмой крови, однако в ней отсутствует фибриноген и факторы свертывания. Форменные элементы крови включают эритроциты, тромбоциты и лейкоциты (рис. 17). Из них только лейкоциты являются истинными клетками, эритроциты и тромбоциты человека относятся к постклеточным структурам. Концентрации форменных элементов определяют при анализе крови в расчете на 1 мкл (1 мм3) или 1 л крови. Результаты анализа записывают в виде гемограммы, отражающей наряду с некоторыми биологическими показателями содержание отдельных форменных элементов (таблица 1): Таблица 1
Красные кровяные тельца (рис. 17), или эритроциты наиболее многочисленные форменные элементы крови. Они имеют форму двояковогнутых дисков. В отличие от большинства клеток организма человека эритроциты лишены ядра. Свежие эритроциты зеленовато-желтого цвета и только в толстом слое получают красноватый оттенок. В крови взрослого человека обычно циркулирует 25-30 триллионов эритроцитов. В 1 микролитре, или кубическом миллиметре крови мужчины содержится 4,5-5,5 миллионов эритроцитов и у женщины – 4,0-5,0 миллиона красных кровяных телец. Однако число красных кровяных клеток у здоровых людей может варьировать в зависимости от возраста, эмоциональной и мышечной нагрузки, действия экологических факторов и т. д. Эритроциты не способны активно передвигаться – они просто плывут в потоке крови, двигаясь под действием нагнетающей силы сердца. Эритроциты образуются в красном костном мозге, а затем разрушаются макрофагами селезенки, печени и красного костного мозга. Около 120 дней кружит в теле эритроцит (например, при занятии "моржеванием", продолжительность жизни эритроцитов может сокращаться до 24 суток), после этого он «идет в утиль» и пожирается макрофагом. Потерю эритроцитов приходится постоянно восполнять, и при необходимости (ранение, обильное кровотечение из носа, сильная менструация или внезапный дефицит кислорода в воздухе) специальный гормон – эритропоэтин – многократно ускоряет процесс их производства. В обычных условиях наш костный мозг производит примерно 2,5 млн. эритроцитов в секунду.
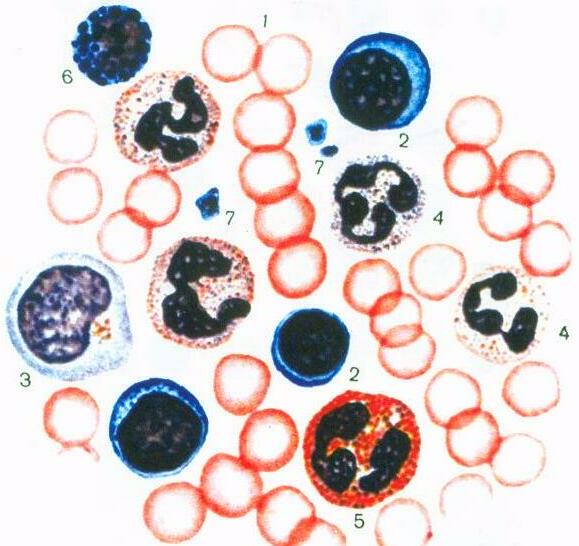
Рис. 17. Мазок крови человека. Окраска по Романовскому-Гимзе. Увел. 10х90: 1 — эритроциты; 2 — лимфоциты (малый и большой);3 — моноцит; 4 — нейтрофильные гранулоциты (лейкоциты);5 — эозинофильный гранулоцит (лейкоцит);б — базофильный гранулоцит (лейкоцит);7 — кровяные пластинки (тромбоциты).
Каждый эритроцит содержит красный пигмент – гемоглобин. Гемоглобин является самой важной молекулой в доставке кислорода от легких к тканям и представляет собой не просто белковую молекулу, пассивно связывающуюся с кислородом, а сложную молекулярную машину, в задачу которой входит захватить максимальное количество кислорода в легких, доставить его к периферическим тканям и, забрав оттуда углекислый газ, транспортировать его в легкие. В норме в кровотоке присутствует около 1 % не вполне зрелых эритроцитов, сохранивших в цитоплазме небольшое количество рибонуклеопротеидов, обеспечивающих на ранних стадиях развития синтез гемоглобина. При специальном окрашивании – крезилвиолетом – они видны как сетевидные структуры, поэтому такие клетки назвали ретикулоцитами. Ретикулоциты созревают в кровотоке до эритроцитов за 24-30 ч. Большинство эритроцитов (66 %) имеют форму двояковогнутого диска. Однако возможны и другие формы: в виде колпачка – стоматоциты (18,5 %), округлые клетки с шиповатыми выростами – эхиноциты (5,7 %), округлые – сфероциты (4,2 %) и некоторые другие. Изменение формы эритроцита по сравнению с самой распространенной называется пойкилоцитозом. Диаметр большинства эритроцитов в окрашенных мазках составляет 7,2 мкм – это нормоциты, менее 6 мкм - микроциты, а более крупные – от 9 до 12 мкм – макроциты. Появление в крови большого разнообразия эритроцитов по величине называется анизоцитозом. По содержанию гемоглобина эритроциты также неодинаковы. Их подразделяют на нормохромные, гипохромные и гиперхромные. Способность к переносу кислорода зависит от количества в них гемоглобина. Уменьшение количества эритроцитов или их насыщенности гемоглобином называется анемией и приводит к нарушению окислительных процессов в организме и развитию гипоксии – кислородному голоданию.
На строение и функции эритроцитов большое влияние оказывает осмотическое давление. В гипотоническом растворе эритроциты разбухают, гемоглобин из них выходит, и оболочка видна в виде «тени» (гемолиз). Гемолиз эритроцитов вызывают растворители жиров, например, липолитические ферменты змеиного яда, плазма чужой крови и т.д. В гипертоническом растворе вода уходит из эритроцитов и они сморщиваются. Гемоглобин эритроцита, связанный с кислородом, - оксигемоглобин – придает розовую окраску кожным покровам, в частности, губам. Отдавший кислород дезоксигемоглобин имеет пурпурный цвет, поэтому при нарушении оксигенации в легких отмечают некоторое посинение губ (цианоз) и бледность кожи. Угарный газ прочно связывается с гемоглобином, это соединение окрашивает губы в ярко-красный цвет. Плазмолемма эритроцитов является самой толстой (20 нм) и наиболее изученной мембраной из всех биологических мембран. Она содержит рецепторы иммуноглобулинов, компонентов комплемента и ряда других веществ. В ее состав входят многочисленные интегральные и периферические белки, участвующие в транспортных процессах (в качестве ионных насосов, каналов, переносчиков) и обеспечивающие прикрепление элементов цитоскелета. Она обладает гибкостью, прочностью, растяжимостью, резистентностью к окислению, протеолизу и влиянию других повреждающих факторов. На наружной поверхности плазмолемма эритроцитов несет антигены Rh и детерминанты групп крови. Цитоскелет эритроцитов образован рядом периферических и транспортных белков (рис. 18). В его состав входят: спектрин, гликофорин, анкирин, белки полосы 3 и полосы 4.1. Последние два названия отражают положение фракций при электрофорезе белков мембраны эритроцита. Белок полосы 3 выполняет помимо цитоскелетных функций роль анионного транспортного белка, обеспечивающего процессы газообмена. Спектрин – периферический белок, служащий главным элементом цитоскелета эритроцита. Его молекула состоит из двух перекрученных цепей – димеров (α- и β), которые стыкуются друг с другом «конец в конец». Он образует гибкую двумерную сеть филаментов на внутренней поверхности плазмолеммы эритроцита. Эти филаменты связаны в узлы с помощью актина и белка полосы 4.1 и прикреплены к трансмембранному белку полосы 3 посредством анкирина. Белок полосы 4.1 может связываться с цитоплазматическим доменом другого трансмембранного белка – гликофорина. В состоянии покоя спектриновые нити скручены; при деформации в одних участках они распрямляются и вытягиваются, в других – скручиваются еще сильнее, благодаря чему происходит изменение формы эритроцита без изменения площади его поверхности. При более значительной деформации, требующей увеличения поверхности, может нарушаться связь элементов цитоскелета с плазмолеммой, и возникшая деформация станет необратимой или произойдет фрагментация плазмолеммы. Благодаря описанному устройству цитоскелета эритроцит обладает гибкостью и способен обратимо деформироваться в мелких сосудах.
Белые кровяные тельца (рис. 17), или лейкоциты значительно отличаются от эритроцитов. Они имеют ядро, поэтому и являются истинными клетками крови. Лейкоциты лишены гемоглобина (поэтому бесцветны) и способны к активному движению: могут двигаться против тока крови и даже проскальзывать сквозь стенки кровеносных сосудов и внедряться в ткани. Лейкоциты далеко не так многочисленны, как эритроциты. Концентрация лейкоцитов у взрослого человека в норме составляет 4,9-9,0 × 109 клеток в литре. Величина этого показателя существенно варьирует в физиологических условиях, изменяясь у одного и того же человека в связи со временем суток, характером и тяжестью выполняемой работы, приемом пищи и другими факторами. Основная функция лейкоцитов – участие в защитных реакциях нашего организма. Лейкоциты не разрушаются в каком-либо определенном органе. Одни из них погибают под действием бактерий, другие проходят через эпителий пищеварительного тракта или мочевых путей и удаляются из организма с экскрементами или мочой. По морфологическим и тинкториальным признакам лейкоциты делят на зернистые (гранулоциты) – нейтрофильные, эозинофильные, базофильные и незернистые (агранулоциты) – лимфоциты и моноциты. Гранулоциты – нейтрофильные, эозинофильные, базофильные – это дифференцированные, специализированные клетки, содержат в цитоплазме гранулы, имеют дольчатое ядро, способны к фагоцитозу, но фагоцитируют, выйдя из кровотока в окружающие сосуд ткани. Разрушаясь, они выделяют ферменты и биологически активные вещества, оказывающие влияние на окружающие ткани и проницаемость капилляров. Их жизненный цикл складывается из возникновения и созревания в красном костном мозге, циркуляции в крови, участия в защитных реакциях и гибели в тканях. Нейтрофильные гранулоциты (нейтрофилы) – самые многочисленные, составляют 47-72 % от числа лейкоцитов. В крови находятся 8-12 ч., в тканях – 5-7 суток. По степени зрелости различают полиморфноядерные (ПМЯ) - 60-65%, палочкоядерные (П) - 1-6% и юные (Ю) - 0-0,5%. Показателем зрелости служит степень сегментации ядра. Ядро ПМЯ гранулоцита состоит из 2-5 сегментов, ядрышко не выявляется. Один из сегментов ядра имеет у женщин тельце Барра – половой хроматин – конденсированную Х-хромосому в виде барабанной палочки. У женщин половой хроматин встречается в одном ПМЯ гранулоците из 38, у мужчин – в 1 из 500. В цитоплазме зрелых нейтрофилов органелл мало, немного митохондрий, слабо выражен комплекс Гольджи. Количество гранул колеблется от 50 до 200. 80% составляют специфические гранулы, мелкие, окрашивающиеся в мазках в лиловый цвет. Поскольку в процессе развития нейтрофильных гранулоцитов эти гранулы появляются довольно поздно (на стадии миелоцита), их называют вторичными или миелоцитарными.
Они содержат щелочную фосфатазу, бактерицидные ферменты (лизоцим, лактоферрин), белок, связывающий витамин В12, и коллагеназу. Второй тип гранул – азурофильные, лизосомоподобные, появляются на более ранней стадии (промиелоцита), поэтому их называют первичными, или промиелоцитарными. В них содержится миелопероксидаза, набор разнообразных гидролитических ферментов, катионные белки, лизоцим и кислые гликозаминогликаны.
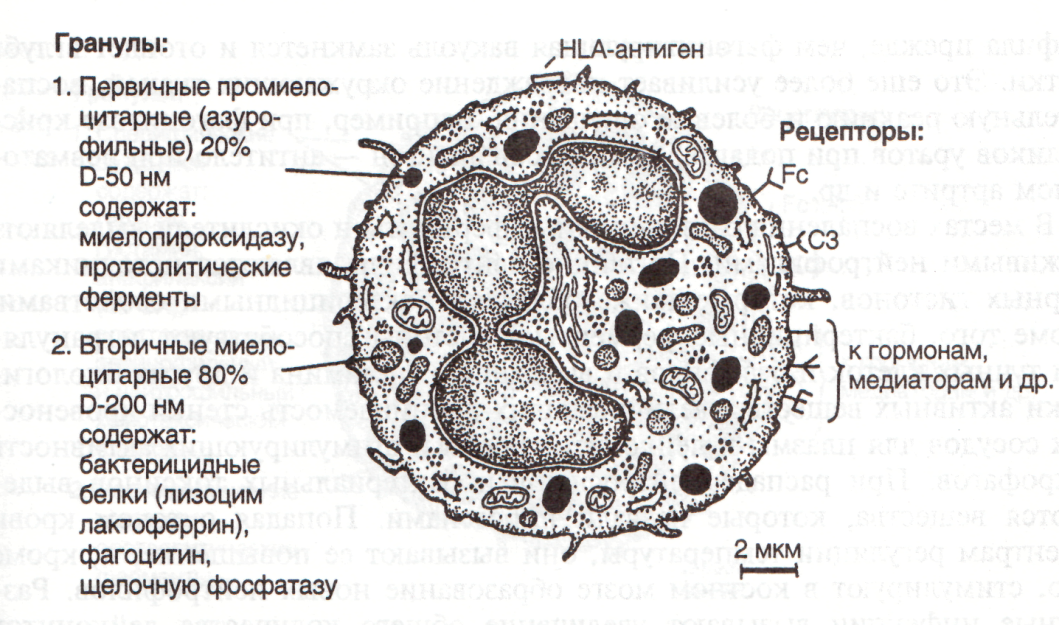
Рис.19. Нейтрофильный гранулоцит: HLA — антигены главного комплекса гистосовместимости I класса.Рецепторы: Fc — к иммуноглобулинам; С3 — к комплементу
Основная функция нейтрофильных гранулоцитов – это антибактериальная защита и участие в воспалительных реакциях. Их называют микрофагами. Наиболее активны они при кислых значениях рН. Плазмолемма, кроме HLA-антигенов, Fc-рецепторов к антителам и СЗ-рецепторов к СЗ компоненту комплемента, имеет рецепторы к адренергическим и холинергическим агентам, гистамину, простагландинам, кортикостероидам и др. (рис. 19). Через Fc-рецептор антитела к микробам фиксируются на плазмолемме, связываясь с микробами, окутанными антителами. Через СЗ-рецептор осуществляется связывание с микробами, покрытыми белками комплемента. В обоих случаях такой контакт резко изменяет метаболизм нейтрофила и приводит к образованию и выбросу мощных биооксидантов (О2- и Н2О2 - ), что называют респираторным взрывом. Одновременно начинается фагоцитоз. Фагосома сливается вначале со специфической гранулой. Ее содержимое умерщвляет бактерию. Затем фагосома сливается с азурофильной гранулой и тогда происходит разрушение бактерии под действием гидролитических ферментов. Процесс фагоцитоза иногда бывает настолько бурным, что лизосомные гидролитические ферменты выделяются из нейтрофила прежде, чем фагоцитирующая вакуоль замкнется и отойдет вглубь клетки. Это еще более усиливает повреждение окружающих тканей, воспалительную реакцию и болевые ощущения, например, при фагоцитозе кристалликов уратов при подагре, комплексов антиген – антитело при ревматоидном артрите и др. В местах воспаления бактерицидные ферменты и окислители выделяются живыми нейтрофилами. Погибшие нейтрофилы являются источниками ядерных гистонов, которые также обладают бактерицидными свойствами. Кроме того, бактерицидные ферменты и гистоны способствуют дегрануляции тучных клеток и базофилов и выделению гистамина и других биологически активных веществ, увеличивающих проницаемость стенки кровеносных сосудов для плазмы и лейкоцитов крови и стимулирующих активность макрофагов. При распаде нейтрофилов и бактериальных токсинов выделяются вещества, которые назвали пирогенами. Попадая с током крови к центрам регуляции температуры, они вызывают ее повышение, и, кроме того, стимулируют в костном мозге образование новых нейтрофилов. Различные инфекции вызывают увеличение общего количества лейкоцитов в крови – лейкоцитоз. В этих случаях в кровь выходят и не вполне зрелые лейкоциты. Для нейтрофилов – это юные (метамиелоциты) и палочкоядерные формы. Они отличаются от зрелых формой ядра. Чем моложе клетка, тем менее сегментировано ядро. При увеличении количества незрелых форм говорят о сдвиге лейкоцитарной формулы влево. Свои основные функции – фагоцитоз бактерий и участие в воспалении – нейтрофилы проявляют вне сосудов – в тканях. Базофильные гранулоциты (базофилы) – самые малочисленные, составляют 0,5-1% от числа лейкоцитов. Диаметр в мазке – 10-12 мкм. В кровотоке находятся 48 ч, в тканях погибают быстро. Ядро лопастное, органеллы малочисленны. Гранулы (в количестве около 400) метахроматичны, т. е. азуром II окрашиваются в фиолетовый цвет благодаря высокому содержанию кислых протеогликанов. Выделяют специфические и неспецифические азурофильные лизосомоподобные гранулы (рис. 20). Специфические гранулы диаметром до 1,5 мкм содержат пероксидазу, гистамин, гепарин, медленно реагирующую субстанцию анафилаксии, АТФ, факторы хемотаксиса нейтрофилов и эозинофилов. Гепарин препятствует свертыванию крови, предотвращает образование кровяного сгустка и фибрина. Гистамин повышает проницаемость базальной пластины и основного вещества соединительной ткани, чем способствует выходу плазмы и форменных элементов крови, развитию отека и воспаления. Медленно реагирующая субстанция анафилаксии вызывает стойкое сокращение мышечных клеток стенки бронхов, расширение и проницаемость стенки сосудов. Базофилы крови по содержимому гранул и биологическому действию сходны с тучными клетками соединительной ткани. Те идругие имеют на плазмолемме рецепторы к иммуноглобулинам класса Е, которые могут образовываться в организме в результате бурной иммунной реакции на различные антигены – аллергены. IgE через рецепторы фиксируются на этих клетках и при повторном контакте с тем же аллергеном связываются с ним.
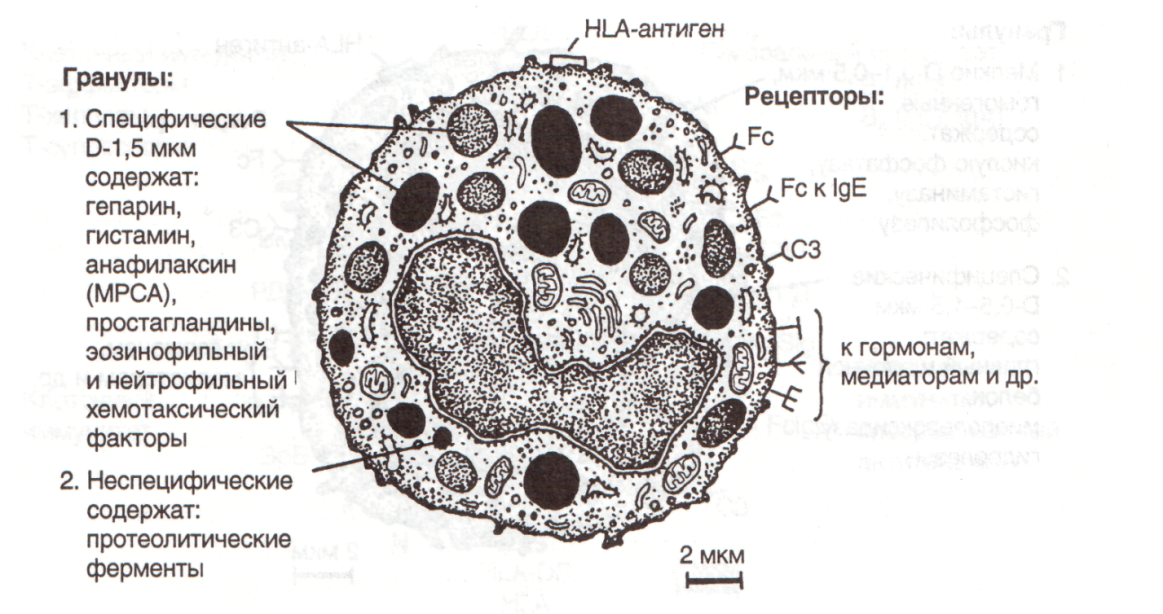
Рис.20. Базофильный гранулоцит: HLA — антигены главного комплекса гистосовместимости I класса. Рецепторы: Fc — к иммуноглобулинам; СЗ — к комплементу; Fc к IgE — к иммуноглобулинам класса Е В результате гранулы выходят из клеток. Проявлением этих воздействий могут быть мгновенные высыпания, волдыри, отеки и удушье – аллергические реакции немедленного типа, вплоть до анафилактического шока со смертельным исходом. Базофилы могут принимать участие в кожной реакции гиперчувствительности замедленного типа на введение антигенов разного происхождения, а также в образовании инфильтратов в других органах (дыхательных путях, почках). Как и другие гранулоциты, они способны к фагоцитозу и образованию биооксидантов (H2О2- и О2-). Основную функцию базофилов крови можно определить как регуляцию процессов свертывания крови и проницаемости сосудов, участие в иммунных реакциях. Эозинофильные гранулоциты (эозинофилы) составляют 0,5-5% от числа лейкоцитов (рис. 21). Для эозинофилов характерны суточные колебания – максимальное количество в крови ночью, минимальное – утром. Диаметр их составляет 12-17 мкм. В крови эозинофилы находятся 7-12 ч, в тканях 8-12 суток. Несмотря на малое количество в крови, в тканях их довольно много: в костном мозге в 200, а в соединительной ткани в 500 раз больше. По степени зрелости в крови они, как и в случае нейтрофилов, могут быть сегментоядерные (2-5 сегментов), палочкоядерные и юные. Среди органелл заметно развиты митохондрии, рибосомы и комплекс Гольджи. Эозинофилы содержат до 200 специфических и неспецифических гранул. Специфические гранулы (около 0,5—1,5 х 0,3 мкм) покрыты мембраной, могут содержать кристаллоид из главного основного белка с большим содержанием аргинина, окрашивающегося кислыми красителями.
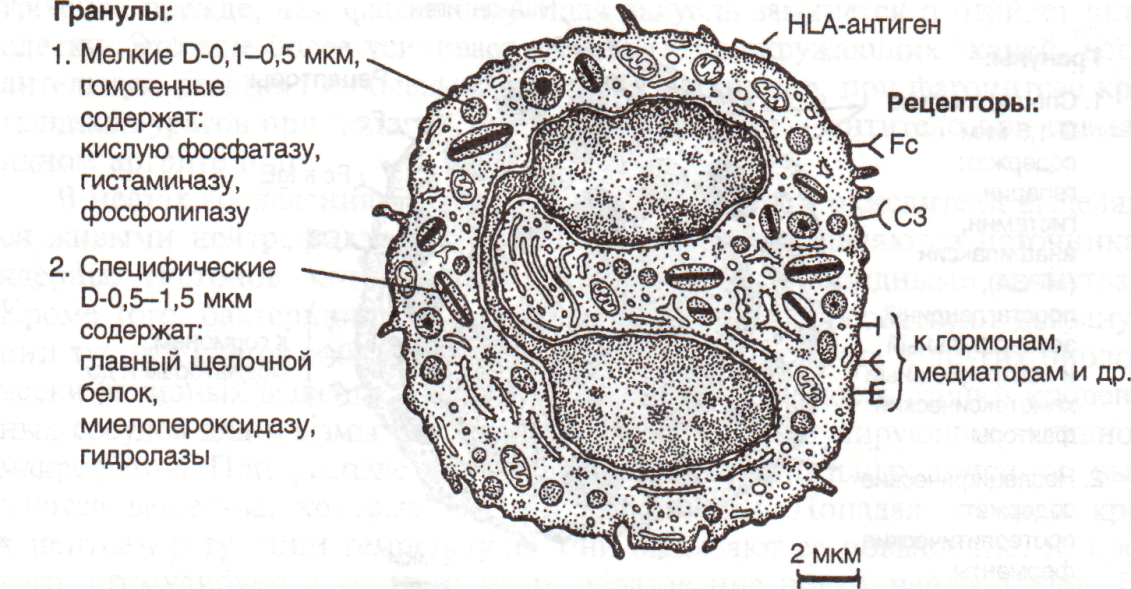
Рис.21. Эозинофильный гранулоцит: HLA — антигены главного комплекса гистосовместимости I класса. Рецепторы: Fc — к иммуноглобулинам; СЗ — к комплементу Главный основной белок обладает способностью убивать бактерии, разрушать кутикулу паразитов и нейтрализовать гепарин. В них содержится также миелопероксидаза и ряд гидролитических ферментов. Гранулы второго типа более мелкие (0,1-0,5 мкм), гомогенные, в их составе определены арилсульфатаза, гистаминаза, кислая фосфатаза. Гистаминаза разрушает гистамин, арилсульфатаза – медленно реагирующую субстанцию анафилаксии. Эозинофилы обладают хемотаксисом по отношению к гистамину, лим-фокинам (медиаторы лимфоцитов), комплексам антиген – антитело. Они способны фагоцитировать и накапливать гистамин, кроме того, выделяют фактор, тормозящий выброс гистамина базофилами и тучными клетками. Они последними перемещаются в очаги воспаления и способствуют устранению воспалительных реакций. Эозинофилы активно участвуют в проти-вопаразитарной защите. При контакте с паразитами выделяют на их поверхность ферменты, катионные белки и биооксиданты, способные разрушать кутикулу. При аллергических реакциях, гельминтозах и других паразитарных болезнях их содержание в периферической крови повышается. Функции эозинофила можно определить как ограничение местных воспалительных реакций, противопаразитарную защиту, участие в обезвреживании ядов и токсинов. Агранулоциты. К агранулоцитам относят лимфоциты и моноциты. Лимфоциты (рис. 22) составляют 19-37% лейкоцитов, и по размерам их делят на малые – 4,5-6 мкм в диаметре, средние 7-10 мкм и большие – 10 мкм и более. Размер лимфоцита обусловлен степенью его зрелости и состоянием иммунологической активности. Не вполне зрелые, а также активированные антигеном лимфоциты относятся к средним и большим.
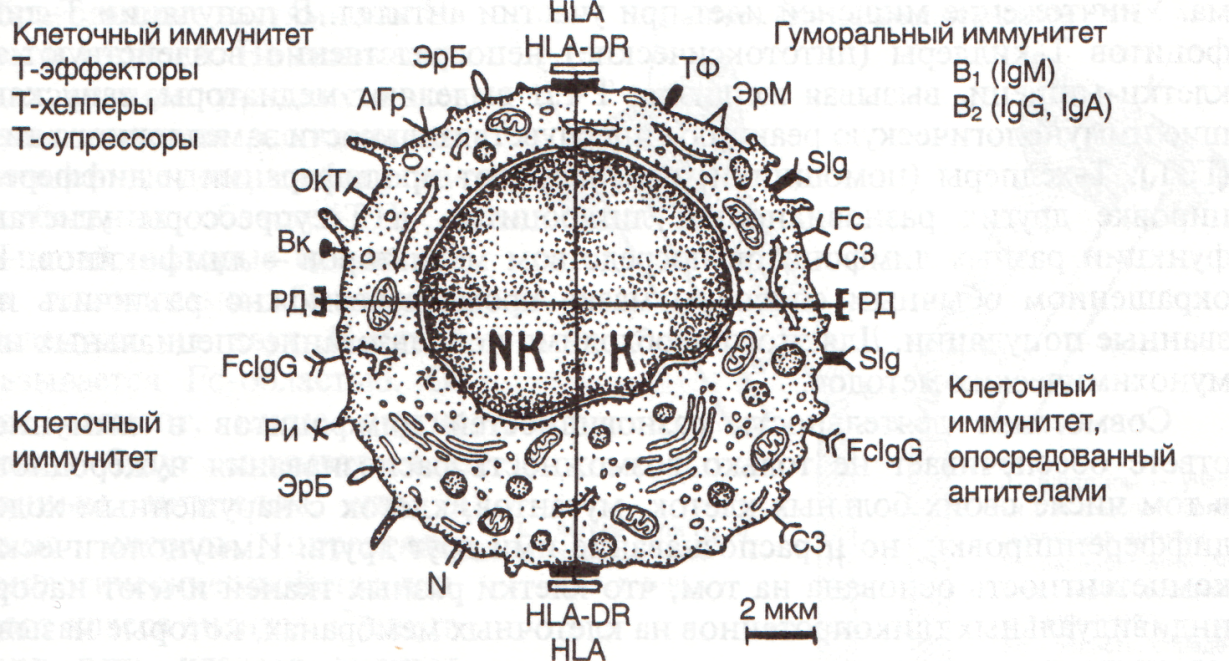
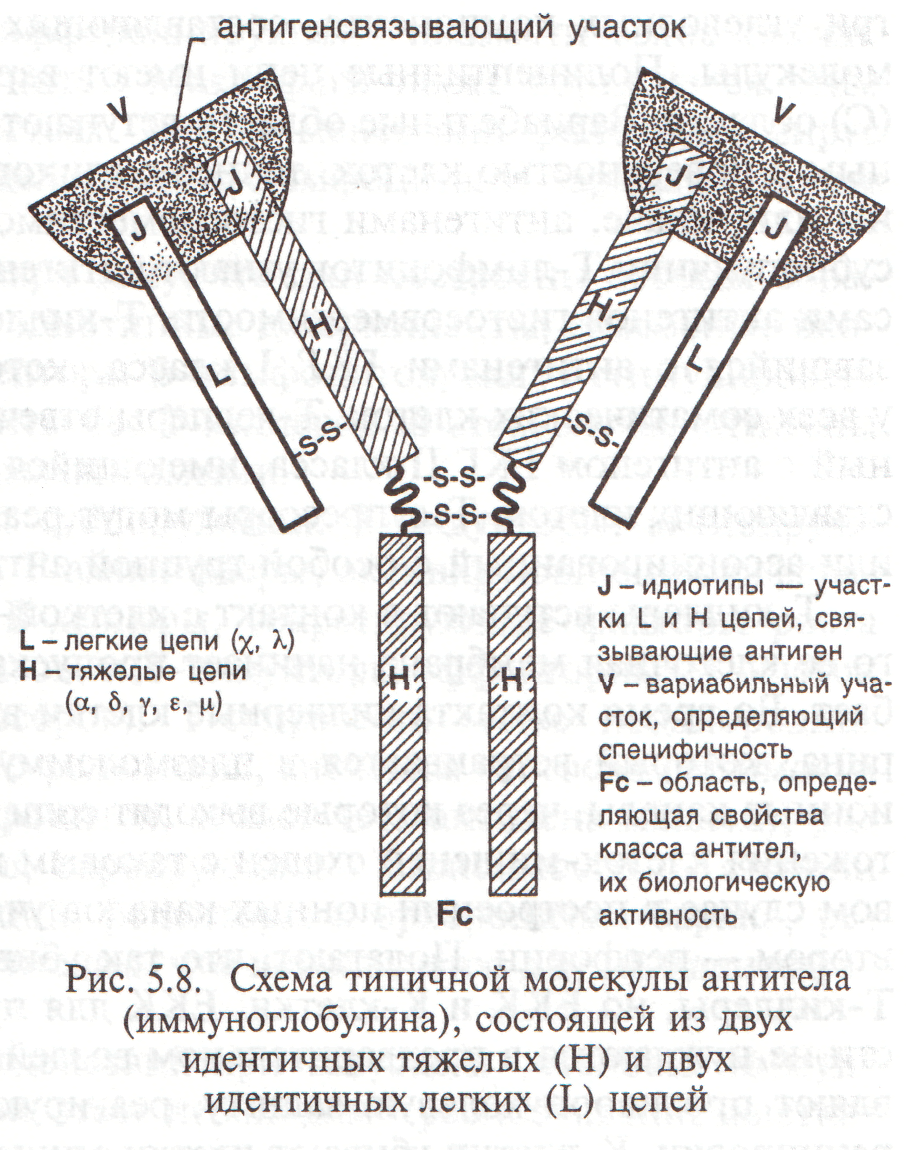
Рис.22. Лимфоциты. Популяции и субпопуляции отличаются совокупностью рецепторов и других компонентов клеточной оболочки, определяющих их участие в иммунных реакциях. Т-, В-, NK - и К-клетки — популяции лимфоцитов; HLA и HLA - DR — антигены главного комплекса гистосовместимости I и II класса соответственно. Рецепторы: ЭрБ — к эритроцитам барана; АГр — рецептор к антигенам; ОкТ — антигены к гибридомным антителам; Вк — к вирусу кори; РД — к факторам роста и дифференцировки; Ри — к интерферону; Fc IgG — к иммуноглобулинам класса G; СЗ — к СЗ компоненту комплемента; SIg (M, D, G, А, Е) — поверхностные иммуноглобулины, рецепторы к антигенам; ЭрМ — к эритроцитам мыши; ТФ — к медиаторам Т-лимфоцитов. N — NK антиген Малые лимфоциты имеют совсем немного цитоплазмы (на препаратах – в виде узкого базофильного ободка вокруг ядра). Хроматин плотно конденсирован. У средних и больших лимфоцитов ядро менее плотное. При ультрамикроскопии выявляют рибосомы, небольшое количество митохондрий, единичные профили ГЭС, комплекс Гольджи. Некоторые средние и большие лимфоциты имеют в цитоплазме мелкие гранулы, их относят к естественным киллерным клеткам. В ядрах всех лимфоцитов обнаружены ядрышки. Главная функция лимфоцитов — это обеспечение иммунных реакций, защита от всего чужеродного, попадающего в организм или образующегося в нем. В основе этих реакций лежит способность лимфоцитов реагировать на чужеродные молекулы (антигены) при помощи рецепторов плазмолеммы. Совокупность этих рецепторов и других компонентов плазмолеммы определяет способ участия лимфоцитов в иммунных реакциях. По свойствам выделяют четыре основные группы клеток: Т-лимфоциты, В-лимфоциты, естественные киллерные клетки (ЕКК, или NK-клетки) и К-клетки. Т-лимфоциты, NK и К-клетки осуществляют клеточные формы иммунного ответа, при которых для уничтожения клетки-мишени нужен непосредственный контакт лимфоцита и клетки-мишени. В-лимфоциты и плазматические клетки ответственны за гуморальный иммунитет, они секретируют особые белки — антитела, поступающие в кровь и другие жидкости организма. Уничтожение мишеней идет при участии антител. В популяции Т-лимфоцитов Т-киллеры (цитотоксические) непосредственно воздействуют на клетки-мишени, вызывая их лизис; Т-гзт выделяют медиаторы, запускающие иммунологическую реакцию гиперчувствительности замедленного типа (ГЗТ), Т-хелперы (помощники) способствуют пролиферации и дифферен-цировке других разновидностей лимфоцитов, а Т-супрессоры угнетают функции разных лимфоцитов посредством медиаторов — лимфокинов. На окрашенном обычным способом мазке крови невозможно различить названные популяции. Для этого необходимо использование специальных им-мунохимических методов. Совместная деятельность разновидностей лимфоцитов в иммунном ответе обеспечивает не только возможность распознавания чужеродного, в том числе своих больных клеток, мутантов, клеток с нарушенным ходом дифференцировки, но и распознавание ими друг друга. Иммунологическая компетентность основана на том, что клетки разных тканей имеют наборы индивидуальных гликопротеинов на клеточных мембранах, которые называют антигенами гистосовместимости, или трансплантационными антигенами. Главные антигены гистосовместимости синтезируются в клетке под контролем комплекса генов иммунного ответа – главного комплекса гистосовместимости (ГКГ или на англ. МНС). У человека ГКГ расположен в коротком плече 6-й хромосомы. Поверхностные антигены ГКГ бывают двух классов. I класс (HLA—антигены) есть на всех соматических клетках, II класс (HLA-DR—антигены) на В-лимфоцитах, активизированных Т-лимфо-цитах и антиген-представляющих клетках (макрофагах, дендритных, интер-дигитирующих). Лимфоциты способны различать антигены ГКГ своих и чужих клеток. В основе распознавания лежит химическая реакция связывания молекул рецепторов лимфоцитов с молекулами антигенов. Эта реакция специфична. Каждому антигену соответствует только определенный рецептор и определенный лимфоцит. Антигенспецифические рецепторы В-лимфоцитов – это антитела, или точнее, белки иммуноглобулины (Ig) преимущественно классов М и D. Их называют поверхностными иммуноглобулинами, обозначая SIg. Каждый В-лимфоцит имеет около 105 таких молекул-рецепторов. Когда к рецепторам присоединяется антиген, В-лимфоцит активируется, многократно делится, и его многочисленные потомки начинают секретировать растворимые антитела с одинаковыми антиген-связывающими участками к данному конкретному антигену. Антитела поступают в тканевую жидкость, лимфу, кровь. Потомки активированного В-лимфоцита заканчивают свою дифференцировку, преобразуясь через плазмобласт в плазматическую клетку, которые интенсивно секретируют антитела. Каждая молекула антитела (рис. 23) состоит из двух идентичных тяжелых (Н) полипептидных цепей и двух идентичных легких (L). Тяжелые цепи имеют V-образную форму, легкие расположены параллельно тяжелым, но только в области ветвей. На концах ветвей находятся антигенсвязывающие участки, образованные частями как Н- так и L-цепей. На связывающих антиген участках молекулы антитела расположены антигенные детерминанты вариабельных областей Н- и L-цепей, которые называются идиотипами. Основание молекулы из двух Н-цепей называется Fc-областью. От нее зависит, какие другие белки будут связываться с данным антителом, что, в свою очередь, определяет биологические свойства данного класса антител. Существует пять классов антител: IgA, IgD, IgE, IgG, IgM, имеющие различные Н-цепи: α, β, ε, γ, μ. L-цепи бывают двух типов: χ и λ. С любым классом Н-цепей могут быть связаны L-цепи любого типа. Различные сочетания Н- и L-цепей обеспечивают миллионы разновидностей антител с уникальными участками – идиотипами – для связывания антигенов. Антитела инактивируют вирусы, бактериальные токсины, оседая на микроорганизмах, фиксируют на них особые белки плазмы крови – систему комплемента, в результате чего микробы погибают. Белки системы комплемента в этом случае встраиваются в клеточную оболочку и формируют ионные каналы, пропускающие воду, что приводит к набуханию и гибели клетки-мишени. Фиксация антител на микроорганизмах способствует поглощению их фагоцитами и уничтожению NK-клетками и К-клетками. Помимо уникальных для каждого В-лимфоцита иммуноглобулиновых рецепторов имеются Fc-рецепторы с единой для всех В-лимфоцитов специфичностью и СЗ-рецепторы к комплементу. Важным поверхностным компонентом, как уже говорилось, являются антигены HLA-DR (Iа – у мыши), обеспечивающие взаимодействие с активированными Т-лимфоцитами. В-лимфоциты человека имеют рецепторы и к эритроцитам мыши, так что образуют с ними розетки, что используется для их выявления. Определены также рецепторы к цитокинам, митогенам и др., а также дифференцировочные антигены, входящие в характеристики популяции и субпопуляций. Антигенспецифические рецепторы Т-лимфоцитов являются гликопротеидами, построенными из двух полипептидных цепей (альфа и бета), имеющих сходные размеры и организацию.
Рис.23. Схема типичной молекулы антитела (иммуноглобулина), состоящей из двух идентичных тяжелых (Н) и двух идентичных легких (L) цепей
К каждой из них присоединено по три углеводных компонента, составляющих в целом до трети всей массы молекулы. Полипептидные цепи имеют вариабельную (V) и константную (С) области. Вариабельные области вступают в контакт с антигеном, связанным с поверхностью клеток, точнее с гликопротеинами клеточной мембраны или, иначе, антигенами гистосовместимости (продуктами ГКГ). Разные субпопуляции Т-лимфоцитов узнают антиген в ассоциации с разными классами антигенов гистосовместимости. Т-киллеры реагируют на антиген, связавшийся с антигенами ГКГ I класса, которые, как сказано ранее, есть у всех соматических клеток. Т-хелперы отвечают на антиген, ассоциированный с антигеном ГКГ II класса, имеющийся у лимфоцитов и антиген-пред-ставляющих клеток. Т-супрессоры могут реагировать на антиген в растворе или ассоциированный с особой группой антигенов ГКГ II класса. Т-киллеры вступают в контакт с клеткой-мишенью, в результате которого ее клеточная мембрана начинает пропускать внутрь воду, и клетка погибает. Во время контакта киллерные клетки выделяют гранулы белка перфорина, который встраивается в плазмолемму клетки-мишени и формирует ионные каналы, через которые выходят соли и входит вода. Механизм уничтожения клеток-мишеней сходен с таковым при гуморальном ответе: в первом случае в построении ионных каналов участвуют белки комплемента, во втором – перфорин. Полагают, что так убивают клетки-мишени не только Т-киллеры, но ЕКК и К-клетки. ЕКК для проявления киллерной активности не нуждаются в предварительном воздействии антигенов. Они осуществляют противоопухолевую защиту, реагируют на белки клеточной диффе-ренцировки. К-клетки убивают клетки-мишени, если на клеточных оболочках последних предварительно осели антитела, к которым К-клетки имеют рецепторы. Все виды киллерных клеток принимают участие в отторжении трансплантатов. В некоторых случаях на месте локализации антигена развивается реакция гиперчувствительности замедленного типа (ГЗТ), в результате которой разрушаются собственные клетки, пораженные микроорганизмами. Т-киллеры в данном случае называют Т-эффекторами ГЗТ (Т-гзт). При развитии реакции ГЗТ антиген поглощается макрофагами, затем частично обработанный экспрессируется на его мембране и распознается Т-гзт. Последний сек-ретирует медиаторы – хемотаксические факторы, привлекающие моноциты, макрофаги и гранулоциты. В результате возникает местное воспаление. Т-хелперы и Т-супрессоры относят к регуляторам иммунных реакций. Т-хелперы необходимы большинству В- и Т-лимфоцитов для осуществления ответа на антиген. Получив информацию об антигене, Т-хелперы выделяют ряд медиаторов, в частности, хелперный фактор для дифференцировки и включения синтеза антител в В-лимфоцитах, интерлейкин-2, активирующий Т-киллеры, фактор, ингибирующий миграцию макрофагов (ФИМ). Роль Т-хелперов наглядно выступает при заболевании СПИД. Вирус иммунодефицита человека (ВИЧ) проникает в Т-хелперы, поражая их, через специфические рецепторы. При заражении вирусом Т-хелпера его клон не может дать нормальное количество клеток. В-лимфоциты лишаются необходимых хелперных факторов и не дифференцируются в плазматические клетки. Нарушается гуморальный иммунитет. Макрофаги также поражаются этим вирусом, но в меньших количествах. Тем не менее, они фиксируют вирус на плазмолемме и при взаимодействиях с лимфоцитами заражают новые клетки. Некоторые антигены, благодаря тому, что они построены особым образом и содержат повторяющиеся однотипные детерминанты, способные блокировать одновременно все рецепторы В-лимфоцитов, могут стимулировать их дифференцировку в плазмоциты без Т-хелперов. В этом случае антигены и ответ на них называют тимуснезависимыми. Среди Т-хелперов выделяют субпопуляции: Т-индукторы, активирующие вспомогательные А-клетки, Т-амплифаеры, активирующие пролиферацию разных Т-лимфоцитов, Т-В-хелперы, секретирующие факторы роста и дифференцировки В-лимфоцитов, и Т-индукторы эффекторных Т-клеток (Т-В-хелперов, Т-гзт, Т-супрессоров). Т-супрессоры тоже неоднородны. Т-лимфоциты человека имеют Fc-рецепторы, антигены гистосовместимости HLA-DR и Р 25 (маркер Т-лимфоцитов, аналог тета-антигена мышей), ряд дифференцировочных антигенов, варьирующих в зависимости от степени дифференцировки и субпопуляций, рецепторы к эритроцитам барана, рецепторы к моноклональным антителам, что используется для их идентификации. Регуляция клеточных взаимодействий при запуске и остановке иммунных реакций очень сложна. При этом необходимо распознавание клетками-участницами не только антигенов, но и друг друга. Так, окончание гуморального ответа на антиген отчасти обусловлено связыванием его секретируемыми антителами, в результате чего антиген перестает присоединяться к рецепторам новых В-лимфоцитов и активация их прекращается. Наряду с этим, вероятно, работает и другой механизм, получивший название иммунологической сети, модель которой предложена Н. Ерне в 1974 г. Согласно этой модели, рецептор В-лимфоцита, являясь антителом, или иммуноглобулином, имеет свой набор антигенных детерминант – идиотипов. Полагают, что в организме против каждого собственного идиотипа вырабатываются антитела, следовательно, против каждого рецептора есть антирецептор. При попадании в организм антигена А размножается клон анти-А, или идиотип А. Этот клон тоже начнет размножаться, а остановит его новый клон-антиидиотип против антиидиотипа А и т. д. Антиидиотип всегда супрессор. Считается, что рецепторы супрессоров — антиидиотипы. Размеры такой идиотипической сети могут быть огромны, так как каждый лимфоцит, взаимодействующий с анти-А-лимфоцитом, может сходным образом реа
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 145; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.234.62 (0.041 с.) |