
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Список используемых сокращенийСтр 1 из 14Следующая ⇒
Реферат
В данной работе проведено исследование реакции ацилирования лигнина о-аминобензойной кислотой в среде «тионилхлорид - трифторуксусная кислота». В результате проведенных исследований были синтезированы продукты ацилирования, определено содержание связанной кислоты потенциометрическим методом, проведено исследование методом ЯМР и ИК-спектроскопии. На основе полученных данных рассчитаны константы скорости реакции и термодинамические параметры активированного комплекса реакции ацилирования. Дипломная работа содержит: 115 страниц печатного текста, 5 рисунков, 16 таблиц и 49 литературных источников. Список используемых сокращений
ФПЕ - фенилпропановые единицы; ЦБП - целлюлозно-бумажная промышленность; ЛСК - лигносульфоновые кислоты; ЖЛС - железолигносульфонатный комплекс; ФЦК - феррицианид калия; ЛЦМ - лигнинцеллюлозный материал КМЦ - АКК - ароматическая карбоновая кислота; СЭЦ - сложный эфир целлюлозы; о-АБК -о-аминобензойная кислота; о-АБЛ-о-аминобензоат лигнина; ТФУК - трифторуксусная кислота; ТХ - тионилхлорид; ИК - инфракрасный; ЯМР - ядерно-магнитный резонанс; ТОЗМ - теория объёмного заполнения микропор; НИР - научно-исследовательская работа; Введение
Одна из актуальных задач рационального природопользования - решение проблемы утилизации крупнотоннажных промышленных отходов. Накопленные промышленные отходы занимают значительные земельные территории, выступают источником загрязнения окружающей среды, следствием чего является ухудшение условий жизни человека. Количество некоторых углеродсодержащих отходов столь велико, что их рассматривают как вторичные техногенные сырьевые ресурсы. Лигнин как составная часть древесины наиболее трудноутилизируемый отход, который образуется при ее химической переработке на целлюлозно-бумажных и гидролизных предприятиях. С другой стороны, он потенциальный сырьевой ресурс для многих стран. В настоящее время отсутствуют исчерпывающие технические решения по утилизации лигнинов, хотя обзор научной литературы последних лет свидетельствует о возрастающем интересе исследователей к этому сырьевому ресурсу. Целью данной работы является ацилирование сульфатного лигнина для получения о-аминобензоатов и расчет кинетических закономерностей и термодинамических параметров активированного комплекса, изучение сорбционных свойств полученных сложных эфиров лигнина.
Литературный обзор
Древесина
Древесина является материалом биологического происхождения, и большая часть вещества древесины состоит из высокомолекулярных соединений. В абсолютно сухом состоянии древесина на 99 % состоит из органических соединений. На долю неорганической части древесины в среднем приходится 1 %. Элементарный химический состав органической части древесины всех пород практически одинаков. Абсолютно сухая древесина содержит в среднем 49-50 % углерода, 43-44 % кислорода, около 6 % водорода и 0,1-0,3 % азота [1]. Эти химические элементы образуют сложные химические соединения: целлюлозу, лигнин, гемицеллюлозы и экстрактивные вещества. Содержание органических веществ в древесине зависит от породы, возраста и других факторов. Древесина осины содержит меньше лигнина, больше легкогидролизуемых полисахаридов, более реакционноспособна в реакциях ацилирования и содержит все мономерные составляющие единицы лигнина. Лигнин входит в состав всех наземных растений, занимая в растительном мире по количеству второе место после целлюлозы. В одревесневших клеточных стенках аморфный лигнин скрепляет полисахаридные структуры, заполняет пустоты между фибриллами целлюлозы и гемицеллюлоз, придает механическую прочность и устойчивость стволам и стеблям растений. Лигнин придает гидрофобность проводящим клеткам древесины. Лигнин не содержится в грибах, водорослях и лишайниках. Лигнин
Лигнин (от лат. lignum - дерево, древесина) представляет собой природный полимер, характеризующее одеревеневшие стенки растительных клеток. Лигнин - аморфное вещество от светло-кремового до темно-коричневого цвета (в зависимости от способа выделения), молекулярная масса растворимых лигнинов от 1 до 150 тыс., плотность 1,25-1,45 г/см3. Лигнин окрашивается основными красителями и даёт цветные реакции, характерные для фенолов. Лигнин проявляет пластические свойства при повышенном давлении и температуре, особенно во влажном состоянии. Принято различать протолигнин - лигнин содержащийся внутри растения в его естественной форме, и технические его формы, полученные извлечением из растительной ткани при помощи различных физикохимических методов.
Массовая доля лигнина в древесине хвойных пород составляет в среднем 27-30 %, а в древесине лиственных пород 18-24 % [2]. В отличие от целлюлозы и других полисахаридов, выделенный из древесины лигнин не является индивидуальным веществом, а представляет собой смесь ароматических полимеров родственного строения. Для лигнинов древесины характерны цветные реакции с рядом органических и неорганических реагентов, используемые для установления одревеснения: например, с флороглюцином - реакция Визнера. Препарат пропитывают 12 %-ной соляной кислотой и затем наносят каплю 5-10 %-го спиртового раствора флороглюцина. Одревесневшие клетки приобретают пурпурно-красную окраску или характерную фиолетовую окраску, интенсивность которой зависит от степени лигнификации. Цветные реакции на лигнин используются при микроскопических исследованиях срезов древесины. Часто применяют реакцию с перманганатом калия (реакция Мейле). При этом срезы древесины обрабатывают в течение 5 мин. 1 %-м раствором перманганата, промывают водой, смачивают слабой соляной кислотой, опять промывают, затем смачивают раствором аммиака. Препарат лиственной древесины окрашивается в красный, а хвойной - в желтоватый цвет. Основная масса природного лигнина в древесине имеет пространственную (трехмерную сетчатую, возможно, фрактальную) структуру и химически связана с гемицеллюлозами. Поэтому лигнин не способен растворяться в воде и органических растворителях. Для перевода лигнина в растворимое состояние требуется его частичная деструкция, разрушение химических связей. Понятие макромолекулы для лигнинов является условным, обычно рассматривают структурные схемы, отображающие статистический набор установленных фрагментов и связей того или иного препарата лигнина. Среди выделенных лигнинов различают препараты нерастворимых и растворимых лигнинов. Нерастворимые лигнины сохраняют сетчатую структуру. Растворимые лигнины, представляющие фрагменты сетки имеют разветвлённую структуру с высокой степенью разветвлённости и неоднородны по молекулярной массе. Лигнин выделяют из предварительно экстрагированной древесины в присутствии кислотных катализаторов, необходимых для ускорения гидролиза связей лигнина с гемицеллюлозными компонентами клеточной стенки, и, частично, эфирных связей собственно лигнина. Реагенты и растворители, применяемые для извлечения лигнина из древесины, часто связываются химически с лигнином, образуя его производные, менее склонные к реакциям конденсации (сшивания цепей), чем лигнин. Реакции конденсации лигнина, так же как и процессы делигнификации древесины, катализируются кислотами. Лигнин не изготавливают специально, он и его химически модифицированные формы являются отходами биохимического производства. В ходе физико-химической переработки растительной ткани молекулярная масса лигнина уменьшается в несколько раз, а его химическая активность возрастает. Из раститительных тканей лигнин может быть выделен: растворением углеводных (полисахаридных) компонентов, например их гидролизом в присутствии минеральных кислот (сернокислотный и солянокислый лигнин); действием медноаммиачного раствора, представляющего собой раствор гидроксида тетраамминмеди (II) в 25 %-ном водном растворе аммиака [Cu(NH3)4](OH)2 (медно-аммиачный лигнин); окислением периодатом (периодатный лигнин); растворением самого лигнина (нагреванием в присутствии щелочи). В гидролизной промышленности получают порошковый гидролизный лигнин. В целлюлозном производстве образуются водорастворимые формы лигнина. Существуют две основные технологии варки целлюлозы [3], более распространенная сульфатная варка (щелочная) и менее употребляемая сульфитная (кислотная) варка. Лигнин, получаемый в сульфатном производстве - сульфатный лигнин в большой степени утилизируется в энергетических установках целлюлозных заводов. В сульфитном производстве образуются растворы сульфитных лигнинов (лигносульфонатов), часть которых накапливается в лигнохранилищах, а часть уходит со сточными водами предприятия в реки и озера.
Применение лигнина Лигнин - ценное химическое сырьё, уже используемое во многих производствах и в медицине. Лигнин самостоятельно как материал находит ограниченное применение. В основном, он идёт в отход или на производство топливных брикетов. Редкое использование связано также с взрывоопасностью лигнина, что затрудняет его переработку. Одним из вариантов использования лигнина является синтез его производных, в частности - ацилирование. Сульфатный лигнин ограниченно применяется в производстве полимерных материалов, фенолформальдегидных смол, и как компонент клеящих композиций в производстве ДСП, картона, фанеры и др. Гидролизный лигнин служит котельным топливом в лесохимических производствах, а также сырьем для получения гранулированного активного угля, пористого кирпича, удобрений, уксусной и щавелевой кислот, наполнителей. Ежегодно в мире получается около 70 млн. тонн технических лигнинов. В энциклопедиях пишут о том, что лигнин является ценным источником химического сырья. К сожалению, пока это сырье организационно, экономически и технически не слишком и не всегда доступно. Например, разложение лигнина на более простые химические соединения (фенол, бензол) при сравнимом качестве получаемых продуктов обходится дороже их синтеза из нефти или газа. По данным International Lignin Institute в мире используется на промышленные, сельскохозяйственные и другие цели не более 2 % технических лигнинов [3]. Остальное сжигается в энергетических установках или захоранивается в могильниках. Трудность промышленной переработки лигнина обусловлена сложностью его природы, многовариантностью структурных звеньев и связей между ними, а также нестойкостью этого природного полимера, необратимо меняющего свойства в результате химического или термического воздействия.
Структурные единицы лигнина Лигнин как полимер состоит из фенилпропановых структурных единиц (мономерных составляющих звеньев) - ФПЕ, обозначаемых сокращённо С6-С3, или единицы С9. Лигнин хвойных пород, появившихся в эволюции раньше лиственных, имеет более простое строение и состоит в основном из ФПЕ одного типа - гваяцилпропановых структурных единиц (I), в значительных количествах входят сирингилпропановые единицы (II) (рисунок 1). Гваяцилпропановые единицы (G-единицы) рассматривают как производные пирокатехина, а сирингилпропановые единицы (S-единицы) - как производные пирогаллола [4].
Рисунок 1 - Структурные единицы лигнина
В соответствии с основным типом структурных единиц лигнины хвойных пород относят к гваяцильным лигнинам, а лигнины лиственных пород - к гваяцилсиригильным лигнинам. Кроме гваяцилпропановых единиц в состав хвойных лигнинов входят в небольшом количестве, а в состав лиственных лигнинов в ещё меньшем n-гидроксифенилпропановые единицы (III) [4]. Лигнин - это органический гетероцепной кислородсодержащий полимер, но в отличие от полисахаридов, относящихся к полиацеталям у лигнина отсутствует единый тип связи между мономерными звеньями. Наряду с углерод-кислородными (простыми эфирными) связями С-О-С присутствуют и углерод-углеродные связи С-С между звеньями, характерные для карбоцепных полимеров. В структурных единицах лигнина содержатся различные полярные группы и в том числе способные к ионизации (кислые) фенольные гидроксилы и в небольшом числе карбоксильные группы, вследствие чего лигнин является полярным полимером, проявляющим свойства полиэлектролита. Лигнин - аморфный полимер, как природный, так и выделенный. Из-за высокой степени разветвлённости макромолекулы выделенных растворимых лигнинов имеют глобулярную форму, и такие препараты представляют собой порошки. В лигнине, благодаря наличию большого числа гидроксильных и других полярных групп, значительно развиты водородные связи (внутри- и межмолекулярные). Модификация лигнина
Древесина может рассматриваться как лигнинный пластик, усиленный целлюлозными волокнами. Лигнин в древесине можно модифицировать вместе с другими компонентами древесины путём пластикации (жидкий аммиак, мочевина, полиэтиленгликоль), ацетилирования, по реакции с фенолом и формальдегидом (использование древесной муки для производства фенолформальдегидных пластиков) и разделением волокна, используя пар высокого давления и последующее горячее прессование с получением твёрдого картона (процессы Мэйсонит и Асилунд) [7]. Многие миллионы тонн древесины перерабатываются ежегодно целлюлозно-бумажной промышленностью с целью отделения лигнина от целлюлозных волокон. Следовательно, отработанные щелока целлюлозного производства являются наиболее доступным источником лигнина.
Сульфатный лигнин (или тиолигнин) является главным компонентом чёрного щелока. Он может быть выделен с высоким выходом подкислением и последующим фильтрованием. В настоящее время, однако, из 85 сульфатных заводов США только один завод производит сульфатный лигнин для продажи. Производство его исчисляется 9 тыс. тонн в год. Это лишь одна десятая доля процента лигнина, получающегося в виде чёрных щелоков. Другая компания Crown Zellerbach использует черный щелок для производства диметилсульфоксида. Однако, если органические вещества производить для продажи, то они должны быть заменены каким-либо другим топливом, необходимым при регенерации химикатов. Следовательно. Стоимость любых продуктов из черного щелока должна быть достаточно высокой, чтобы компенсировать капиталовложения и расходы на дополнительное топливо вместо вложенного лигнина. Во многих отношениях сульфатный лигнин является более разносторонним материалом, чем лигносульфонаты. Он может быть легко выделен из отработанного щелока. Он достаточно реакционноспособен по отношению к этерификации, нитрованию, меркурированию и галогенированию. Он реагирует с фенолами, аминами, альдегидами и сульфидами. Реакция с сульфитом натрия приводит к образованию натриевых лигносульфонатов с различным содержанием сульфогрупп. Эти сульфированные лигнины дороже, чем лигносульфонаты, но они свободны от углеводов. В сульфитцеллюлозном производстве достигнут невысокий прогресс в деле регенерации химикатов. В последнее время использование лигнина из сульфитных щелоков снижается, что связано с общей тенденцией уменьшения производства сульфитной целлюлозы. Сульфитный способ окупает себя хорошо в производстве растворимых целлюлоз, но не может сравниться с сульфатным способом в производстве бумаги. Поэтому и в будущем предпочтение будет отдаваться сульфатному способу. Однако не исключена возможность увеличения производства и переработки сульфитных щелоков в связи с решением проблемы сточных вод. Разделение катионов Лигносульфонаты кальция могут быть легко превращены в сульфонаты других оснований при добавке растворимого сульфата желаемого катиона и осаждении ионов кальция в виде нерастворимого сульфата. Лигносульфонаты аммония, калия, железа, цинка, хрома и другие получаются этим способом. B лигносульфонатах аммония катион также может быть легко заменен на другие катионы при добавке соответствующих тидроокисей и способом ионообмена. Лигносульфонаты натрия и магния для замены основания требуют использования катионо- обменных смол. Ионообменный процесс Абиперм (Abitibi Power and Paper Company and Pfaudler Permutit Inc.) [13] был разработан с целью регенерации химикатов в процессе варки целлюлозы с бисульфитом натрия. Процесс заключается в пропускании отдутого отработанного щелока через слой пермутита Q (сульфированная полистирольная ионообменная смола), который удаляет катионы натрия и другие катионы из лигносульфонатов. Катионы удаляют из смолы обработкой сернистой кислотой, и получающиеся бисульфиты возвращают на целлюлозный завод. Полупромышленные исследования показали возможность регенерировать 80 % основания в щелоках на натриевом основании без ухудшения качества смолы. Другой патент на процесс такого типа был выдан Л. K- Свенсону. Причард-О. R. F. (Ontario Research Foundation) процесс предусматривает предварительное удаление нежелательных многовaлентных ионов. Этот процесс позволяет регенерировать около 80 % основания при содержании в получаемом растворе не более 1 % S02. Однако если в варочном щелоке надо более высокое содержание связанного S02, регенерация ухудшается. При содержании 2,25 % связанной серы удалось регенерировать только 54 % основания. B процессе Причард-Фраксон к сернистой кислоте добавляется ацетон, что приводит к понижению рН и адсорбции дополнительных количеств двуокиси серы. Кроме того, было найдено, что при удалении ацетона продувкой паром многовалентные ионы отделялись осаждением [13]. О-аминобензойная кислота
О-аминобензойная кислота (антраниловая кислота) NH2C6H4COOH представляет собой бесцветные кристаллы; температура плавления 145 °C; возгоняется, растворяется в воде, бензоле, эфирах; хорошо растворима в горячих хлороформе, этаноле, пиридине. Соли о-АБК со щелочными металлами, а также минеральными кислотами хорошо растворимы в воде; растворы обладают голубой флуоресценцией. При перегонке кислота декарбоксилируется до анилина. Она образует с Cd, Со, Cu (II), Ni, Zn, Pb и Hg в уксуснокислых растворах (рН 2,5-5) внутрикомплексные малорастворимые соединения, что используется для гравиметрического определения перечисленных элементов. Диазотирование о-АБЛ приводит к о-диазобензойной кислоте (является внутренней солью), которая при УФ-облучении образует дегидробензол. С солями Cu(II) в уксуснокислой среде образует ярко-зеленый осадок (м-аминобензойная кислот дает голубое окрашивание); в отличие от м- и n-аминобензойных кислот, при сплавлении её с небольшим избытком SnCl4 и обработке охлажденного плава водным раствором спирта появляется фуксино-красная окраска. В промышленности о-АБК получают: 1) действием водного раствора NH3 на фталевый ангидрид (рН 7,5-8,5; 40 °C) и последующим взаимодействием полученной Na-соли фталаминовой кислоты с раствором NaOCl при 60 °C (расщепление по Гофману): 2) действием на щелочной раствор фталимида NaOCl или NaOBr. Кислоту выделяют разбавлением HCl (40-50 °C); выход 84 %. Процесс может быть осуществлен периодическим или непрерывным способом.
Промежуточный продукт при синтезе индиго и других азокрасителей. Производные этой кислоты применяют в производстве азокрасителей и душистых веществ. Для парфюмерии наиболее важны эфиры NH2C6H4COOR - метилантранилат (R = CH3) и этилантранилат (R = С2Н5) имеющие запах цветов апельсинового дерева. Антраниловой кислотой при рафинации хлопкового масла высаживают токсичный полифенол госсипол, присутствие которого препятствует употреблению данного масла в пищу.
Экспериментальная часть
Подготовка лигнина
Для исследований использовали сульфатный лигнин.
Экстракция лигнина Поскольку лигнин содержит в своем составе смолы и талловые масла, которые затрудняют протекание реакции ацилирования, проводилось удаление экстрактивных веществ в аппарате Сокслета спиртобензольной смесью (соотношение 1:1 по объёму) в течение 8 часов [31].
Предгидролиз лигнина Наряду с экстрактивными веществами в состав древесины входят гемицеллюлозы, вступающие в реакцию наравне с целлюлозой, но из-за малой молекулярной массы (по сравнению с целлюлозой) они легко переходят в раствор при осаждении продукта. Для удаления гемицеллюлоз древесные опилки подвергались предгидролизу. Процесс происходил посредством кипячения древесных опилок в 0,5-1 %-ном растворе H2SO4 (модуль 1:50) в течении 4 часов, в дальнейшем смесь охлаждалась и промывалась дистиллированной водой до нейтральной среды по лакмусовой бумаге и высушивалась до постоянной массы. Полученный лигнин перед ацилированием выдерживался в эксикаторе над CaCl2 в течение недели для удаления остаточной влаги [32].
Подготовка исходных реагентов
Тионилхлорид дополнительно не очищали. О-аминобензойную кислоту дополнительно не очищали. Перегонке подвергалась - трифторуксусная кислота. Трифторуксусная кислота марки «ч.д.а.» перегонялась при атмосферном давлении в присутствии H2SO4 (в соотношении ТФУК: H2SO4 как 3:1 по объёму). Для синтезов использовалась фракция с Ткип.=72,4 °С.
Ацилирование лигнина
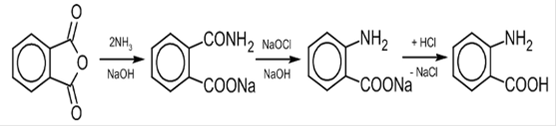
Ацилирование лигнина проводилось по ранее разработанной методике ацилирования карбоновыми кислотами с использованием ТФУК. Синтез проводился в круглодонной колбе, снабженной механической мешалкой, форштосом и обратным холодильником. В колбу помещали проэкстрагированный лигнин, и заливали предварительно приготовленной ацилирующей смесью, состоящей из о-АБК, ТФУК и ТХ. Приготовление смеси проводили следующим образом: растворяли определённое количество (эквивалентное навеске целлюлозосодержащего материала) ароматической кислоты в трифторуксусной кислоте, затем добавляли эквивалентное количество тионилхлорида. Полученную смесь выдерживали в течение 30 минут при выбранной температуре синтеза для взаимодействия тионилхлорида с ароматической кислотой [33,34]. Ацилирование лигнина проводили, варьируя время синтеза в пределах 1-5 часов в диапазоне температур 25-55 °С. Продукты тщательно отмывали от присутствующих, не прореагировавших, кислот на фильтре Шотта и сушили до постоянной массы на воздухе. Количество полученного продукта определяли в процентах относительно исходной навески лигнина по формуле (2.1):
где m1 - масса полученного продукта;0 - исходная навеска лигнинсодержащего сырья. Далее полученные продукты ацилирования лигнина исследовались методом ИК-спектроскопии и на содержание о-АБК методом потенциометрии.
ИК-спектроскопия
В связи с плохой растворимостью получаемых продуктов в доступных растворителях используется метод таблетирования суспензий исследуемых продуктов в бромиде калия на спектрофотометре ИКС-40 в интервале частот 4200-400 см-1. Интерпретацию спектров проводили с использованием справочных данных [35-37].
ЯМР-спектроскопия
Снятие ЯМР-спектров проводили на приборе BRUKER AVANCE III 300 WB. Спектры 13С высокого разрешения в твердом теле регистрировались на частоте 75 мГц с использованием стандартной методики кросс поляризации с подавлением протонов и вращением под магическим углом (CPMAS), время контакта 2000 мксек, время накопления FID 40 мсек, задержка между сканами 5 с, образец помещался в циркониевый ротор внешним диаметром 7 мм с крышкой из Kel-F и вращался с частотой 5 кГц. Производилось накопление 1024 сканов при комнатной температуре. Химический сдвиг отсчитывался относительно тетраметилсилана [38]. Обсуждение результатов
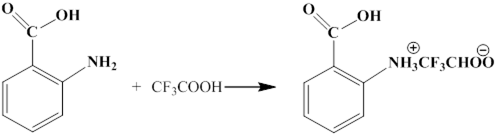
Проводимые на кафедре ТППиЭ АлтГТУ в течение нескольких лет исследования, показали возможность получения СЭЦ из целлюлозосодержащего сырья - древесины. В связи с тем, что получение лигнина с ароматическими кислотами не исследовано, представлялось интересным изучить взаимодействие лигнина с ароматическими кислотами, в частности с о-аминобензойной кислотой. Целью нашей работы было получение сложных эфиров лигнина с оАБК в среде «трифторуксусная кислота - тионилхлорид». Взаимодействие лигнина с ароматическими аминокислотами позволяет получить практически значимые продукты лигнина, которые могут быть использованы в различных областях народного хозяйства. Сульфатный лигнин в ходе проделанной работы обрабатывался ацилирующей смесью: о-аминобензойная кислота - трифторуксусная кислота - тионилхлорид. Трифторуксусная кислота в процессе ацилирования лигнина выполняет роль растворителя и катализатора реакции. Процесс ацилирования можно представить следующими стадиями: взаимодействие о-аминобензойной кислоты с ТФУК при интенсивном перемешивании;
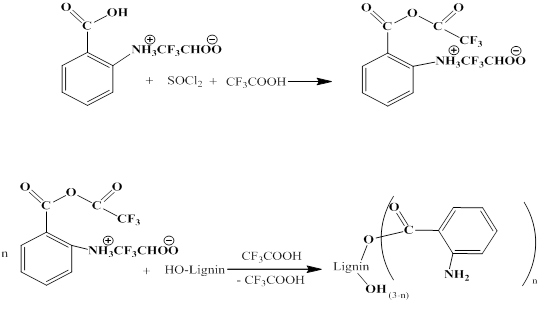
добавление тионилхлорида к смеси и выдерживание при постоянной температуре до полного взаимодействия:
По окончании реакции ацилированный лигнин высаждали в воду, промывали до нейтральной среды, высушивали и доводили до постоянной массы. В полученных соединениях определяли выход (в %), количество связанной о-аминобензойной кислоты. Количество полученного продукта определяли в процентах относительно исходной навески лигнина по формуле:
где m1 - масса полученного продукта; m0 - исходная навеска лигнина В таблице 1 приведены результаты определения выхода продукта ацилирования лигнина смесью «о-АБК - ТФУК - ТХ». Таблица 1 - Количество полученного продукта в процентах относительно исходной навески лигнина
В процессе ацилирования выход продукта составляет выше 100 % относительно исходной навески лигнина. Возрастание массы ацилированного лигнина происходит за счет присоединения ароматической кислоты, при этом возрастание выхода продукта с повышением времени и температуры синтеза коррелируется с данными по содержанию связанной кислоты. Для определения связанной кислоты использован метод потенциометрического титрования. По данным химического анализа на содержание связанной о-аминобензойной кислоты рассчитано количество связанных гидроксильных групп в лигнине, представленное в таблице 2.
Таблица 2 - Количество связанных гидроксильных групп в лигнине
Приведенные данные показывают, что с увеличением температуры и продолжительности синтеза возрастает количество связанных гидроксильных групп в лигнине. Как видно из полученных данных, количество прореагировавших гидроксильных групп лигнина больше исходного количества свободных алифатических и ароматических групп в чистом лигнине. Это связано с тем, что реакция протекает не только по свободным гидроксильным группам, но и по метоксильным и простым эфирным связям, которые становятся не устойчивыми в процессе ацидолиза. Реакция ацилирования данной системой начинается в гетерогенной среде и проходит на поверхности макромолекулы лигнина и является топохимической, поэтому обработку кинетических данных проводили по уравнению Ерофеева-Колмогорова:
ln[-ln(1 - α)] = lnk + n · lnτ, (3.2)
где α - степень превращения гидроксильных групп в сложноэфирные;- константа скорости реакции;- эмпирический коэффициент, учитывающий число элементарных стадий при превращении зародыша в активно растущее ядро и число направлений, в которых растут ядра; τ - время синтеза. Степень превращения рассчитывается по формуле:
где Сон - количество замещенных гидроксильных групп в полученных сложных эфирах лигнина в момент времени τ; Сон max - максимальное количество гидроксильных групп в лигнине, равное 34. Кинетика процесса ацилирования рассмотрена по уравнению 3.2 для топохимических реакций. По кинетической зависимости, представленной на рисунке 2, определены константы скорости реакции (коэффициент корреляции 0,94-0,97).
- 250С; 2 - 350С; 3 = 450С; 4 = 550С Рисунок 2 - Кинетические анаморфозы реакции ацилирования лигнина о-аминобензойной кислотой
В данных условиях реакции наблюдаются линейные зависимости (рисунок 1) между ln[-ln(1-a)] и ln t, на основании которых определяется lnK с применением метода Саковича по уравнению 3.4.
К = n∙k1/n, (3.4)
где n и k - эмпирические коэффициенты уравнения Ерофеева-Колмогорова;- константа скорости реакции в с-1. Термодинамические параметры реакции ацилирования вычисляли на основании уравнения Эйринга (3.5) при построении графика в координатах
Где К - константа скорости, ћ - постоянная Планка (6,62·10-34 Дж·с), Т - температура (К), Кb - постоянная Больцмана (1,38·10-23 ·Дж / К), ∆S¹ - энтропия активации (Дж / (моль·К)),- универсальная газовая постоянная (8,31 Дж / (моль·К), ∆Н¹ - энтальпия активации.
Рисунок 3 - Зависимость константы скорости реакции ацилирования лигнина о-аминобензойной кислотой от температуры Значение термодинамических параметров для реакции ацилирования лигнина о-аминобензойной кислотой составило для теплового эффекта реакции DH = 313 кДж/моль, энтропия активации DS = 612 Дж/моль·К. По найденным параметрам рассчитана свободная энергия Гиббса активации переходного комплекса реакции ацилирования лигнина м-аминобензойной кислотой, ее значение составляет 121,44 кДж/моль. Полученное значение энтальпии активации указывает на энергетические затраты, необходимые для диффузии ацилирующего агента к гидроксилам лигнина и образования переходного комплекса. Исходя из полученного значения энтропии активации, можно предположить, что происходит быстрое разрушение активированного комплекса с переходом в продукты реакции. Вычисленное значение энергии Гиббса активации переходного комплекса коррелируется с ранее полученными данными по сложным эфирам целлюлозы, синтезированными из древесины осины. Исходя из этого можно сделать предположение, что на реакцию ацилирования ароматическими кислотами не оказывает влияние вид растительного сырья (древесина, целлюлоза, лигнин), поскольку общая энергетика процесса имеет одинаковое значение. Анализ ацилированного лигнина методом ИК - спектроскопии (рисунок 4) показал наличие полос поглощения в области 3600-3400 см-1 характерных для полос поглощения валентных колебаний NH2 и OH-групп, при этом интенсивность полосы поглощения значительно ниже, чем у чистого лигнина и смещена к области 3200 см-1, что говорит о преобладании аминогрупп введенной кислоты. Полоса поглощения в области 1730 - 1750 см-1, имеющая большую интенсивность, характерна для валентных колебаний СО - групп в сложных эфирах, и подтверждает образование о-аминобензоата лигнина с высоким содержанием в связанном виде о-аминобензойной кислоты. Присутствие полос поглощения в областях 1610 - 1450 см-1, ответственных за колебания ароматического кольца, обосновывается присутствием структурных единиц остаточного лигнина, увеличивают свою интенсивность в связи с введением ароматической кислоты. Полоса поглощения в области 1730 см-1 увеличивает свою интенсивность с ростом температуры и продолжительности синтеза, что подтверждает увеличение количества прореагировавших гидроксильных групп лигнина. В ходе проведенных экспериментов были получены о-аминобензоаты лигнина с содержанием о-аминобензойной кислоты до 32 % от массы ацилированного лигнина. Методом ИК-спектроскопии доказано образование о-аминобензоата лигнина. Для полученных о-аминобензоатов лигнина, а также чистого лигнина были изучены сорбционные свойства на ионы поливалентных металлов: Cu2+, Pb2+, Th4+ (приложение Б). Предельная адсорбция насыщения и энергия адсорбции для различных ионов была рассчитана по уравнению Дубинина-Радушкевича (3.6) (таблица 3).
где А - величина равновесной адсорбции, мг/г; А0 - величина предельной адсорбции, мг/г;- универсальная газовая постоянная 8,31 Дж/(моль∙К); Т - температура, К; Е - энергия адсорбции катионов металлов, Дж/моль; С0 - исходная концентрация, мг/л; С - концентрация после адсорбции, мг/л;
Таблица 3- Предельная адсорбция насыщения и энергия адсорбции
Для определения предельной сорбционной емкости сорбента и исследования влияния температуры на распределение ионов меди в гетерогенной системе водный раствор - сорбент были получены изотермы сорбции тяжелых металлов при комнатных температурах. В исследованных процессах ионного обмена на сорбенте концентрация подвижных ионов в фазе сорбента при равновесии соизмерима с избыточной адсорбцией. Экспериментальные изотермы были обработаны в рамках модели сoрбции ТОЗМ. Обработка линейных зависимостей (lnA -ln(Cs/Cp) методом наименьших квадратов свидетельствует, что модель ТОЗМ удовлетворительно (с коэффициентом корреляции 0,97 - 0,99) описывает процесс, однако, дает несколько завышенные величины предельной сорбции. Известно, что предельная сорбция на немодифицированных лигноцеллюлозных сорбентах не превышает 1 моль/кг. Эта величина согласуется с содержанием карбоксильных групп в сорбенте. Вероятно, причина завышенной величины предельной сорбции по модели ТОЗМ связана с ионообменным механизмом сорбции ионов металлов целлюлозосодержащим сорбентом.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-03-14; просмотров: 101; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.240.224 (0.117 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 (2.1)
(2.1)
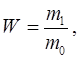 (3.1)
(3.1)
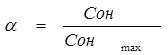 , (3.3)
, (3.3)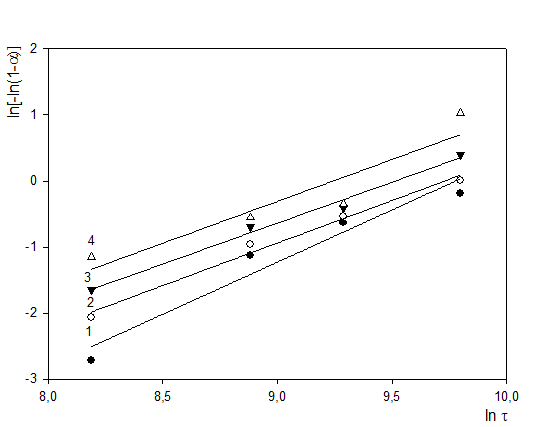
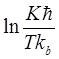 от 1/Т и на основании данного уравнения определяли энергию и энтропию активации.
от 1/Т и на основании данного уравнения определяли энергию и энтропию активации.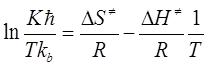 , (3.5)
, (3.5)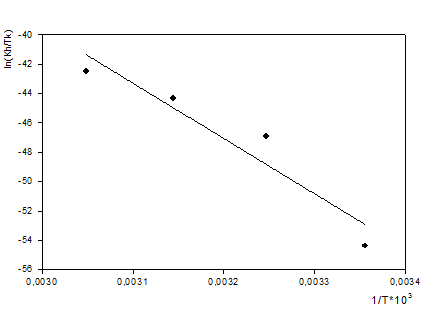
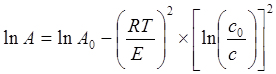 , (3.6)
, (3.6)


