Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Розділ 10. Виробництво мінеральних добривСодержание книги
Поиск на нашем сайте
“Землю ми взяли не вспадок від своїх батьків, а в борг від своїх дітей” Девіз організації “Green Piace” Мінеральними добривами називаються солі та інші неорганічні природні та одержані промисловим способом речовини, що містять в своєму складі елементи необхідні для живлення рослин і збільшення родючості грунтів. До складу рослин входять близько 60 хімічних елементів. Серед них найбільше значення для живлення рослин мають Нітроген, Фосфор і Калій. Азот входить до складу рослинного білка, де його вміст становить 15-19%, він потрібний і у разі синтезу вітамінів, ферментів та інших фізіологічно активних речовин рослин. Без азоту затримується ріст рослин, листя передчасно жовтіє. Фосфор входить до складу ферментів і фосфатидів протоплазми і відіграє важливу роль у процесах поділу клітин та передачі спадкових властивостей. При недостачі фосфору плоди повільніше дозрівають, у них накопичується менше цукру і крохмалю. Сполуки калію регулюють функції ферментів, стимулюють обмін речовин і ріст рослин. Крім того, калій регулює водний режим рослин і сприяє їх стійкості проти засухи і заморозків. Саме цей елемент блокує надходження в рослини радіоактивного цезію і важких металів. Споживання рослинами В, S, Mn, Zn, Mo,Co та інших елементів порівняно невелике, але значення мікроелементів для розвитку рослин незаперечне. Сульфур входить до складу білків, Манган сприяє фотосинтезу і утворенню хлорофілу в рослинах, Бор посилює вуглеводневий та білковий обмін, підвищує стійкість рослин проти захворювань. Молібден і Цинк впливають на обмін речовин, Кобальт суттєво впливає на урожайність кормових культур. Тому щорічний випуск мінеральних добрив у світі становить 600 млн. тонн, а отрутохімікатів 4 млн. тонн. Класифікація мінеральних добрив (МД) МД класифікуються за різними ознаками: За природою живильних елементів: нітратні, фосфатні, калійні, магнієві, борні – три перші основні. За числом живильних компонентів: однокомпонентні (прості) і комплексні (подвійні і потрійні або повні). За концентрацією живильних компонентів: концентровані (більше 33%) та висококонцентровані (більше 60%). За агрегатним станом: тверді, рідкі, порошкоподібні, кристалічні, гранульовані. За швидкістю засвоєння: швидкозасвоювані та пролонговані (цитратно- та лимоннорозчинні). За розчинністю: розчинні та нерозчинні у воді. Вимоги до добрив: 1) висока концентрація основного компоненту; 2) стійкість до злежування; 3) малогігроскопічність; 4) легко вноситься у грунт. Виробництво калійних добрив Сировиною для виробництва калій хлориду слугують: - сильвініт КСl · NaCl – вміст калію 22-25% у перерахунку на К2О; - карналіт KCl · MgCl2 · 6Н2О – вміст калію 17% у перерахунку на К2О; Існують 2 способи одержання калію хлориду: флотаційний та галургічний (політермічний). Флотаційний спосіб базується на флотогравітаційному розділенні водорозчинних мінералів калійної руди в середовищі насиченого ними сольового розчину. Метод включає в себе наступні операції: 1. Подрібнення сильвінітної руди до розмірів 1-3 мм, з подальшим розмолом – до 0,5 мм. 2. Вилучення глинистого шламу (флотація, гравітаційне осадження). 3. Флотаційне розділення на сильвін (KCl) і галіт (NaCl) – основна флотація. 4. Перечисточна флотація для видалення із нього домішок, що залишилися. 5. Зневодненння. 6. Сушка вологого концентрату. Галургічний (політермічний) спосіб базується на різній залежності розчинності компонентів від температури (на різних температурних коефіцієнтах розчинності КСl і NaCl).
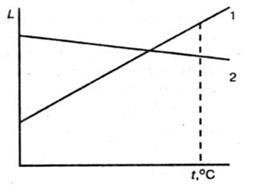
Рис. 10.1. Залежність розчинності КСl і NaCl від температури: 1 – KCl, 2 – NaCl Процес галургічного вилучення калій хлориду із сильвініту включає наступні стадії: 1. Подрібнення сильвінітної руди; 2. Вилужнювання КСl із сильвініту гарячим зворотним маточним розчином. 3. Відокремлення гарячого щьолоку від твердої фази (пісок, глина, NaCl) шляхом фільтрування через воронку для гарячого фільтрування. 4. Охолодження розчину і кристалізація із нього калій хлориду. 5. Фільтрування системи за допомогою вакуум-насоса. 6. Сушка КCl. 7. Нагрівання зворотного розчину і повернення на 2 стадію.
|
||||
|
Последнее изменение этой страницы: 2017-02-22; просмотров: 308; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.01 с.) |