
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Класифікація хіміко-технологічних процесівСтр 1 из 34Следующая ⇒
Екотехнологія Черкаси 2015 ББК 35 3 – 14 УДК 66.0 (0.75)
Рецензенти: Шевченко О. П., кандидат хімічних наук, доцент Черкаського національного університету імені Богдана Хмельницького; Хоменко О. М., кандидат хімічних наук, доцент, завідувач кафедри екології Черкаського державного технологічного університету.
Бойко В. І., Шафорост Ю. А. Екотехнологія: Навчальний полібник / В. І. Бойко, Ю. А. Шафорост. – Черкаси: Видавничий відділ ЧНУ, 2013. – с.
Навчальний посібник «Екотехнологія» підготовлено для студентів університету напряму підготовки «хімія». В ньому наведено інформацію про основні компоненти хімічного виробництва, викладено загальні закономірності хімічної технології як теоретичної основи хімічного виробництва. Описані властивості, застосування та процеси виробництва найважливіших неорганічних та органічних речовин.
Передмова
Викладання «Екотехнології» в університеті повинно забезпечити підготовку висококваліфікованих викладачів хімії в загально-освітніх школах, коледжах, вищих навчальних закладах та інженерно-технічних працівників у науково-дослідних та виробничих установах. Курс «Екотехнології» повинен ознайомити студентів із основними галузями застосування хімії в народному господарстві, із найважливішими виробничими процесами, в ході яких отримуються засоби виробництва та предмети споживання, методами здійснення екологічно безпечних технологічних процесів. Даний курс включає лекційні та лабораторні заняття, а також виробничу практику на хімічних підприємствах. Лекційний курс повинен ознайомити студентів із загальними положеннями і теоретичними основами екотехнології, основними типами виробничих апаратів та принципами побудови технологічних схем найбільш типових виробництв. Студент повинен ознайомитися із сировинними та енергетичними ресурсами, хімізмом основних технологічних стадій виробництва, фізико-хімічною характеристикою реакцій, що лежать в основі процесу, основними параметрами процесів і апаратів, в яких можуть бути здійснені виробничі процеси та окреслити загальну технологічну схему виробництва. При цьому слід враховувати техніко-економічні показники та вимоги до охорони літосфери, водного та повітряного басейнів.
На лабораторних заняттях студенти повинні деталізувати основні положення програмового матеріалу, розширити фактаж, розглянути проблемні місця матеріалу, що виноситься на самостійне опрацювання та виконати залікову контрольну роботу з даної теми. На виробничій практиці студентам надається можливість наочно ознайомитися з хімічними виробництвами, у першу чергу з тими, які вони вивчали в курсі «Екотехнологія». Мета виробничої практики: розширення технологічного світогляду, одержання правильних уявлень про будову апаратів, хід виробничого процесу, принципи контролю здійснення виробничого процесу, ознайомлення із зовнішнім виглядом готових продуктів та принципами організації та економіки виробництва, способами здійснення екологічно безпечних виробництв. РОЗДІЛ 1. ЗАГАЛЬНІ ПИТАННЯ ЕКОТЕХНОЛОГІЇ Термін «екологія» (від грец. оikos – будинок і logos – вчення) первоначально означав розділ біологічної науки про взаємодію організмів рослинного та тваринного світу і середовища їх проживання (Е.Геккель, 1869р). В наш час цей термін означає сукупність наукових і практичних проблем взаємодії людини і природного середовища, використовується як синонім «раціонального використання і охорони природи», тобто цей термін набув більш широкого значення. Характеризуючи особливості технології Д.І.Менделєєв зазначив, що це є «вчення про вигідні (тобто такі, що поглинають найменше людської праці і енергії природи) прийоми переробки природних продуктів в продукти споживання.» «Технологія повинна вивчати найвигідніші способи, вибрати із можливостей найбільш придатну – за вигідності даним умовам часу і місця, щоб надати продукту найбільшу дешевизну при бажаних властивостях і формах». Технологія вивчає методи і процеси переробки сировини в предмети споживання та засоби виробництва. У цих процесах змінюється хімічний склад та властивості вихідних матеріалів. Загально прийнято підрозділяти технологію на механічну та хімічну, розуміючи під механічною ту область технології, яка вивчає процеси, що ведуть до зміни зовнішнього вигляду і форми матеріалу, а під хімічною – галузь технології, що вивчає процеси зміни складу і внутрішньої структури речовини, які здійснюються шляхом хімічних реакцій. Технологія вивчає шляхи здійснення фізичних і хімічних процесів у конкретних техно-екологічних умовах, звертаючи особливу увагу на екологічну доцільність процесів.
Проте зробити правильний вибір – не просте завдання. Ще Ф.Енгельс писав, що «кожна із перемог над природою має в першу чергу ті наслідки, на які ми розраховуємо, але в другу і третю чергу наступають зовсім інші непередбачені наслідки, які дуже часто знищують значення перших». Про цей висновок постійно повинен пам’ятати учений, конструктор, що створює нову машину чи технологічний процес, керівник, що організовує і здійснює виробничий процес. В системі виробництво – природа (технологія – екологія) не можна віддати перевагу ні виробництву над природним середовищем, ні природному середовищу над виробництвом. Задача сьогодення полягає в тому, щоб забезпечити таку взаємодію компонентів системи виробництво – природа, при якому високі темпи економічного росту і підвищення рівня життя узгоджуються із збереженням і поліпшенням якості довкілля. У великих промислових центрах за рік на кожного мешканця припадає близько 1 тонни шкідливих промислових відходів різного агрегатного стану. Динаміка забруднення навколишнього середовища за останні 50 років не має прецедентів в історії цивілізації, що породжує небезпідставну тривогу вчених не лише за життя наступних поколінь, як це було раніше, а й за життя самих творців «науково – технічного прогресу». На думку деяких футурологів, подібно до того як, перенасичення довкілля продуктами життєдіяльності часто є лімітуючим фактором збільшення популяції живих організмів, так перед людством постала «проблема виживання у власних покидьках». Людству необхідно змінити свої споживацько – егоїстичні життєві орієнтири (США – 4,8% населення планети споживає 33% енергоносіїв). Для цього передусім, треба підвищити загальносуспільний рівень освіченості, компетентності і дійовість державних органів влади та всіх учасників виробничого процесу. Інтелектуальний потенціал науки здатний суттєво змінити концепцію і зміст промислових технологій, а отже і стан довкілля. Необхідно виробити техніко – еколого-економічну концепцію синергетичного симбіозу технологічних і природних систем. Розробка і реалізація цієї концепції потребує саме від технологів, екологів і економістів взаєморозуміння і погодження рішень. Динаміка росту народонаселення на планеті Земля Палеонтологічні відомості свідчать, що вік Землі становить 4,5 млрд. років. Якщо цей проміжок часу прийняти за добу (24 год), то в таких часових одиницях життя на Землі існує принаймні 20 год., перші живі істоти вийшли з моря на сушу 6 год. 35 хв. тому, ссавці існують 3 год. 46 хв., а людина – останні 10 секунд. Подовж тривалого існування планети Земля мали місце і природні катаклізми, стихійні явища тощо. Проте лише згубна дія людського суспільства, особливо, подовж останніх півтори сотні років, призвела до глибокої екологічної катастрофи. Однією із першопричин цього явища є демографічний вибух, експоненційне зростання кількості населення на планеті Земля.
Це призвело до збільшення темпів і обсягів знищення природних ресурсів, нагромадження великої кількості відходів виробництва і побуту, забруднення оточуючого середовища, глобальних кліматичних змін, хвороб, голоду, вимирання. Атмосфера Атмосфера – це зовнішня оболонка Землі, що сягає від її поверхні в космічний простір приблизно на 300 км. Історія виникнення і розвитку атмосфери досить складна і тривала, вона налічує близько 3 млрд. років. Подовж 50 млн. років, як вважають вчені, склад і властивості атмосфери стабілізувалися. Атмосфера – захисна оболонка Землі, якби її не існувало, то температурні коливання становили б ± 200ºС. Парниковий ефект Вуглекислий газ Озонові дірки Діапазони спектра оптичного випромінювання
Згубним для живих організмів є короткохвильове УФ випромінювання діапазону С, В. Від дії цих променів захищає Землю озоновий шар, що знаходиться на висоті 20 – 50км. Озон синтезується із кисню Кислотні дощі Оксиди сульфуру, карбону, нітрогену, що потрапляють у атмосферу внаслідок роботи ТЕС, автодвигунів, виробничих викидів, сполучаються із атмосферною вологою, утворюють дрібні крапельки сульфатної, карбонатної, нітратної кислот, які переносяться вітром у вигляді кислотного туману і випадають на землю кислотними дощами. Це призводить до зниження урожайності сільськогосподарських культур, вимивання із ґрунту
Тютюновий дим Людина, яка палить, видихає повітря, забруднення якого в 384 тис. разів перевищує ГДК. Вдихати тютюновий дим в 4 рази шкідливе, ніж вихлопні гази автомобіля безпосередньо із вихлопної труби. Тютюновий дим містить: нікотин, слабкодіючу наркотичну речовину, а також порядку 200 токсичних речовин (CO, бензпірен). За даними ВОЗ від хвороб спричинених палінням щороку вмирає 1,5 млн чоловік. Ризик вмерти курцю в 5,4 рази більший, ніж середній. Паління вагітними жінками призводить 100% до зміни плоду на генетичному рівні. Пасивне паління неменш шкідливе для здоров’я людини. Гідросфера Гідросфера – це водяна сфера нашої планети, сукупність океанів, морів, вод континентів, льодових покриттів. Загальний об’єм природних вод становить близько 1,5 млрд км³ (1/800 об’єму планети). Води вкривають 71% поверхні планети. Маючи рекордновисоку питому теплоємність, вода є важливим фактором у кліматотворчому процесі на Землі. Основні, найбільш небезпечні форми забруднення світового океану: а) ДДТ, мізерна концентрація яких (1 частина на 10 млн) веде до стрімкого зниження здатності фітопланктону до фотосинтезу, а отже і до вироблення кисню; б) синтетичні речовини, що містять поліхлоровані біфеніли (ПХБ) та відходи хімвиробництва, що нерозчинні у воді. Вони легко проникають в біологічні системи і накопичуються з трофічною метою; в) нафтові забруднення, що не мають ефективних методів видалення і є причиною серйозних екологічних наслідків; г) нагріті води, які є причиною суттєвого зміщення природної рівноваги. На прісну воду припадає лише 2% об’єму гідросфери. Використання більшої частини прісної води ускладнене. Одним із лімітуючих факторів є важкодоступність прісної води, а також повільне її відтворення. В цьому відношенні найбільш зручними є води річок. Другим джерелом прісної води є атмосферна волога, але її надходження є періодичними. На думку експертів підземні води у 21 столітті будуть забезпечувати Нарешті є ще один важливий шлях подолання глобального протиріччя водокористування – диференційне за якостю споживання води в масштабах планети. Літосфера Літосфера – зовнішня тверда оболонка Землі, яка включає всю земну кору з частиною верхньої мантії Землі й складається з осадових, вивержених і метаморфічних порід.
Актуальність екологічного вивчення літосфери зумовлена тим, що у верхній частині земної кори знаходяться ґрунти, значення яких для людини важко переоцінити. Ґрунти – органо-мінеральний продукт багатовікової спільної діяльності живих організмів, води, повітря, сонячного тепла і світла, і є одним із найважливіших природних ресурсів. Найбільш сильний вплив на природний комплекс здійснюють відкриті або кар’єрні, розробки корисних копалин. За впливом на біоценоз ґрунти можуть бути прирівняні до геологічних катастроф. Масштаби перебудови поверхні гірничопромислових басейнів настільки великі, що в науці сформулювалося поняття про техногенний неорельєф. Форми неорельєфу бувають двох типів: вироблені (кар’єри, шахти, виємки) і акумулятивні (відвали, насипні і намивні плантації). Інші проблеми постають при закритих (шахтних) розробках корисних копалин. Багаторічні гірничі роботи часто призводить до опускання (на 6 - 7 м) земної поверхні на великих площах. До аналогічного динамічного ефекту призводить багаторічна інтенсивна експлуатація нафти, газу та підземних вод. Осідання земної поверхні найбільш інтенсивно проходить у районах, що утворені молодими неущільненими рихлими породами. Існує тісний зв'язок між ростом сільськогосподарського виробництва і прогресуючим забрудненням природного середовища. Ціла низка небажаних наслідків і змін грунту пов’язані з широким використанням мінеральних добрив, пестицидів, гербіцидів. Кількість речовин, що залучаються в колообіг у процесі, сільськогосподарської діяльності, виміряється величинами того ж порядку, що й у процесі промислового освоєння. Щорічно на поля надходить понад 35 млн. тонн добрив, 4 млн. тонн пестицидів, а на початок 21 століття виробництво добрив зросте до 100 – 120 млн. тонн. Слід зазначити, що ставлення до внесення добрив, пестицидів, гербіцидів не повинно бути нігілістичним. Використання цих препаратів, насамперед добрив, повинно бути диференційованим і враховувати такі аспекти як потребу тої чи іншої рослини в певному елементі, наявність даного елементу в ґрунті. Такий науковий підхід до внесення добрив дає приріст урожаю сільгоспкультур на 50% Напрями потоків Прямоточні, або паралельноточні, процеси характеризуються рухом реагентів або теплових потоків і матеріалів в одному і тому ж напрямку.
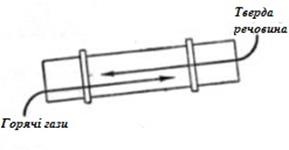
Рис.2.1. Прямоточний рух потоків Протитечійні процеси характеризуються зустрічними або протилежними один одному напрямками руху реагентів або теплових потоків.
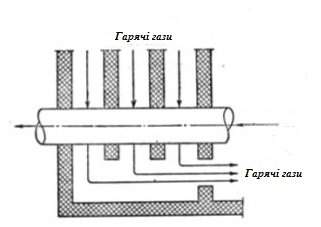
Рис.2.2. Протитечійний рух потоків Якщо потоки реагентів або тепла і матеріалів рухаються під кутом один до одного, то такі схеми називаються перехресними.
Рис.2.3. Перехресний рух потоків Поняття про прямоточні, протитечійні та перехресні процеси має сенс лише стосовно гетерогенних процесів. Протитечійний рух матеріальних і енергетичних потоків має переваги перед прямотоком, проте є й значна кількість процесів де доцільно використовувати паралельний потік. Основні переваги протитечії перед прямотоком: 1. Більша повнота здійснення процесу; 2. Більша середня рушійна сила процесу (що виражається різницею концентрацій реагентів і температур), що дозволяє зменшити розміри апаратури. Прямоток, у свою чергу, має наступні переваги: 1. Можливість створити більшу різницю температур і концентрацій реагентів на вході в апарат і досягнути локально більшої швидкості процесу (при меншій середній швидкості по всьому апарату); 2. Більш м’які умови протікання процесу на виході матеріалу із апарату (відсутність небезпеки перегріву, пересушування, переохолодження). Регенерація Багато технологічних схем передбачають регенерацію речовин, тобто переведення прореагованих речовин у первинний стан і їх повторне використання. Регенерувати можна не лише речовини, але й енергію. Наприклад, тепло пічних газів можна частково використовувати для нагріву камер з цегляною насадкою, так званих регенераторів, з наступним використанням фізичного тепла насадки регенераторів для нагрівання повітря, що входить у піч. Регенерації підлягає вода, каталізатор, тепло тощо. Матеріальний баланс На основі матеріального розрахунку, що здійснюється в основному за стехіометричними рівняннями реакцій, складається матеріальний баланс процесу, що здійснюється. Всякий матеріальний баланс базується на законі збереження маси: маси речовин, що введені у виробничий процес рівні масі продуктів реакції, напівпродуктів і відходів. Матеріальний баланс виражається у вигляді рівняння і таблиці, що складається із двох частин приходної – для речовин, що вводяться і витратної – для одержаних речовин і втрат. Для наочності баланси зображують часто у вигляді діаграм.
Рис.2.5. Діаграма матеріального балансу виробництва фосфору (на 1 тонну продукту) Тепловий баланс За аналогією складається енергетичний баланс (головним чином тепловий і електроенергетичний), що базується на законі збереження енергії. У приходні статті теплового балансу, як правило, входять: 1) теплота, що сповіщається екзотермічними хімічними реакціями; 2) фізична теплота, що приноситься нагрітими речовинами, що реагують; 3) теплота, сповіщена у процес зовні. У витратні статті входять: 1) теплота, що поглинається ендотермічними реакціями; 2) фізична теплота, що виводиться продуктами реакції; 3) втрати тепла в оточуюче середовище.
Рис.2.6. Діаграма теплового балансу виробництва фосфору (на 1 тонну продукту) Термохімічні розрахунки Хімічна взаємодія, як правило, супроводжується тепловим ефектом. При цьому теплота може і поглинатися, і виділятися. Процеси, що протікають з виділенням теплоти називаються екзотермічними, для яких характерне поглинання теплоти – ендотермічними. Рівняння процесу, що враховує тепловий ефект, називається термохімічним. Наприклад: N2(газ) + 3H2(газ) ⇄ 2NH3(газ) + 92,30 КДж Тепловий ефект реакції необхідно характеризувати не лише абсолютною величиною, але й знаком. Історично склалось дві системи відліку: термохімічна й термодинамічна. У першій із них тепловий ефект екзотермічної реакції рахується позитивним (екзо-зовнішній). Ендотермічні реакції супроводжуються негативним тепловим ефектом, теплота поглинається системою (ендо-внутрішній). У термодинаміці прийнята зворотна система знаків, тобто теплота, що поглинається системою рахується позитивною, а теплота, яку система виділила в оточуючий простір – негативною. В термодинамічній системі знаків тепловий ефект реакції ототожнюється із зміною ентальпії системи N2(газ) + 3H2(газ) ⇄ 2NH3(газ) Глибоке узагальнення термохімічних закономірностей дає закон термохімії, сформульований в 1836 р. російським академіком Германом Івановичем Гессом: тепловий ефект хімічної реакції, що протікає або при сталому об’ємі або при сталому тиску, не залежить від числа проміжних стадій, а визначається лише початковим і кінцевим станом системи. Закон Гесса можна проілюструвати схемою
 A + B = AB A + B = AB
  ∆H ∆H
Із закону Гесса витікає кілька наслідків: 1. Тепловий ефект реакції утворення одного моля сполуки із простих речовин в стандартному стані при заданих Т, Р не залежать від способу утворення сполуки. Такий тепловий ефект називається теплотою утворення. У термодинаміці в якості стандартних умов приймається температура 250С=298К і тиск 1,0132•ּ105 Па. 2. Другий наслідок закону Гесса дозволяє розрахувати тепловий ефект реакції за теплотами утворення вихідних речовин і продуктів взаємодії. Він формулюється: стандартний тепловий ефект реакції рівний алгебраїчній різниці суми стандартних теплот утворення продуктів реакції і суми стандартних теплот утворення вихідних речовин (із врахуванням стехіометричних коефіцієнтів): аА + вВ = сС + dD
РОЗДІЛ 4. ТЕПЛОВІ ПРОЦЕСИ Основи теплопередачі Перенос енергії у формі тепла, що відбувається між тілами з різною температурою, називається теплообміном. Рушійною силою будь-якого процесу теплообміну є різниця температур більш нагрітого і менш нагрітого тіл, за наявності якої тепло самочинно, у відповідності до другого закону термодинаміки, переходить від більш нагрітого до менш нагрітого тіла. Теплообмін між тілами є обміном енергією між молекулами, атомами і вільними електронами; в результаті теплообміну інтенсивність руху частинок більш нагрітого тіла знижується, а менш нагрітого – зростає. Розрізняють три принципово відмінних елементарних способи розповсюдження тепла: теплопровідність, конвекцію та теплове випромінення. Теплопровідність – це перенос теплоти внаслідок безладного (теплового) руху мікрочастинок, що дотикаються одна до одної. Цей рух може бути або рухом самих молекул (гази, краплинні рідини), або коливаннями атомів (у кристалічній гратці твердих тіл), або дифузією вільних електронів (у металах). У твердих тілах теплопровідність є зазвичай основним видом розповсюдження теплоти. Конвекцією називається перенос теплоти внаслідок руху і переміщення макроскопічних об’ємів газів або рідин. Перенос теплоти можливий за умов природної, або вільної, конвекції, що обумовлена різницею густини у різних точках об’єму рідини (газу), що виникає унаслідок різниці температур у цих точках або за умов вимушеної конвекції при примусовому русі усього об’єму рідини, наприклад у разі переміщування її мішалкою. Теплове випромінення – це процес розповсюдження електромагнітних коливань з різною довжиною хвилі, обумовлений тепловим рухом атомів і молекул тіла, що випромінює теплоту. Всі тіла здатні випромінювати енергію, яка поглинається іншими тілами і знову перетворюватися у теплоту. Таким чином, відбувається променевий теплообмін, він складається із процесів випромінення і поглинання променів. За реальних умов теплота передається не яким-небудь одним із зазначених вище способів, а комбінованим шляхом. Перенос теплоти від стінки до газуватого (рідкого) середовища або у зворотному напрямку називається тепловіддачею. Ще більш складним є процес передачі теплоти від більш нагрітої до менш нагрітої рідини (газу)через поверхню або стінку, що їх розділяє. Цей процес називається теплопередачею. Передача теплоти конвекцією (конвективний теплообмін) Перенос теплоти конвекцією тим інтенсивніший, чим більш турнбулентно рухається вся маса рідини і чим енергійніше здійснюється перемішування її частинок. Таким чином, конвекція пов’язана із механічним переносом теплоти і сильно залежить від гідродинамічних умов руху рідини. Для інтенсифікації конвективного теплообміну бажано, щоб тепловий пограничний шар був якомога тоншим. З розвитком турнбулентності потоку пограничний шар стає настільки тоншим, що конвекція виявляє домінуючий вплив на теплообмін. Для зручності розрахунку тепловіддачі в основу кладуть рівняння відносно простого виду, відоме під назвою закону тепловіддачі або закону охолодження Ньютона: dQ = α dF (tст – tр) dτ (1.3) Згідно цьому рівнянню, кількість теплоти dQ, що віддається за час dτ поверхнею стінки dF, що має температуру tст, рідині з температурою tр, прямо пропорційна dF і різниці температур tст-tр. Коефіцієнт пропорційності α у рівнянні (1.3) називається коефіцієнтом тепловіддачі. Величина α характеризує інтенсивністьпереносу тепламіж поверхнею тіла, наприклад твердої стінки, і оточуючим середовищем (краплинною рідиною або газом). Коефіцієнт тепловіддачі виражається наступним чином: [α] = Таким чином, коефіцієнт тепловіддачі α вказує, на кількість теплоти, яка передається від 1 Внаслідок складної структури потоку, особливо за умов турнбулентного руху, величина α є складною функцією багатьох змінних. Коефіцієнт тепловіддачі залежить від наступних факторів: · швидкості рідини w, її густини ρ та в’язкості µ, тобто змінних, що визначають режим руху рідини; · теплових властивостей рідини (питомої теплоємності Ср; теплопровідності λ), а також коефіцієнта об’ємного розширення β; · геометричних параметрів – форми і визначаючих розмірів стінки (для труб – їх діаметр d і довжина L),а також шероховатості ε стінки). Внаслідок складної залежності коефіцієнта тепловіддачі від великого числа факторів неможливо отримати розрахункове рівняння для α, придатне для всіх випадків тепловіддачі. Лише шляхом узагальнення дослідних даних за допомогою теорії подібності можна одержати узагальнене (критеріальне) рівняння для типових випадків тепловіддачі, що дозволяє розраховувати α для умов конкретної задачі. Теплове випромінювання Довжини хвиль теплового випромінення лежать в основному у невидимій (інфрачервоній) частині спектра і мають довжину 800-40000 нм. Вони відрізняються від видимих світлових променів лише довжиною (довжина світлових хвиль 400-800нм). Тверді тіла володіють суцільним спектром випромінення: вони здатні випромінювати хвилі всіх довжин за будь-якої температури. Проте інтенсивність теплового випромінення зростає із підвищенням температури тіла, і при високих температурах (приблизно при t ≥ 600°С) проміневий теплообмін між твердими тілами і газами набуває домінуючого значення. Теплове і світлове випромінення має однакову природуі тому характеризується спільними законами: промінева енергія розповсюджується в однорідному і ізотропному середовищі прямолінійно. Потік променів, що виділяється нагрітим тілом, потрапляючи на поверхню іншого, променевипромінюючого тіла, частково поглинається, частково відбивається (при цьому кут падіння рівний куту відбиття) і частково проходить крізь тіло без змін. Якщо тіло повністю поглинає всі промені, що на нього падають, то таке тіло називається абсолютно чорним. Тіло, яке відбиває всі промені, що на нього падають, називається абсолютно білим. Тіло, яке пропускає всі промені, що на нього падають, називається абсолютно прозорим або діатермічним. Абсолютно чорних, абсолютно білих і абсолютно прозорих тіл реально не існує. Всі тіла в природі, які поглинають, відбивають і пропускають ту чи іншу частину променів, що на них падають називаються сірими тілами. Кількість енергії, що випромінюється тілом в одиницю часу в усьому інтервалі довжин хвиль (від λ=0 до λ=∞) одиницею поверхні F тіла, характеризує випромінюючу здатність E тіла: E = де Після перетворення, розкладання знаменника в ряд і наступного інтегрування рівняння (1.4) приходимо до ряду, що сходиться, обрахунок суми членів якого дозволяє виразити повну енергію випромінювання або випромінювальну здатність абсолютно чорного тіла: Е0 = К0·Т4, (1.5) де Т – абсолютна температура поверхні тіла, °К; К0=5,67·10-8 вт/(м2·°К4) – константа випромінення абсолютно чорного тіла. Рівняння (1.5) має назву закону Стефана-Больцмана. Згідно закону, випромінювальна здатність абсолютно чорного тіла пропорційна четвертому степеню абсолютної температури його поверхні. Для сірих тіл необхідно знати залежність між їх випромінювальною і поглинальною здатністю. Ця залежність виражається законом Кірхгофа, згідно якому відношення випромінювальної здатності будь-якого тіла до його поглинальної здатності при цій же температурі є величиною сталою, рівною випромінювальній здатності абсолютно чорного тіла. Теплові промені, потрапляючи на шероховаті поверхні, багаторазово відбиваються від неї, що приводить до кращого поглинання променевої енергії у порівнянні із поглинанням гладкою поверхнею. Тоді у відповідності із законом Кірхгофа, шероховаті поверхні повинні володіти також більшою випромінювальною здатністю, ніж гладкі. Навпаки, випромінювальна здатність полірованих поверхонь, що добре відбиває промені, які на неї падають, у відповідності до закону Кірхгофа, повинна бути низькою.
Нагрівання Нагрівання водяною парою Одним із найбільш часто використовуваних агентів для нагрівання є насичена водяна пара. Найбільш поширений спосіб нагрівання – нагрівання глухою парою, тобто в такий спосіб, коли тепло передається через стінку теплообмінного апарата. В тих випадках, коли допустимо змішування середовища, яке нагрівається з паровим конденсатом, використовують нагрівання гострою парою, яку вводять безпосередньо в рідину, яка нагрівається. Нагрівання гарячою водою Коефіцієнт тепловіддачі гарячої води нижче, ніж гарячої пари, тому нагрівання гарячою водою використовується рідше, лише в разі потреби нагріти речовину до температур не більше 100˚. Нагрівання топочними газами Топочні гази дозволяють здійснювати нагрів до 1000-1100° С, причому при незначному надлишковому тиску в теплообміннику. Недоліком такого способу нагріву є нерівномірність нагріву, складність регулювання температурного режиму. Охолодження Штучне охолодження Ряд процесів хімічної технології проводять за температур, значно нижчих, ніж ті, що можна одержати, використовуючи в якості охолоджуючих агентів повітря, воду і лід. До числа процесів, що здійснюються при штучному охолодженні, відносяться деякі процеси абсорбції, кристалізації, розділення газів, сублімаційної сушки. Великого значення набувають холодильні процеси в металургії, електротехніці, електроніці, ядерній, ракетній, вакуумній та інших галузях техніки. Штучне охолодження завжди зв’язане з переносом тепла від тіла з більш низькою температурою до тіла з більш високою температурою. Такий перенос, у відповідності до другого закону термодинаміки, потребує затрати енергії. Тому сповіщення енергії системі є необхідною умовою одержання холоду. Умовно розрізняють: 1) помірне охолодження (діапазон температур від кімнатних до -100°С); 2) глибоке охолодження (до температур нижче -100°С); У свою чергу, одержання температур нижче (-100°С) умовно класифікується наступним чином: а) техніка глибокого охолодження (від -100 ° С до -218 ° С) б) кріогенна техніка (від 40 ° до 0,3 ° К) в) техніка ультранизьких температур (до 0,00002 ° К) Способи одержання температур вище 2 ° К знайшли технічне застосування. Одержання більш низьких температур відноситься до сфери лабораторної техніки. Використання температур, що відповідають глибокому охолодженню, дозволяє розділяти газові суміші шляхом їх часткового або повного зрідження і одержувати багато технічно важливих газів, наприклад динітроген, диоксиген, дигідроген, етен тощо. Методи штучного охолодження В процесах штучного охолодження зниження температури холодильного агента, що відіграє роль переносчика теплоти, здійснюється за допомогою адіабатичного розширення різноманітних попередньо стиснених газів. Розширення газів можна здійснити: а) при пропуска
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-22; просмотров: 218; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.106.100 (0.145 с.) |
 діє так як скло в парнику: пропускає сонячні промені, а теплове випромінювання затримує. Небезпека парникового ефекту полягає в тому, що при підвищенні температури на 2,5º С, внутрішні райони континенту стануть сухішими, узбережжя – вологими, зима – короткою і теплою, літо – довге і жарке. Кліматичні зони змістяться на 400 км на північ, почнеться танення вічної мерзлоти та арктичного льоду, що призведе до підйому рівня світового океану на 2 – 3 метри.
діє так як скло в парнику: пропускає сонячні промені, а теплове випромінювання затримує. Небезпека парникового ефекту полягає в тому, що при підвищенні температури на 2,5º С, внутрішні райони континенту стануть сухішими, узбережжя – вологими, зима – короткою і теплою, літо – довге і жарке. Кліматичні зони змістяться на 400 км на північ, почнеться танення вічної мерзлоти та арктичного льоду, що призведе до підйому рівня світового океану на 2 – 3 метри. під дією УФ-С і УФ-В випромінювання. Озонова дірка виникла над Антарктидою, підвищений УФ-фон спостерігається над Новою Зеландією, Шніцбергеном. Причина виникнення озонових дір полягає у взаємодії озону з фреонами, компонентами хладоагентів і аерозольних упаковок. Фреони – це галогенвмісні органічні сполуки.
під дією УФ-С і УФ-В випромінювання. Озонова дірка виникла над Антарктидою, підвищений УФ-фон спостерігається над Новою Зеландією, Шніцбергеном. Причина виникнення озонових дір полягає у взаємодії озону з фреонами, компонентами хладоагентів і аерозольних упаковок. Фреони – це галогенвмісні органічні сполуки. , що веде до деградації флори і фауни, гинуть ліси, утворюються зсуви ґрунту, гинуть комахи, отруюється вода в річках, озерах, а отже гине риба. Кислотні дощі є причиною руйнування пам’ятників архітектури, а також згубно діють на органи дихання людей, подразнюють очі.
, що веде до деградації флори і фауни, гинуть ліси, утворюються зсуви ґрунту, гинуть комахи, отруюється вода в річках, озерах, а отже гине риба. Кислотні дощі є причиною руйнування пам’ятників архітектури, а також згубно діють на органи дихання людей, подразнюють очі. всіх потреб у прісній воді. Крім того, важливу роль належить відіграти збільшенню доступності льодовикових вод або шляхом транспортування льоду (наприклад айсберг) або дією на сток талих льодовикових вод. Важлива роль відводиться процесам демінералізації солоних і солонуватих вод.
всіх потреб у прісній воді. Крім того, важливу роль належить відіграти збільшенню доступності льодовикових вод або шляхом транспортування льоду (наприклад айсберг) або дією на сток талих льодовикових вод. Важлива роль відводиться процесам демінералізації солоних і солонуватих вод.


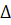 Н. При запису термодинамічного рівняння в цій системі тепловий ефект не включається в рівняння процесу, а записується в одній строчці з рівнянням, але з інтервалом. Так, наведене вище рівняння, матиме вигляд:
Н. При запису термодинамічного рівняння в цій системі тепловий ефект не включається в рівняння процесу, а записується в одній строчці з рівнянням, але з інтервалом. Так, наведене вище рівняння, матиме вигляд:
 = [c
= [c  (D)] – [a
(D)] – [a  =
=  =
= 
 поверхні стінки до рідини (або від рідини до 1
поверхні стінки до рідини (або від рідини до 1  , (1.4)
, (1.4) – енергія, випромінювана тілом.
– енергія, випромінювана тілом.


