
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Оптические свойства коллоидных растворовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Для золей характерна оптическая неоднородность, обусловленная тем, что коллоидные частицы обладают свойством рассеивать падающие на них лучи света, так как длина световой волны (λ) больше размера частицы дисперсной фазы. Если рассматривать коллоидные растворы в проходящем свете, то они кажутся совершенно прозрачными и ничем не отличающимися от истинных растворов. Однако при рассмотрении этих же растворов в отражённом свете можно наблюдать опалесценцию – явление бокового свечения. Опалесценция становится более заметной, если вместо параллельного пучка света через коллоидный раствор пропускать пучок сходящихся лучей, поместив между этим раствором и источником света выпуклую линзу. При рассмотрении такого раствора сбоку в нём виден яркий светящийся конус (рис. 35).
а б
Рис. 35. Конус Тиндаля (а) и схема его получения (б) − признак коллоидного состояния вещества
Впервые это явление наблюдал М.В. Ломоносов, однако подробно оно было изучено Д. Тиндалем, и поэтому светящийся конус называют конусом Тиндаля. На рис. 36 показана модель эффекта Тиндаля в кинотеатре.
Рис. 36. Модель эффекта Тиндаля в кино (отражение света пылинками)
Причина эффекта Тиндаля заключается в следующем. Коллоидный раствор содержит мелкие взвешенные частицы дисперсной фазы, показатель преломления которой отличается от показателя преломления дисперсионной среды. При попадании на эти частицы пучка света они становятся центрами рассеяния света, а образуемые ими вторичные волны усиливают друг друга и порождают рассеяние света. Светорассеяние является уникальным свойством коллоидных систем, которое позволяет отличить их от истинных растворов.
Оптические свойства дисперсных систем используются при определении структуры, размеров и формы коллоидных частиц, что основано на соизмеримости электромагнитной световой волны с их размерами. Поскольку коллоидные частицы золей значительно меньше длин лучей видимого света, то они довольно интенсивно рассеивают (но не отражают) свет вследствие его дифракции [26] в микрогетерогенной системе. Явление рассеяния света коллоидными частицами позволило создать ультрамикроскоп, с помощью которого частицы, рассматриваются как светящиеся точки. Эти точки свидетельствуют о броуновском движении (рис. 30),вызываемом хаотичными ударами со стороны молекул среды, находящихся в тепловом движении. Это движение препятствует коагуляции и оседанию коллоидных частиц и является одной из причин устойчивости золей. Изучение броуновского движения показало, что кинетическиесвойства коллоидных растворов близки к таковым истинных растворов. Однако интенсивность движения частиц дисперсной фазы в коллоидных растворах намного меньше, чем молекул в истинных растворах (что связано с большой разностью в их размерах).
ТЕСТОВЫЕ УПРАЖНЕНИЯ 1. С увеличением энергии взаимодействия частиц вблизи границы раздела фаз удельная поверхностная энергия …. 1) уменьшается 2) изменяется неоднозначно 3) не изменяется 4) увеличивается
2. Повышение концентрации вещества вблизи границы раздела фаз называется …. 1) диффузией 2) десорбцией 3) адсорбцией 4) абсорбцией
3. Вещество, адсорбированное на поверхности раздела фаз, называется … 1) адсорбентом 2) адсорбером 3) адсорбтивом 4) адсорбатом
4. Вещество, обладающее адсорбционной способностью, называется …. 1) адсорбером 2) адсорбтивом 3) адсорбентом 4) адсорбатом
5. Физическая адсорбция от хемосорбции отличается …. 1) высоким тепловым эффектом и необратимостью 2) высоким тепловым эффектом и обратимостью 3) невысоким тепловым эффектом и необратимостью 4) невысоким тепловым эффектом и обратимостью
6. Химическая адсорбция от физической отличается …. 1) обратимостью 2) наличием межмолекулярного взаимодействия
3) увеличением свободной энергии Гиббса 4) необратимостью
7. Зависимость адсорбции от равновесной концентрации (в случае газов от равновесного парциального давления) при постоянной температуре называется … адсорбции. 1) изобарой 2) адиабатой 3) изотермой 4) изохорой
8. Изотерма адсорбции обычно описывается уравнением …. 1) Ван-дер-Ваальса 2) Ленгмюра 3) Смолуховского 4) Больцмана
9. Поверхностно-инактивными веществами являются …. 1) высшие жирные кислоты 2) высшие спирты 3) неорганические соли 4) жиры
10. Высокую поверхностную активность проявляют …. 1) неорганические кислоты 2) соли высших карбоновых кислот 3) соли низших карбоновых кислот 4) неорганические соли
11. Поверхностно-активным веществом является …. 1) HCOONa 2) Na2SO4 3) H2SO4 4) C17H35COONa
12. В состав ПАВ может входить группа …. 1) –СООН 2) –СН3 3) –С17Н35 4) –С2Н5
13. С увеличением длины углеводородного радикала поверхностная активность карбоновых кислот …. 1) уменьшается 2) изменяется неоднозначно 3) не изменяется 4) увеличивается
14. Концентрация ПАВ вблизи поверхностного слоя по сравнению с концентрацией в остальном объёме жидкости …. 1) практически одинакова 2) значительно ниже 3) изменяется неоднозначно 4) значительно выше
15. В присутствии ПАВ поверхностное натяжение воды …. 1) уменьшается 3) увеличивается 2) не изменяется 4) изменяется неоднозначно
16. Эффект изменения поверхностного натяжения под действием ПАВ, влияющий на смачиваемость твёрдых тел, используется при …. 1) флотации руд 2) восстановлении металла 3) электрофорезе 4) растворении электролитов
17. Различие в адсорбционной способности веществ используется 1) дериватографии 2) полярографии 3) хроматографии 4) томографии
18. Твёрдое тело, на поверхности которого происходит разделение и концентрирование веществ, в хроматографическом анализе называется …. 1) сорбтивом 2) абсорбентом 3) сорбатом 4) адсорбентом
19. Гетерогенная система, состоящая из двух и более фаз с сильно развитой поверхностью раздела, называется …. 1) диффузионной 2) дисперсной 3) поверхностной 4) неоднородной
20. Характерным признаком дисперсных систем является …. 1) постоянство состава 2) устойчивость 3) гетерогенность 4) гомогенность
21. Основной характеристикой дисперсных систем является … частиц дисперсной фазы. 1) размер 2) масса 3) количество 4) форма
22. К дисперсным системам, в которых дисперсионной средой является газ, а дисперсной фазой – твёрдое вещество, относится …. 1) мыльная пена 2) молоко 3) дым 4) краска 23. Примером дисперсной системы, в которой дисперсионной средой является жидкость, а дисперсной фазой – газ, является …. 1) мыльная пена 2) коровье молоко 3) печной дым 4) оливковый майонез
24. Система, в которой твёрдые частицы распределены в жидкости, называется …. 1) гелем 2) эмульсией 3) пеной 4) суспензией
25. К дисперсным системам, в которых дисперсионной средой является газ, а дисперсной фазой – жидкость, относится …. 1) туман 2) дым 3) пенопласт 4) крем
26. Туман относится к дисперсным системам типа …. 1) пены 2) эмульсии 3) золи 4) аэрозоли
27. Майонез – представитель дисперсных систем типа …. 1) аэрозоли 2) гели 3) суспензии 4) эмульсии
28. Краски относятся к дисперсным системам типа ….
1) пены 2) эмульсии 3) золи 4) аэрозоли
29. Дым является дисперсной системой типа …. 1) гели 2) аэрозоли 3) эмульсии 4) пены
30. Маргарин относится к дисперсным системам типа …. 1) суспензии 2) аэрозоли 3) эмульсии 4) золи
31. Молоко является представителем дисперсных систем типа …. 1) эмульсии 2) пены 3) аэрозоли 4) золи
32. К дисперсным системам относится …. 1) яблочный сок 2) молоко 3) вода 4) рассол
33. В природе диспергирование веществ происходит при …. 1) светорассеянии 2) выпадении атмосферных осадков 3) землетрясении 4) вулканических извержениях
34. Образование коллоидных частиц возможно в реакции …. 1) Сl2 + KOH → 2) Pb (NO3)2 + NaI → 3) KOH + H2SO4 → 4) MnO2 + HCl →
35. Коагуляция золя может происходить при добавлении …. 1) сильного электролита 2) неэлектролита 3) растворителя 4) воды
36. Для золя гидроксида меди, полученного по реакции …. CuSO4 (изб.) + 2NaOH → Cu(OH)2↓ + Na2SO4, наиболее эффективное коагулирующее действие оказывает ион …. 1) Cl– 2)
37. Для золя сульфата бария, полученного по реакции Ва(NО3)2 + Nа2SО4 (изб.) = ВаSО4↓ + 2NаNО3, наибольший коагулирующий эффект оказывает ион …. 1) Fe2+ 2) Mg2+ 3) Fe3+ 4) K+
38. Для коллоидного раствора иодида серебра, полученного по реакции АgNО3 + КI(изб.) = АgI↓ + КNО3, наилучшее коагулирующее действие проявляет ион …. 1) Na+ 2) Ca2+ 3) Mg2+ 4) Al3+ 39. Коагуляцию золя сульфата бария, полученного по реакции ВаСl2 + К2SО4 (изб.) = ВаSО4↓ + 2КСl, будут вызывать …. 1) сульфат-ионы 2) анионы 3) хлорид-ионы 4) катионы
40. Коагуляцию золя сульфата стронция, полученного по реакции Sr(NO3)2 (изб.) + Na2SO4 = SrSO4↓ + 2NaNO3, будут вызывать …. 1) анионы 2) ионы натрия 3) катионы 4) ионы стронция
41. Ионы, адсорбирующиеся на поверхности агрегата мицеллы и определяющие заряд её гранулы, называются …. 1) коагулирующими 2) потенциалопределяющими 3) поверхностными 4) адсорбционными
42. В золе гидроксида железа(III), полученного гидролизом хлорида железа(III), потенциалопределяющими являются ионы …. 1) H+ 2) OH– 3) Fe3+ 4) Cl–
43. В коллоидных частицах, образующихся при действии избытка соляной кислоты на раствор нитрата серебра, потенциалопределяющими являются ионы …. 1)
44. В мицеллярных агрегатах, полученных действием избытка раствора нитрата серебра на раствор бромида калия, потенциалопределяющими являются ионы …. 1)
45. В коллоидных частицах, образующихся при добавлении избытка раствора хлорида натрия к раствору нитрата серебра, потенциалопределяющими являются ионы ….
1) Cl– 2) Ag+ 3) Na+ 4)
46. Коллоидные частицы, полученные взаимодействием избытка раствора хлорида бария с разбавленной серной кислотой, …. 1) заряжены положительно 2) заряжены отрицательно 3) не имеют заряда 4) электронейтральны
47. Коллоидные частицы, образующиеся в результате взаимодействия миллимолярных растворов хлорида натрия и нитрата серебра в соотношении 1: 2, …. 1) не имеют заряда 2) электронейтральны 3) имеют отрицательный заряд 4) имеют положительный заряд
48. Коллоидные частицы, полученные взаимодействием раствора хлорида бария с избытком разбавленной серной кислоты, …. 1) заряжены положительно 2) электронейтральны 3) заряжены отрицательно 4) не имеют заряда
49. Коллоидные частицы гидроксида железа(III), полученного гидролизом солей железа(III), …. 1) заряжены положительно 2 не имеют заряда 3) электрически нейтральны 4) заряжены отрицательно
50. Коллоидные частицы, образующиеся при взаимодействии равных объёмов водных растворов ацетата серебра (с = 10-3 моль/л) и бромида калия (с = 5·10-4 моль/л), в электрическом поле …. 1) совершают колебательные движения 2) перемещаются к положительно заряженному электроду 3) перемещаются к отрицательно заряженному электроду 4) остаются неподвижными
51. Коллоидные частицы, образующиеся при слиянии равных объёмов миллимолярного раствора нитрата серебра и сантимолярного раствора бромида натрия, в электрическом поле …. 1) совершают колебательные движения 2) перемещаются к катоду 3) перемещаются к аноду 4) остаются неподвижными
52. Ионы, вызывающие разрушение коллоидного раствора, называются …. 1) коагулирующими 2) потенциалопределяющими 3) адсорбционными 4) стабилизирующими
53. Коагулирующая способность ионов с увеличением их заряда …. 1) уменьшается 2) увеличивается 3) не изменяется 4) изменяется неоднозначно
54. С уменьшением заряда ионов их коагулирующая способность …. 1) не изменяется 2) изменяется неоднозначно 3) уменьшается 4) увеличивается
55. Метод получения коллоидных систем, основанный на дроблении частиц, называется …. 1) гидролитическим 2) диспергационным 3) конденсационным 4) пептизационным
56. Коллоиды, в которых вода не взаимодействует с ядрами коллоидных частиц, называются …. 1) гомогенными 2) гидрофобными 3) гидрофильными 4) гетерогенными
57. Скорость перемещения гранул в коллоидных растворах по сравнению с молекулами в истинных жидких растворах …. 1) одинакова 2) существенно меньше 3) больше 4) различается незначительно
58. Коллоидные растворы отличаются от истинных растворов наличием частиц …. 1) различной природы 2) меньших размеров 3) различной формой 4) бо́льших размеров
59. Метод разделения веществ, основанный на проникновении растворённых низкомолекулярных веществ и ионов через мембрану, непроницаемую для коллоидных частиц, называется …. 1) переносом 2) седиментацией 3) электрофорезом 4) диализом
60. Нейтрализация электрического заряда и удаление гидратной оболочки гранулы вызывает … коллоида.
1) изменение заряда 2) перераспределение 3) разрушение 4) стабилизацию
61. Частицы труднорастворимого вещества образуют … мицеллы. 1) ядро 2) адсорбционный слой 3) гранулу 4) агрегат
62. Процесс соединения коллоидных частиц в более крупные частицы называется …. 1) флотацией 2) стабилизацией 3) коагуляцией 4) седиментацией
63. Хаотическое движение частиц дисперсной фазы в дисперсионной среде называется …. 1) колебательным 2) прямолинейным 3) поступательным 4) броуновским
Ответы на тестовые упражнения
1.4; 2.3; 3.4; 4.3; 5.4; 6.4; 7.3; 8.2; 9.3; 10.2; 11.4; 12.1; 13.4; 14.4; 15.1; 16.1; 17.3; 18.4; 19.2; 20.3; 21.1; 22.3; 23.1; 24.4; 25.1; 26.4; 27.4; 28.3; 29.2; 30.3; 31.1; 32.2; 33.4; 34.2; 35.1; 36.3; 37.3; 38.4; 39.4; 40.1; 41.2; 42.3; 43.2; 44.3; 45.1; 46.1; 47.4; 48.3; 49.1; 50.3; 51.2; 52.1; 53.2; 54.3; 55.2; 56.2; 57.2; 58.4; 59.4; 60.3; 61.4; 62.3; 63.4.
ЛАБОРАТОРНАЯ РАБОТА № 1 АДСОРБЦИЯ Цель работы: изучение зависимости адсорбции веществ на поверхности раздела фаз от их природы. Приборы и посуда. Штатив для пробирок, штатив с держателем, пипетка, микрошпатель, резиновая груша, вата, стеклянная палочка, стеклянная воронка, пробирки с резиновыми пробками, химические стаканы ёмкостью 50 и 100 мл.
Реактивы и материалы. Водные растворы: серной кислоты (0,5 н.), аммиака (2 н.), хлорида бария (0,5 н.), хлорида алюминия (0,05 н.), иодида калия (0,01 н.), нитрата свинца (0,01 н.), метиленовой сини, лакмуса.
Прокалённый древесный уголь (порошок). Фильтровальная бумага. Указания по технике безопасности. Перед выполнением опытов необходимо изучить "Инструкцию по технике безопасности в химической лаборатории", обратив внимание на работу с растворами кислот и аммиака. Адсорбция красителей
а) адсорбация лакмуса активированным древесным углём
В стеклянную воронку вложите бумажный фильтр, смочите его водой и плотно прижмите к стенке. Закрепите воронку в держателе штатива и пропустите через неё 3 мл раствора лакмуса. Отметьте, изменился ли цвет раствора. Поместите в воронку с фильтром 6 микрошпателей порошка активированного древесного угля и пропустите через его слой четверть пробирки раствора лакмуса. Сравните цвета раствора лакмуса и фильтрата и объясните изменение окраски.
б) адсорбация метиленовой сини гидроксидом алюминия
В стакан с 50 мл раствора хлорида алюминия добавьте при перемешивании раствор аммиака до образования коллоидного раствора. Составьте уравнение протекающей химической реакции. Отфильтруйте осадок образовавшегося гидроксида алюминия, используя стеклянную воронку с бумажным фильтром, и затем через осадок на фильтре пропустите раствор метиленовой сини. Объясните наблюдаемый эффект. Адсорбция ионов
а) адсорбция ионов свинца(II) древесным углём
В пробирку с 4 каплями раствора нитрата свинца добавьте каплю раствора иодида калия. Отметьте, что происходит. Составьте уравнение протекающей химической реакции. В другую пробирку с 15 каплями раствора нитрата свинца, добавьте 2 микрошпателя порошка активированного древесного угля и, закрыв отверстие пробирки пробкой, энергично встряхивайте её содержимое в течение 3 минут. Оберните носик пипетки ватой и отберите через неё в чистую пробирку 4 капли раствора. Добавьте к этому раствору каплю раствора иодида калия. Что наблюдается в этом случае? Составьте уравнение протекающей химической реакции.
б) адсорбция ионов свинца(II) сульфатом бария
В пробирку с 4 каплями раствора нитрата свинца добавьте 10 капель дистиллированной воды и раствор перемешайте стеклянной палочкой. С помощью пипетки перенесите 4 капли полученного раствора во вторую пробирку и добавьте столько же капель раствора иодида калия. Отметьте, что происходит. Составьте уравнение протекающей химической реакции. В третью пробирку с 5 каплями раствора хлорида бария добавьте 10 капель раствора серной кислоты. Отметьте, что происходит. Декантируйте раствор, затем в пробирку с осадком добавьте 4 капли раствора нитрата свинца и 10 капель дистиллированной воды. Смесь перемешайте стеклянной палочкой. После отстаивания осадка с помощью пипетки перенесите в четвёртую пробирку 4 капли раствора и добавьте столько же капель раствора иодида калия. Отметьте, что происходит. Сравните количество образовавшегося осадка с выпавшим из раствора, в который не был добавлен сульфат бария. Объясните, почему уменьшилась концентрация ионов свинца в растворе? ЛАБОРАТОРНАЯ РАБОТА № 2 ДИСПЕРСНЫЕ СИСТЕМЫ Цель работы: изучение условий образования и коагуляции коллоидных растворов. Приборы и посуда. Штатив для пробирок, штатив с держателем, водяная баня, пробиркодержатель, асбестовая сетка, тренога, лупа, микрошпатель, стеклянная воронка, пипетка, стеклянная палочка, часовое стекло, 4 пробирки с резиновыми пробками, мерный цилиндр (на 20 мл), химические стаканы ёмкостью 50 и 100 мл, плоскодонная коническая колба ёмкостью 100 мл.
Реактивы и материалы. Водные растворы: хлороводородной (соляной) кислоты (2 н.), азотной кислоты (2 н.), гидроксида натрия (20 %-ный), хлорида натрия (насыщенный и 0,1 н.), хлорида бария (0,1 н.), хлорида алюминия (0,1 н.), хлорида железа(III) (концентрированный и 2 %), иодида калия (0,05 н.), нитрата серебра (0,001 н. и 0,05 н.), нитрата свинца (0,01 н.), карбоната натрия (10 %), силиката калия (10 %), сульфата натрия (0,1 н.), сульфита натрия (1 %), тиосульфата натрия (0,05 н.) фосфата натрия (0,1 н.), перманганата калия (0,05 н.), гексацианоферрата(II) калия (концентрированный и 0,05 н.), танина (0,1 %), мыла (2 %), желатина (0,5 %), фенолфталеина (1 %, спиртовый). Фильтровальная бумага. Мел и сера (мелко растёртые порошки), декагидрат тетрабората натрия (бура), бензол, этиловый спирт, машинное или растительное масло, флуоресцеин. Указания по технике безопасности. Перед выполнением опытов необходимо изучить "Инструкцию по технике безопасности в химической лаборатории", обратив внимание на работу с растворами кислот, аммиака и правила нагревания на газовой горелке пробирок с растворами веществ.
|
|||||||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 447; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.95.31 (0.012 с.) |






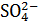 3)
3)  4)
4) 
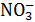 2) Cl– 3) K+ 4) Ag+
2) Cl– 3) K+ 4) Ag+


