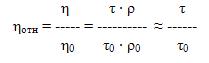Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Поверхностные явления. Способы получения и свойства коллоидных растворов.Содержание книги
Поиск на нашем сайте Коллоидно-дисперсные системы Коллоидная химия – наука, изучающая физико-химические свойства гетерогенных высокодисперсных систем в твердом состоянии и в растворах. Дисперсной системой называется система, в которой одно вещество в более или менее раздробленном (дисперсном) состоянии равномерно распределено в массе другого вещества. Раздробленное вещество в этом случае называют дисперсной фазой (ДФ), а среду, в которой оно распределено – дисперсионной средой (ДС). Степень дисперсности определяется величиной, обратной диаметру частиц. По степени дисперсности дисперсные системы классифицируют на: 1. Грубодисперсные (диаметр частиц больше 10-7 см) – не проходят через тонкие бумажные фильтры, быстро оседают, видимы в обычный микроскоп.
Классификация коллоидно - дисперсных систем 1. По степени взаимодействия дисперсной фазы и дисперсионной средыразличают: а) Лиофобные коллоиды - системы со слабым взаимодействием между дисперсной фазой и дисперсионной средой. б) Лиофильные коллоиды – системы с сильным взаимодействием между дисперсной фазой и дисперсионной средой. Если ДС является вода, то системы соответственно называются гидрофобными и гидрофильными. Лиофильные системы образуются самопроизвольно, следовательно, термодинамически устойчивы. Как правило, они представляют собой растворы полимерных органических соединений (белки, полисахариды). Лиофобные системы являются термодинамически неустойчивыми. Они образуются из неорганических соединений (солей, оснований).
а) Золи – бесструктурные коллоидные растворы, в которых частицы ДФ слабо взаимодействуют между собой и свободно передвигаются друг относительно друга. По внешнему виду золи напоминают истинные растворы. б) Гели – структурированные коллоидные растворы, в которых частицы ДФ связаны между собой с образованием пространственной структуры типа каркасов. В них коллоидные частицы малоподвижны и способны совершать только колебательные движения. По внешнему виду гели желеобразны. Строение коллоидных частиц В коллоидных системах структурной единицей является коллоидная частица или мицелла. Строение коллоидных частиц и возникновение на них заряда объясняет мицеллярная теория коллоидных систем в соответствии с которой заряд на коллоидных частицах возникает либо за счет ионизации молекул, находящихся на поверхности твердой фазы, либо в результате избирательной адсорбции на твердой фазе. Рассмотрим второй случай. Получим мицеллу СuS в K2S в результате реакции обмена СuС12 + K2S (избыток) = СuS + 2KС1 Нерастворимый продукт реакции СuS является агрегатом мицеллы и находится в избытке раствора K2S, выполняющего роль стабилизатора. На твердой кристаллической поверхности осадка в соответствии с правилом Панета-Фаянса будут адсорбироваться ионы стабилизатора S2–, достраивая кристаллическую решетку и сообщая частицам отрицательный заряд.Ионы S2– называются потенциалопределяющими ионами. Агрегат и потенциалопределяющие ионы составляют ядро мицеллы. К отрицательному заряду будут притягиваться противоионы K+, образуя плотный слой противоионов. Потенциалопределяющие ионы и противоионы плотного слоя вместе образуют адсорбционный слой. Адсорбционный слой вместе с агрегатом составляют гранулу (или частицу). Гранула заряжена, её заряд определятся знаком и величиной заряда потенциалопределяющих ионов. Часть противоионов, не вошедших в адсорбционный слой, образуют диффузный слой. Гранула и диффузный слой составляют мицеллу. Мицелла таким образом электронейтральна. Составим формулу мицеллы СuS в K2S: Устойчивость коллоидных растворов Устойчивость дисперсных систем характеризует способность дисперсной фазы сохранять состояние равномерного распределения частиц дисперсной фазы во всем объеме дисперсионной среды. В дисперсных системах различают седиментационную (кинетическую) и агрегативную устойчивость. Седиментационная устойчивость характеризует способность частиц дисперсной фазы находиться во взвешенном состоянии и не оседать под действием силы тяжести. Агрегативная устойчивость характеризует способность частиц дисперсной фазы противодействовать их слипанию между собой за счет адсорбционных сил. Коллоидные растворы седиментационно устойчивые системы, что обусловлено малыми размерами частиц, но агрегативно неустойчивы. В них самопроизвольно идут процессы слипания частиц, поэтому такие системы не могут существовать без стабилизаторов. Биологические жидкости – кровь, плазма, лимфа, моча – представляют коллоидные растворы. О состоянии организма можно судить по многим показателям этих жидкостей, и прежде всего, крови. Наличие патологических процессов сопровождается изменением количества форменных элементов крови (эритроцитов, лейкоцитов и др.), скорости оседания эритроцитов (СОЭ), свертываемости крови. Все эти свойства связаны с устойчивостью биологических жидкостей, поэтому изучение устойчивости коллоидных растворов очень важно в медицинской практике.
Контрольные вопросы 1. Межфазные явления, их термодинамическая характеристика. Сорбция. Адсорбция. Абсорбция. Физическая и химическая сорбция. 2. Понятие ПАВ, их свойства и применение в медицине. 3. Электролитная адсорбция, ее закономерности. Правила электролитной адсорбции. 4. Ионообменная адсорбция, ее закономерности. Иониты, их классификация. Ионообменная емкость, способы ее выражения. Применение ионитов в медицине 5. Определение коллоидных растворов. Сущность понятий «дисперсная фаза» и «дисперсионная среда». 6. Классификация коллоидных систем на золи и гели, лиофобные и лиофильные. 7. Общие и специфические свойства коллоидных растворов в сравнении с истинными растворами. 8. Молекулярно-кинетические свойства коллоидных систем. 9. Оптические свойства коллоидных систем. 10. Электрокинетические явления. Электрофорез и электроосмос и их значение для медицины. 11. Двойной электрический слой коллоидных систем. Способы образования двойного электрического слоя. 12. Мицелла и ее строение. 13. Электрокинетический или дзета-потенциал и его свойства. Зависимость агрегативной устойчивости мицеллы от величины дзета-потенциала и концентрации электролита. Изоэлектрические состояние мицеллы. 14. Устойчивость и коагуляция коллоидных систем. Правила электролитной коагуляции. Тестовые задания Выберите правильный вариант ответа 01. ДИСПЕРСНОСТЬ — ЭТО ВЕЛИЧИНА, ОБРАТНАЯ _________ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ 1) размеру 2) плотности 3) массы 4) объема
02. НА ПОВЕРХНОСТИ ОСАДКА AgI БУДУТ ПРЕИМУЩЕСТВЕННО АДСОРБИРОВАТЬСЯ АНИОНЫ 1) NO2– 2) CH3COO– 3) I– 4) NO3–
03. В КОЛЛОИДНОЙ ЧАСТИЦЕ, ОБРАЗУЮЩЕЙСЯ ПОД ДЕЙСТВИЕМ ИЗБЫТКА РАСТВОРА НИТРАТА СЕРЕБРА НА РАСТВОР ЙОДИДА КАЛИЯ ПОТЕНЦИАЛОПРЕДЕЛЯЮЩИМ БУДЕТ ИОН 1) Na+ 2) Cl– 3) Ag+ 4) NO3–
04. ПЕРЕМЕЩЕНИЕ КОЛЛОИДНЫХ ЧАСТИЦ ПОД ДЕЙСТВИЕМ ЭЛЕКТРИЧЕСКОГО ПОЛЯ К ПРОТИВОПОЛОЖНОЗАРЯЖЕННОМУ ЭЛЕКТРОДУ НАЗЫВАЕТСЯ 1) электроосмос 2) ультрафильтрация 3) электрофорез 4) диализ
05. КОАГУЛЯЦИЮ ЗОЛЯ, ПОЛУЧЕННОГО ПО УРАВНЕНИЮ K2SiO3 + H2SO4 (изб.) = H2SiO3 + K2SO4, БЫСТРЕЕ ВЫЗОВЕТ 1) сульфат-анион 2) ион калия 3) хлорид-анион 4) ион кальция
06. КОЛЛОИДНЫЕ РАСТВОРЫ ОТЛИЧАЮТСЯ ОТ ИСТИННЫХ РАСТВОРОВ ____ЧАСТИЦ 1) различной формой 2) отсутствием движения 3) большими размерами 4) меньшими размерами
07. КОАГУЛЯЦИЮ ЗОЛЯ ПОД ДЕЙСТВИЕМ ЭЛЕКТРОЛИТА ВЫЗЫВАЕТ 1) ион электролита с зарядом, одноименным заряду потенциалопределяющего слоя 2) катон и анион электролита 3) молекула электролита 4) ион электролита с зарядом, одноименным заряду диффузионного слоя
08. КОАГУЛИРУЮЩАЯ СПОСОБНОСТЬ ИОНОВ С УВЕЛИЧЕНИЕМ ИХ ЗАРЯДА 1) увеличивается 2) уменьшается 3) изменяется неоднозначно 4) не изменяется
09. КОЛЛОИДНЫЕ СИСТЕМЫ, В КОТОРЫХ РАСТВОРИТЕЛЬ (ВОДА) ВЗАИМОДЕЙСТВУЕТ С ЯДРАМИ КОЛЛОИДНЫХ ЧАСТИЦ, НАЗЫВАЮТСЯ 1) гидрофобными 2) гидрофильными 3) гидрогенными 4) гетерогенными
10. КОЛЛОИДНАЯ ЧАСТИЦА, ПОЛУЧЕННАЯ ПРИ ВЗАИМОДЕЙСТВИИ РАСТВОРА ХЛОРИДА БАРИЯ И ИЗБЫТКОМ СЕРНОЙ КИСЛОТЫ 1) имеет частичный положительный заряд 2) не имеет заряда 3) заряжена отрицательно 4) заряжена положительно Дополните высказывание 11. СТРУКТУРНОЙ ЕДИНИЦЕЙ КОЛЛОИДНОГО РАСТВОРА ЯВЛЯЕТСЯ _________.
12. МЕТОД ПОЛУЧЕНИЯ КОЛЛОИДНЫХ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ ПУТЕМ ДРОБЛЕНИЯ КРУПНЫХ ЧАСТИЦ НА БОЛЕЕ МЕЛКИЕ НАЗЫВАЕТСЯ __________________
13. ОСЕДАНИЕ КОЛЛОИДНЫХ ЧАСТИЦ ПОД ДЕ5ЙСТВИЕМ СИЛ РАЗНОЙ ПРИРОДЫ НАЗЫВАЕТСЯ ___________________
14. АГРЕГАТ И ПОТЕНЦИАЛ-ОПРЕДЕЛЯЮЩИЕ ИОНЫ СОСТАВЛЯЮТ __________. Контрольные задания 15. Напишите формулы мицелл и укажите их строение: 1) AgBr в KBr 2) BaCO3 в (NH4)2CO3 3) CaCO3 в CaC12 4) Cu2[Fe(CN)6] в K4[Fe(CN)6] 16. Составьте формулу мицеллы золя AgС1, полученной при взаимодействии равных объемов 0,01М раствора AgNO3 и 0,05 М раствора NaC1. Укажите, какой ион будет оказывать наибольшее коагулирующее действие в данном золе. 17. Составьте формулу частицы дисперсной фазы золя, полученного в результате реакции обмена при сливании 14 см3 0,007 моль/дм3 раствора ZnSO4 и 6 см3 0,004 моль/дм3 раствора NaOH.
Литература 1. Общая химия. Биофизическая химия. Химия биогенных элементов: Учеб. для вузов / Ю. А. Ершов, В.А. Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. – 5-е изд., стер. – М.: Высш.шк., 2005. – С. 423 – 446; 491 – 518. 2. Практикум по общей химии. Биофизическая химия. Химия биогенных элементов: Учеб. пособие для студентов медицинских спец. вузов / Ю.А. Ершов, А.М. Кононов, С.А. Пузаков и др.; Под ред. Ю.А. Ершова, В.А. Попкова. – М.: Высш. шк., 2008. – С. 207-214. Свойства растворов высокомолекулярных веществ (ВМВ) Растворы ВМВ Высокомолекулярные вещества (полимеры) – это вещества с молекулярной массой от десяти тысяч до нескольких миллионов единиц. Размеры молекул ВМВ в вытянутом состоянии могут достигать 1000 нм. Температура кипения ВМВ значительно выше температуры разложения, поэтому они существуют, как правило, только в жидком или твердом состоянии. По происхождению ВМВ делятся на: 1. Природные ВМВ или биополимеры (белки, нуклеиновые кислоты, полисахариды, а также биополимеры смешанного типа – гликопротеины, нуклеопротеины и др.) являются структурной основой всех живых организмов. 2.Синтетические (каучук, полиэтилен, синтетические смолы) и искусственные ВМВ получаются в результате химического синтеза. Методы синтеза ВМВ основаны на реакциях полимеризации, поликонденсации и сополимеризации. 3. Искусственные ВМВ изготавливают на основе природных ВМВ с заранее заданными свойствами. Степенью полимеризации n называется число повторяющихся звеньев в макромолекуле ВМВ. Любой синтетический полимер состоит из макромолекул разной степени полимеризации и характеризуется полидисперсностью. По строению полимерной цепи ВМВ бывают Ø линейными, Ø разветвленными, Ø пространственными. Например, целлюлоза (растительный полисахарид) – имеет линейную структуру, гликоген (животный полисахарид) – имеет разветвленную структуру, фенопласты – имеет пространственную сетчатую структуру. В животном организме присутствуют в основном плохорастворимые полимеры разветвленной и пространственной структур. По способности к электролитической диссоциации ВМВ делятся на Ø неэлектролиты Ø полиэлектролиты. Полиэлектролиты подразделяются на поликислоты, полиоснования и полиамфолиты. Макромолекулы могут принимать различную форму в результате конформационных изменений: линейную, клубка, глобул. Конформации и различные состояния объясняются стремлением к самопроизвольному уменьшению энергии Гиббса (∆G< 0), которое происходит при условии T·∆S > ∆H. Таким образом, конформация представляет собой пространственную форму макромолекул, соответствующую максимуму энтропии. Конформационными переходами можно объяснить многие процессы, происходящие в организме, например, регуляцию активности ферментов. Гибкость как свойство молекулы обусловливает эластичность как свойство материала (например, эластичность волос, кожи и т.п.). Макромолекулы ВМВ имеют уровни структурной организации. Для молекул белков известно 4 уровня структурной организации. Первичная структура – это последовательность аминокислотных остатков в полипептидной цепи. Вторичная структура – пространственная структура в виде α-спирали (фибриноген крови), либо β-структура складчатого листа (кератин волос). Третичная структура – расположение вторичной структуры в пространстве. При этом образуются субъединицы белка или микроструктуры. Четвертичная структура – объединение субъединиц в макроструктуры (гемоглобин крови). Нативная, природно заданная структура белка способна нарушаться под действием различных факторов (резкие колебания температуры, рН, присутствия солей тяжелых металлов и др.). Денатурация белка – это нарушение первоначальных свойств белка, вызванное изменением пространственной структуры его макромолекулы и сопровождающееся изменением физико-химических и биологических свойств белка. Белки в процессе денатурации: • теряют гидрофильные свойства, • нарушаются форма и размеры макромолекул, • увеличивается вязкость растворов, • уменьшается растворимость белков и степень набухания, • денатурированные белки быстрее перевариваются ферментами желудочно-кишечного тракта по сравнению с нативными. Растворы ВМВ являются лиофильными коллоидными системами. Для них характерны свойства как общие с растворами низкомолекулярных веществ и коллоидными системами, так и специфические. Растворы ВМВ с истинными растворами низкомолекулярных веществ имеют ряд общих свойств: 1) образуются самопроизвольно; 2) являются термодинамически устойчивыми и не требуют присутствия стабилизаторов; 3) в растворах ВМВ взвешенными частицами являются не мицеллы, а макромолекулы, способные диссоциировать на ионы; 4) в растворах ВМВ отсутствует четко выраженная поверхность раздела фаз, их можно разбавлять и концентрировать. К специфическим свойствам растворов ВМВ относят: 1) высокую степень набухания полимера; 2) высокая вязкость раствора; 3) низкую нестабильную величину осмотического давления раствора. Набухание ВМВ ВМВ набухают и растворяются в низкомолекулярных жидкостях. Так как подвижность молекул растворителя намного больше подвижности макромолекул, то первой стадией взаимодействия является набухание – проникновение молекул растворителя в структуру ВМВ со значительным увеличением его массы и объема, но с сохранением формы; образуется гель. Если низкомолекулярная жидкость ограниченно растворима в ВМВ, то набухание будет ограниченным, оно не заканчивается образованием текучей системы. Растянутая сетка макромолекул, стремясь сократиться, препятствует увеличению содержания растворителя. При неограниченной растворимости низкомолекулярной жидкости в полимере его пачки после набухания продолжают раздвигаться и макромолекулы постепенно диффундируют в растворитель, образуя раствор. Такое набухание называют неограниченным. В синтетических полярных полимерах и белках набухание начинается с сольватации полярных групп. При этом выделяется наибольшее количество теплоты. Установлено, что, например, на 1 г крахмала выделяется 6,6 кал, на 1 г желатина – 5,7 кал. При образовании сольватных слоев поглощается около 20–40% растворителя от массы сухого полимера. Следующая стадия набухания – поглощение десятикратного объема растворителя – объясняется осмотическими явлениями. С термодинамической точки зрения процессы набухания ВМС и растворения низкомолекулярных веществ весьма сходны между собой. На набухание влияют также такие физико-химические факторы, как температура, рН среды, электролиты и др. Повышение температуры способствует более быстрому набуханию, так как усиливается движение частиц, что способствует разрыхлению внутренних структур. Для каждого высокомолекулярного вещества и растворителя должна существовать своя критическая температура, выше которой происходит их безграничное смешение. Изменение рН среды в более кислую или щелочную сторону от изоэлектрической точки коллоида увеличивает степень набухания. Это объясняется появлением положительного и отрицательного заряда у коллоидных частиц и, следовательно, повышением степени гидратации. Влияние анионов на процесс набухания оценивают с помощью лиотропного ряда Гоффмейстера:
SO42- < C6H5O7 3- < C4H4O6 2- < C2H4O2 - < Cl - < NO3 - < Br - < I - < CNS – цитрат тартрат ацетат
Как видно из данного ряда, соли серной и уксусной кислот замедляют набухание, а роданид-анионы способствуют набуханию. Из катионов: K+ и Na+ способствуют, а ионы Ca2+ - препятствуют набуханию. Набухание оценивается по степени набухания массы жидкости, поглощенной 1 г сухого полимера. Степень набухания определяют весовым и объемным методом. Весовым методом определяют массу сухого и набухшего полимера и по разности находят массу поглощенной жидкости. Объемным методом измеряют изменение объема тела при поглощении им жидкости, или объема жидкости, в котором происходит набухание. Степень набухания α вычисляют по уравнению:
m0, V0 – масса и объем полимера до набухания m, V – масса и объем полимера после набухания
Набухание имеет большое значение в процессах жизнедеятельности растительных и животных организмов. Прорастанию семян всегда предшествует предварительное набухание. Растительные и животные ткани связывают большое количество воды (соединительная ткань) и содержат коллоиды не только в виде растворов, но и в студнеобразном состоянии (протоплазма клеток, хрусталик глаза и др.). Чередование в зависимости от рН среды и концентрации электролитов процессов набухания и обезвоживание соединительной ткани влияет на распределение воды, а также ионов между соединительной тканью и клетками. Набухание и обезвоживание коллоидов наблюдается при самых различных процессах: регенерации тканей, воспалении, образовании отеков, при проникновении кислых жидкостей в ткани, при ожоге кожи крапивой, при укусе насекомых и т.п. Во всех указанных случаях набухание зависит, главным образом, от изменения в тканях рН среды.
Вязкость растворов ВМВ Растворы высокомолекулярных соединений отличаются высокой вязкостью (или внутренним трением), обусловленной силами сцепления между молекулами жидкости. Количественно вязкость характеризуют коэффициентом вязкости η (этта), Па ∙ с. Отношение вязкости раствора к вязкости чистого растворителя обозначают относительной вязкостью:
где, η, ρ, τ – вязкость, плотность, время истечения раствора; η0, ρ0, τ0 – вязкость, плотность, время истечения чистого растворителя. ! В сильно разбавленных растворах ρ ≈ 1г/см3, т.е. плотностью можно пренебречь.
Увеличение вязкости, связанное с изменением концентрации при растворении полимера, принято характеризовать удельной вязкостью:
η – вязкость раствора; η0 – вязкость чистого растворителя. Для линейной (вытянутой) формы макромолекул удельную вязкость рассчитывают по уравнению Штаудингера: ηуд. = К· М(X) · C(X) М (Х) – относительная молекулярная масса полимера [а. е. м.]; C (X) – весовая концентрация полимера [г · м-3]; К – константа, характеризующая особенности гомологического ряда полимера. Величина ηуд/С получила название приведенной вязкости:
Предел ηуд/С при С→0 отражает гидродинамическое сопротивление движению молекул полимера и именуется характеристической вязкостью [η].
При вискозиметрическом методе определения молекулярного веса полимера вначале устанавливают η0, η; затем рассчитывают ηуд и ηприв для растворов различной концентрации и строят график зависимости приведенной вязкости от концентрации. Эта зависимость представляет прямую, которая при продолжении до пересечения с осью ординат отсекает отрезок, равный [η].
Рис. Зависимость ηприв от С ВМВ для раствора высокомолекулярного соединения.
Уравнение Марка-Хаувинка устанавливает связь между характеристической вязкостью и молярной массой ВМВ. [η] = К ∙ Мα, где М – средняя молекулярная масса ВМВ; К – коэффициент постоянный для растворов ВМВ одного гомологического ряда в данном растворителе; α – коэффициент, характеризующий гибкость цепей макромолекул в растворе и их форму в зависимости от конформации. Осмотическое давление растворов ВМВ В растворах ВМВ осмотическое давление имеет ряд особенностей. Это связано с тем, что макромолекула ВМВ может рассматриваться как совокупность молекул меньшего размера. Это учитывает уравнение Галлера: πосм = (СВМВ/МВМВ) ∙ RТ+βС2ВМВ, где СВМВ – весовая концентрация полимера, г/м3; β – коэффициент, учитывающий форму, гибкость, размеры макромолекулы. Если концентрация раствора невелика, то βС2ВМВ → 0, тогда уравнение Галлера переходит в уравнение Вант-Гоффа. Измеряя осмотическое давление растворов различных концентраций и строя график зависимости πосм/ СВМВ от СВМВ, находят значение молярной массы полимера и коэффициента β.
Контрольные вопросы 1. ВМВ. Биополимеры. Белки. Биологическая роль белков и их суточная потребность. 2. Физико-химические характеристики макромолекул белков: молекулярная масса, размер, структура, гибкость. 3. Специфические свойства растворов ВМВ: а) Набухание. Степень набухания, факторы, влияющие на набухание. Ограниченное и неограниченное набухание. б) Вязкость. Удельная, приведенная и характеристическая вязкости. в) Осмотическое давление. 4. Растворы белков. Агрегативная устойчивость белков. Понятие о высаливании, денатурации, коацервации. 5. Влияние рН среды на состав и свойства растворов белков. Изоэлектрическая точка белков и ее значение.
Типовые задачи Задача 1. Определите молярную массу полиметилметакрилата по следующим данным вискозиметрического метода:
Константы: К = 4,7·10– 8; α = 0,77.
Решение: 1. По приведенным данным строим график зависимости ηприв — Сраствора. Методом экстраполяции определяем значение характеристической вязкости ([η]). В нашем случае [η] ≈ 0,4035.
2. Используя уравнение Марка-Хаувинка, находим молярную массу полимера:
[η] = К ∙ Мα lg [η] = lg K + α∙lg M α∙lg M = lg [η] – lg K
lg [η] – lg K lg 0,4035 – lg 4,7·10– 8 lg M = ----------------- = ------------------------------- = 9,005 α 0,77
M = 10 9,005 = 1011579454 (кг/моль)
Ответ: М = 1011579454 (кг/моль) Тестовые задания Выберите правильный вариант ответа 01. НАБУХАНИЕ – ЭТО ПРОЦЕСС ПРОНИКНОВЕНИЯ 1) ВМВ в полимер 2) полимера в ВМВ 3) ВМВ в НМС 4) НМС в ВМВ
02. ПРОЦЕСС НАБУХАНИЯ ВМВ ЯВЛЯЕТСЯ 1) самопроизвольным, ΔG > 0 2) несамопроизвольным, ΔG > 0 3) самопроизвольным, ΔG < 0 4) несамопроизвольным, ΔG < 0
03. НАБУХАНИЕ БЕЛКОВ ПРОИСХОДИТ ПРИ: А) ВОЗНИКНОВЕНИИ ОТЕКОВ; Б) СОКРАЩЕНИИ МЫШЦ; В) ПЕРЕВАРИВАНИИ ПИЩИ; Г) ТЕРМИЧЕСКОЙ КУЛИНАРНОЙ ОБРАБОТКЕ ПИЩИ 1) а, б, в 2) а, в, г 3) а, б, в, г 4) а, в
04. УВЕЛИЧЕНИЕ ВЯЗКОСТИ КРОВИ ПРОИСХОДИТ ПРИ: А) АТЕРОСКЛЕРОЗЕ; Б) ВЕНОЗНЫХ ТРОМБОЗАХ; В) ПОВЫШЕНИИ КОНЦЕНТРАЦИИ БЕЛКА В ПЛАЗМЕ; Г) ОТЕКАХ; Д) СНИЖЕНИИ КОНЦЕНТРАЦИИ БЕЛКА В ПЛАЗМЕ КРОВИ 1) а, б, в 2) а, б, в, г 3) а, б, г 4) а, в, г
05. ПОЛИСТИРОЛ ЯВЛЯЕТСЯ 1) неорганическим полимером 2) олигомером 3) синтетическим полимером 4) природным полимером
06. КРАХМАЛ И ЦЕЛЛЮЛОЗА ЯВЛЯЮТСЯ 1) неорганическим полимером 2) олигомером 3) синтетическим полимером 4) природным полимером
07. В ИЗОЭЛЕКТРИЧЕСКОМ СОСТОЯНИИ ПОЛИЭЛЕКТРОЛИТЫ 1) обладают наибольшей устойчивостью 2) имеют наибольшую степень набухания 3) обладают наименьшей устойчивостью 4) обладают электрофоретической подвижностью Установите соответствие 08.УРАВНЕНИЕ И ЕГО МАТЕМАТИЧЕСКОЕ ВЫРАЖЕНИЕ
Дополните высказывание 09. УВЕЛИЧЕНИЕ ОБЪЕМА И МАССЫ ПОЛИМЕРА ПРОИСХОДИТ В ПРОЦЕССЕ _____________.
10. КОЛЛИЧЕСТВЕННОЙ ХАРАКТЕРИСТИКОЙ ПРОЦЕССА ОГРАНИЧЕННОГО НАБУХАНИЯ СЛУЖИТ ____________________.
11. УВЕЛИЧЕНИЕ ВЯЗКОСТИ, СВЯЗАННОЕ С ИЗМЕНЕНИЕМ КОНЦЕНТРАЦИИ РАСТВОРА ПРИ РАСТВОРЕНИИ ПОЛИМЕРА, ХАРАКТЕРИЗУЮТ _______________. Контрольные задания 12. Рассчитайте среднюю молярную массу полимера, если характеристическая вязкость его равна 0,126 м3/кг, константа К = 5∙10 – 5; α = 0,67. 13. Определите молярную массу полимера по следующим данным:
К = 4,21·10– 4; α = 0,67 14. Время истечения из вискозиметра для 0,8%-го раствора полимера (С5Н5Сl-)n равно 53 с, время истечения растворителя — 40 с. Рассчитайте относительную, удельную и приведённую вязкости. Литература 1. Общая химия. Биофизическая химия. Химия биогенных элементов: Учеб. для вузов / Ю. А. Ершов, В.А. Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. – 5-е изд., стер. – М.: Высш.шк., 2005. – С. 526 – 545. 2. Практикум по общей химии. Биофизическая химия. Химия биогенных элементов: Учеб. пособие для студентов медицинских спец. вузов / Ю.А. Ершов, А.М. Кононов, С.А. Пузаков и др.; Под ред. Ю.А. Ершова, В.А. Попкова. – М.: Высш. шк., 2008. – С. 227-237.
Биогенные элементы Химия биогенных элементов В начале 20 века советским академиком В.И. Вернадским на основе геохимии, биологии и биохимии была создана новая наука – биогеохимия. Биогеохимия – наука, изучающая взаимосвязь элементарного химического состава земной коры и живых организмов, а также миграцию химических элементов и их круговорот в системе «живая материя – земля». Биогеохимияизучает химические процессы, происходящие в земной коре с участием живых организмов. Часть земной оболочки, занятая растительными и животными организмами образует биосферу. В процессе деятельности живых организмов в биосфере образуются минералы и различные природные вещества. Известно около 90 химических элементов в составе земной коры. В составе живых организмов обнаружено около 70 химических элементов периодической системы. Химические элементы, находящиеся в живом организме и обладающие выраженной биологической ролью – называются биогенными элементами. Отбор биогенных элементов в процессе эволюции происходил под влиянием следующих факторов: 1. Распространенность элементов в земной коре. 2. Заряд атомного ядра. Биогенные элементы в основном легкие элементы. 3. Растворимость природных соединений данного элемента в воде. 4. Энергия гидратации иона. 5. Значения координационных чисел атомов. В зависимости от массовой доли элемента (ω%) в организме элементы делят на следующие группы: 1) Макроэлементы с ω (х)>0,01% от массы организма - C, O, H, N, P S, Cl, Ca, Na, Mg, K, Fe. 2) Микроэлементы с ω (х) от 10-3 до 10-5 % от массы организма – Cu, Mo, Co, Cr, F, Br, I и др. 3) Ультрамикроэлементы с ω (х) <10-5 % от массы организма – Hg, Au, Ra и др. Такие элементы, как C, O, H, N,P,S относятся к органогенам. Они входят в состав каждой клетки и в состав биополимеров – белков, нуклеиновых кислот, углеводов. Эти 12 элементов составляют 99,99% массы живого субстрата и 99% живых тканей содержат только эти элементы. 10 металлов, жизненно необходимых для живого организма получили название «металлы жизни»: Ca, K, Na, Mg, Fe, Zn, Cu, Mn, Mo, Co. Различна биологическая роль этих групп элементов. Макроэлементы в организме выполняют роль пластического материала, участвуют в построении тканей, поддержании осмотического давления, кислотно–основного равновесия (гомеостаза), рН среды. Микроэлементы входят в структуру и активные центры ферментов, находятся в составе витаминов, гормонов, влияют на обмен белков, жиров, углеводов. Биологическая роль ультрамикроэлементов изучена мало. По расположению в периодической системе биогенные элементы относятся к s,p и d – семействам химических элементов. При этом, как правило: S - элементы – образуют электролитную среду в крови и других биологических жидкостей(Na, Mg, K, Ca, Н); Р - элементы – это органогены (С, S, N О); D - элементы главным образом микроэлементы. Установлена связь между положением химических элементов в периодической системе и их биологической ролью. Элементы IА группы – влияют на деятельность сердечной мышцы и кровообращения. Элементы IIА группы – оказывают влияние на процессы образования костей, действие гормона инсулина. Элементы VА группы – участвуют в процессах окислительного распада веществ в организме. Элементы VIА группы – способны к взаимному замещению в биологических соединениях. Существует общее правило: в организме количественное содержание химического элемента убывает с увеличением его порядкового номера, при этом возрастает токсичность соединений элементо в. Органы и среды человека по-разному концентрируют в себе химические элементы. Водород и кислород – макроэлементы входят в состав Н2О, которой в организме человека примерно 65%. Углерод, водород, азот, фосфор, кислород – входят в состав белков примерно 80%, которых содержится в селезенке, легких, мышцах. Углерод, водород, кислород – входят в состав углеводов, липидов, которые концентрируются в печени, сыворотки крови. Кальций, магний и фосфор содержатся в костной ткани, твердых тканях зубов; Мо – в почках; Zn – в поджелудочной железе; I – в щитовидной железе; Sr – в костях; Mn, Cr, Br – в гипофизе; Ва – в сетчатке глаза. Большинство микроэлементов концентрируются в печени – функциональном депо микроэлементов. Биогенные элементы в организме находятся как в свободной ионизированной форме, так и в составе различных соединений. Например, железо в кислой среде желудка содержится в виде свободных ионов Fe2+ и Fe3+; щелочной среде кишечника находится в виде Fe(OH)3; в крови – в составе гемоглобина как комплексообразователь Fe2+ с координационным числом 6. Современная медицина широко исследует взаимосвязь между содержанием химических элементов в организме и развитием различных заболеваний. Оказалось, что особенно чутко организм реагирует на изменение концентраций микроэлементов. Так при развитии гипертонической болезни в крови и эритроцитах более, чем в 2 раза уменьшается содержание лития, при инфаркте миокарда в плазме крови снижается содержание ионов Zn2+. Концентрация элемента в живом веществе прямо пропорциональна его содержанию в среде обитания с учетом растворимости соединений элемента. Согласно биогеохимической теории В.И. Вернадского существует «биогенная миграция атомов» по цепочке воздух → почва → вода → пища → человек, в результате которой практически все элементы, окружающие человека во внешней среде, в большей или меньшей степени проникают внутрь организма. В 1926 году академик В.И. Вернадский предложил выделить участки земной коры, отличающиеся накоплением одних элементов и обедненных другими элементами. Эти участки были названы – биохимическими провинциями. Таким образом, одни организмы попадают в условия избытка какого-либо элемента, а другие – недостатка. Это приводит к возникновению эндемических заболеваний характерных для какой-то определенной местности или региона. Например, у лиц, проживающих в областях удаленных от моря, где в воде и растениях наблюдается недостаток иода, развивается эндемическое заболевание щитовидной железы. При избытке фтора в питьевой воде возникает флюфоз – заболевание зубной эмали. Избыток свинца наблюдается на Алтае, меди – на южном Урале. Таким образом, количественное определение содержания элементов в природных источниках, органах, тканях в норме и патологии имеет большое значение для прогнозирования, диагностики и лечения различных заболеваний. Ежедневное поступление химических элементов с пищей должно находиться на определенном уровне:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-15; просмотров: 689; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.230 (0.012 с.) |


 или
или  , где
, где