
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тесты к экзамену по физколлоидной химииСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Первый раствор содержит в 100 мл 1026 частиц; второй – в 1 л 1023 частиц; третий – в 0,5 л 1022 частиц; четвёртый – в 2 л 1027 частиц. В каком растворе осмотическое давление больше? а) в первом; б) во втором; в) в третьем; г) в четвёртом. Тесты по химии - физическая химия Тест Законы Вант - Гоффа и Рауля для растворов неэлектролитов и электролитов
Электрическая проводимость растворов - тестирование
Тесты по коллоидной химии Некоторые концентрированные обратные эмульсии (В/М) можно отнести к связнодисперсным системам, так как частицы дисперсной фазы, соприкасаясь, создают достаточно пластичный, упругий, вязкий каркас, включающий частицы дисперсионной среды. Какие пищевые продукты можно отнести к системам этого типа? а) Сливочное масло, спреды, маргарины; б) Творог; в) Сырое тесто; г) Мармелад; Д) Майонезы.
Тестирование Основные понятия и определения предмета «Коллоидная химия» (тест для проведения ККР)
1.Выберите определение, наиболее полно раскрывающее содержание понятия. Коллоидная химия – это… А) Самостоятельный раздел физической химии; Б) Наука о поверхностных явлениях и дисперсных системах; В) Наука о высокомолекулярных соединениях (ВМС); Г) Наука о процессах, протекающих в жидких дисперсионных средах.
2.Дисперсность – это… а)Количественный параметр, указывающий на степень раздробленности вещества, размер межфазной поверхности; Б) Мера раздробленности вещества; В) Мелко раздробленное состояние вещества; Г) Величина, равная удельной поверхности вещества.
3. Какие признаки наиболее характерны для объектов коллоидной химии? а) Гетерогенность; Б) Наличие межфазной поверхности; В) Термодинамическая устойчивость; Г) Гомогенность; Д) Дисперсность
4. Укажите свойства, не присущие коллоидным системам: а) Прозрачность; б)Появление конуса Тиндаля при освещении в темноте сбоку проекционным фонарем; В) Гомогенность; Г) Наличие большого осмотического давления.
5. Какие разделы почвоведения тесно связаны с предметом коллоидной химии? а) Химический состав почв и грунтов; б) Строение и свойства почвенного поглощающего комплекса; в) Ионный обмен в почвах; г) Биохимия гумуса.
6. Какие физико-химические системы имеют свойства, во многом сходные со свойствами коллоидных систем с жидкой дисперсионной средой? а) Водные растворы полиэлектролитов; б) Водно-солевые растворы; в) Микрогетерогенные системы: суспензии, эмульсии, пены; г) Бинарные системы, образованные двумя органическими жидкостями – гомологами; д) Ассоциативные коллоиды.
7. Какое определение не отражает сущности физического параметра? Поверхностное натяжение определяет… а) Степень гетерогенности; б) Резкость перехода от одной фазы к другой; в) Степень взаимодействия между соприкасающимися фазами; г) Различие между соприкасающимися фазами.
8. Какие методы получения коллоидных систем относятся к дисперсионным? А) Механические методы; б) Метод гидролиза солей; в) Ультразвуковой метод; г) Метод замены растворителя.
9. Какие методы получения коллоидных систем относятся к конденсационным? а) Механические методы; б) Метод гидролиза солей; в) Ультразвуковой метод; г) Метод замены растворителя.
10. Установите соответствие:
11. Все молекулярно-кинетические свойства коллоидных систем являются следствием… а) Броуновского движения; б) Кинетической теории газов; в) Теплового движения частиц; г) Основных законов термодинамики.
12. Установите соответствие:
13. Установите соответствие:
14. Устойчивость дисперсионной системы определяется ее способностью сохранять начальную степень дисперсности частиц и их равномерное распределение в дисперсионной среде. Различают кинетическую и агрегативную устойчивости.
Укажите факторы кинетической устойчивости золей. а) Дисперсность системы; б) Вязкость среды; в) Присутствие в растворе посторонних веществ (электролитов или ВМС); г) Разность плотностей дисперсионной среды и дисперсной фазы.
15. Укажите факторы агрегативной устойчивости золей. а) Броуновское движение; б) Температура; в) Дисперсность; г) Присутствие в растворе посторонних веществ (электролитов или ВМС).
16. Какие определения не соответствуют содержанию понятия «коагуляция»? а) Процесс укрупнения мицелл золя за счет соединения друг с другом; б) Процесс всплытия створоженной дисперсной фазы; в) Процесс слипания мицелл золя под влиянием внешнего воздействия; г) Явление прохождения через поры фильтра свежеосажденного осадка при промывании большим количеством воды.
17. Какое из перечисленных свойств в одинаковой степени присуще лиозолям и суспензиям? а) Эффект Фарадея – Тиндаля; б) Диффузия; в) Коагуляция; г) Пептизация.
18. Порог коагуляции оценивается величиной минимальной концентрации электролита (моль/л), вызывающий коагуляцию. Он зависит от величины зарядов ионов добавляемых электролитов. Установлено, что коагулирующим действием обладают противоионы, а способность к коагуляции увеличивается пропорционально его заряду, взятому в некоторой степени. Как называется это именное правило? а) Правило Нернста – Шилова; б) Правило Траубе – Дюкло; в) Закон Бойля – Мариотта; г) Правило Шульце –Гарди.
19. Слили одинаковые объемы двух водных растворов: 0,1 М раствора йодида калия и 0,05 М раствора нитрата серебра. Какая из формул правильно отражает строение образовавшихся мицелл коллоидного раствора? а) {m[AgI] n I - (n – x) K+}-x xK+
б) {m[AgI] n Ag+ (n – x) NO3-}+x xNO3- в){m[AgI] n Ag+ n I-} г) {m[AgI] n K+ (n – x) NO3-}+x xNO3-
20. Какой из ионов будет обладать наибольшим коагулирующим действием на полученный золь? (См. задание 19) а) Ca2+ б) Al3+ в) SO42- г) PO43-
21. Тиксотропия – специфическое свойство коагуляционных структур. Какое из определений не соответствует сущности этого понятия? а) Восстановление структуры системы после снятия нагрузки; б) Явление изотермического обратимого перехода «золь ↔ гель»; в) Необратимый переход «гель → золь»; г) Увеличение прочности структуры со временем после снятия напряжения.
22. Большинство дисперсных систем агрегативно неустойчивы. Они обладают избытком поверхностной энергии, поэтому в них самопроизвольно идут процессы ее снижения за счет укрупнения частиц. Укрупнение может идти двумя путями: 1 – Эффект Кельвина или изотермическая перегонка – перенос вещества от мелких частиц к крупным; 2 – Коагуляция – слипание или Коалесценция – слияние частиц.
По какому пути пойдут указанные процессы и явления? а) Выпадение дождя; б) Скисание молока; в) Помутнение пива; г) Рост сталактитов в пещерах; д) «Старение» мыльной пены; е) Расслоение майонеза
23. Какие золи называются «белыми»? а) Мутноватые; б) Имеющие голубоватый цвет сбоку и красноватый на просвет; в) Бесцветные; г) Не поглощающие свет.
24. Чем отличаются частички красного золя золота от синего? а) Формой: б) Степенью дисперсности; в) Временем существования: синий золь «старше» красного; г) Они одинаковы, но наблюдаются под разным углом зрения.
25. В каких случаях может наблюдаться опалесценция в коллоидных системах? а) При наблюдении в проходящем свете; б) При наблюдении в отраженном свете; в) На темном фоне; г) При искусственном освещении.
26. С чем связаны голубой цвет неба и морской воды? а) Присутствием в атмосфере и морской воде твердых частиц коллоидного размера; б) Наличием флуктуаций плотности; в) Расположением наблюдателя под определенным углом зрения к источнику света; г) Присутствием окрашенных веществ.
27. Устройство каких приборов основано на явлении опалесценции? А) Фотоэлектроколориметр (ФЭК); Б) Ультрамикроскоп; В) Электронный микроскоп; Г) Нефелометр.
28. Какие слои не характерны для строения мицелл гидрозолей? А) Диффузный; Б) Дипольный; В) Адсорбционный; Г) Ван-дер-ваальсовый; Д) Изоэлектрический.
29. Какие составные части коллоидной частицы движутся в электрическом поле? а) Гранула; б) Ядро; в) Агрегат; г) Мицелла; д) Диффузный слой; е) Адсорбционный слой.
30. Установите соответствие:
31. Установите соответствие:
32. Установите соответствие:
33.Укажите основной признак наличия межфазной поверхности: а) Гетерогенность системы; б) Гомогенность ситемы; в) Раздробленность вещества до размеров менее 1 мкм. г) проявление эффекта Фарадея – Тиндаля.
Тесты Ассоциатиавные коллоиды – растворы поверхностно – активных веществ (ПАВ). Растворы высокомолекулярных соединений (ВМС). Растворы полиэлектролитов 5.1. Понятие поверхностной активности было введено для анализа уравнения адсорбции Гиббса. Какое определение наиболее полно раскрывает сущность понятия «поверхностно – активные вещества»? ПАВ – это вещества… а) Обладающие моющей способностью – детергенты; б) Дифильного строения, обладающие гидрофильной и олефильной частями, способные уменьшать поверхностное натяжение на границе раздела фаз. в) Способные адсорбироваться на поверхности раздела фаз; г) Обладающие положительным значением величины адсорбции. 5.2. Укажите основные типы ПАВ. а) Ионогенные; б) Амфотерные; в) Неионогенные; г) Нейтральные; д) Оксиэтилированные. 5.3. Укажите основные технологические функции ПАВ. а) Пластификаторы; б) Вспениватели; в) Смачиватели; г) Коагулянты; д) Гидрофобизаторы; е) Ионизаторы; ж) Эмульгаторы. 5.4. Какие физико–химические системы в современной научной литературе принято называть «ассоциативными коллоидами» вместо устаревших понятий «полуколлоиды», «семиколлоиды»? а) Водные растворы низкомолекулярных органических веществ; б) Вещества, обладающие моющими свойствами, мыла или детергенты; в) Дифильные органические вещества, способные образовывать термодинамически устойчивые гетерогенные дисперсные системы; г) Истинно растворимые ПАВ. 5.5. Какие физико-химические свойства наиболее полно характеризуют ассоциативные коллоиды? а) Поверхностная инактивность; б) Способность к самопроизвольному мицеллообразованию при определенных концентрациях; в) Высокая поверхностная активность; г) Способность образовывать истинные растворы в широком диапазоне концентраций; д) Способность к солюбилизации. 5.6. Какие физико-химические параметры позволяют количественно оценить ассоциативные или мицеллярные коллоиды? а) Величина предельной мономолекулярной (Ленгмюровской) адсорбции; б) Значение ГБЛ – гидрофильно-липофильного баланса; в) Величина поверхностной активности; г) Величина ККМ – критической концентрации мицеллообразования. 5.7. Какое явление получило название «солюбилизации»? а) Явление самопроизвольного растворения дифильных ПАВ в воде с образованием термодинамически устойчивых растворов; б) Явление самопроизвольного перехода нерастворимых веществ в раствор с помощью мицелл ПАВ с образованием термодинамически устойчивого изотропного раствора; в) Явление образования сферических мицелл Гартли; г) Явление образования гелеобразной структуры. 5.8. Какие свойства являются специфичными для ВМС? а) Нелетучесть; б) Независимость свойств от формы молекул; в) Постепенное размягчение при нагревании; г) Наличие определенной температуры плавления; д) Температура разложения меньше температуры кипения. 5.9. Что такое «точка Крафта» для ассоциативных коллоидов? а) Концентрация ПАВ в растворе, выше которой начинается мицеллообразование; Б) Температура образования жидкокристаллической структуры; В) Критическая, пороговая температура, выше которой начинается мицеллообразование; Г) Концентрация ПАВ, при которой наступает застудневание. 5.10. Вещества, обладающие моющим действием, называют Детергентами или тензидами, Так как при их адсорбции на поверхности раздела «раствор – воздух» поверхностное натяжение воды уменьшается с 0,07 до 0,03 - 0,04 Н/м. Какую геометрическую конфигурацию имеют: 1) мицеллы Гартли; 2) мицеллы Мак – Бена; 3) мицеллы Дебая? а) Пластинчатую и дискообразную; б) Сферическую; в) Складчатую; г) Цилиндрическую; д) Нитеобразную. 5.11. Какие из предлагаемых коллоидных систем являются однофазными, обратимыми, термодинамически устойчивыми? а) Золи и суспензии; б) Мицеллярные растворы ПАВ микроэмульсии; в) Пены; г) Водные растворы полиэлектролитов; д) Капиллярные системы. 5.12. В основе молекулярной теории растворов ВМС Штаудингера лежит утверждение: Растворы ВМС содержат отдельные, не связанные друг с другом макромолекулы, соизмеримые с коллоидными частицами - мицеллами. Какие доказательства свидетельствуют в пользу этой теории? а) Растворы ВМС – гетерогенные системы, агрегативно неустойчивые без стабилизатора; б) Растворы ВМС – гомогенные, термодинамически устойчивые системы, подчиняющиеся правилу фаз Гиббса; в) Растворение ВМС идет самопроизвольно, часто с выделением энергии; г) Диспергирование ВМС требует затраты энергии. 5.13. Растворение ВМС предваряет процесс набухания. Это… а) Экзотермический процесс; б) Эндотермический процесс; в) Процесс, не сопровождающийся выделением или поглощением тепла. 5.14. Какие виды воды характерны для набухших полимеров? а) Поляризационная; б) Гидратационная (Связанная); в) Криоскопическая; г) Капиллярная (Свободная). 5.15. Растворы ВМС, как и лиозоли, в определенных условиях способны терять текучесть и переходить в системы, проявляющие ряд свойств твердого тела. Эти системы носят название… а) Гели; б) Клеи; в) Студни; г) Слизни; д) Латексы. 5.16. Какие свойства присущи студням? а) Эластичность; б) Тиксотропия; в) Набухание; г) Синерезис; д) Контракция; Е) Коацервация; Ж) «Память» к способу получения. 5.17. Какие из перечисленных ВМС являются полиэлектролитами? а) Полиолефины; б) Нуклеиновые кислоты; в) Белки; г) Фенолформальдегидные смолы; д) Карбоксиметилцеллюлоза; е) Натуральный и синтетический каучуки; ж) Гуммиарабик. 5.18. Известно, что заряд частиц белка зависит от рН среды. Как называется состояние, в котором суммарный заряд частицы белка равен нулю? а) Равновесное; б) Нейтральное; в) Изоэлектрическое; г) Полиэлектролитное; Д) Стабильное. 5.19. Как будет заряжена молекула белка, если значение изоэлектрической точки (ИЭТ): 1) меньше рН раствора; 2) больше рН раствора? а) Положительно; б) Отрицательно; в) Заряд равен нулю; 5.20. Белок, входящий в состав пшеничного зерна, – глиадин, имеет ИЭТ =7,1. Как будет заряжена молекула белка в нейтральной водной среде? а) Положительно; б) Отрицательно; в) Заряд равен нулю; 5.21. ИЭТ казеина – белка молока равна 4,6. Как будет заряжена молекула белка в нейтральной водной среде? а) Положительно; б) Отрицательно; в) Заряд равен нулю; 5.22. К какому электроду будет двигаться молекула казеина (ИЭТ = 4,6) при электрофорезе? а) К катоду (-); б) К аноду(+) в) Останется неподвижной. 5.23. Какому значению рН соответствует минимальное значение вязкости растворов полиэлектролитов? а) рН = 7; б) рН = ИЭТ; в) рН >7; г) рН <7. 5.24. Установите соответствие:
ТЕСТЫ К ЭКЗАМЕНУ ПО ФИЗКОЛЛОИДНОЙ ХИМИИ Тема: Агрегатное состояние вещества. Законы идеальных газов. 1. Агрегатное состояние вещества может быть: твёрдым, жидким, газообразным и плазмой; 2. Тип агрегатного состояния вещества зависит при данных условиях: от характера взаимодействия частиц и расстояния между ними; 3. Твёрдые вещества могут иметь следующие типы кристаллических решёток: ионные, атомные, молекулярные, металлические; 4. В узлах кристаллической решётки могут находиться: атомы, ионы, молекулы; 5. Найдите соответствие: хлорид натрия – ионная решётка; б) графит – молекулярная решётка; железо – проводит электрический ток, т. к. в узлах решётки находятся электроны; воск, парафин – имеют неодинаковые свойства в разных направлениях. 6. Плазма получается: при нагревании газа до высоких температур; 7. Выберите показатели, которые могут быть измерены для жидкостей: а) подвижность, текучесть, сжимаемость, полярность; б) вязкость, плотность, поверхностное натяжение; в) температура кипения, кристаллизации, возгона, критическая температура; г) летучесть, прозрачность, показатель отражения. 8. Газ можно: а) уменьшать в объёме и сжижать; б) охлаждать до -273,5° С; в) превратить в твёрдое вещество при резком расширении; г) превратить в жидкость выше критической температуры под большим давлением. 9. Газ является идеальным, если… а) он состоит из одинаковых атомов; б) можно не учитывать массы и взаимодействие частиц газа; в) частицы газа находятся друг от друга на одинаковом расстоянии; столкновения частиц газа являются упругими и нечастыми. 10. Состояние идеального газа описывается равенством: а) PV = nRT; б) PV/T = P0V0/T0; в) p = CRT; г) PT = mRV. 11. Универсальная газовая постоянная равна: а) изменению объёма при нагревании 1 моль газа на 1° К при 101,3 кПа; б) работе расширения 1 моль газа при нагревании его на 1° К; в) работе расширения 1 моль газа при нагревании его на 1° К при 101,3 кПа; г) изменению давления 1 моль газа при нагревании его на 1° К при объёме газа 1 л. 12. Относительная плотность этана по воздуху равна: а) 1,0; б) 1,5; в) 2; г) 0,5. 13. В 1 л любого газа при н. у. содержится молекул: а) 0,27 · 1023; б) 0,27 · 1026; в) 6,02 · 1023; г) 6,02 · 1026. 14. В каком газе больше молекул, если массы газов одинаковы: а) в азоте; б) в кислороде; в) в сероводороде; г) число молекул одинаково. 15. Парциальное давление газа: а) часть общего давления газа в смеси газов; б) равно общему давлению газа в газовой смеси; в) пропорционально объёму газовой смеси; г) пропорционально исходному давлению газа. 16. Смешали три газа объёмом по 1 л, находящиеся под давлением 1 атм. в ёмкости объёмом 3 л. Парциальное давление газов и общее давление смеси равно: а) 1 атм.; 3 атм.; б) 0,33 атм.; 1 атм.; в) 0,33 атм.; 3 атм.; г) 3 атм.; 1 атм. 17. Смешали 1 л водорода (1 атм.), 2 л углекислого газа (2 атм.) в баллоне на 0,5 л. Давление смеси равно: а) 10 атм.; б) 3 атм.; в) 1,5 атм.; г) 1 атм. 18. Найдите правильное соответствие: а) чем больше давление при постоянной температуре, тем меньше объём газа; б) чем меньше парциальные давления газов, тем больше давление газовой смеси; в) 1 л влажного воздуха весит больше 1 л сухого воздуха; г) при сжимании газовой смеси парциальные давления газов в смеси уменьшаются.
19. Давление 1 кг водорода объёмом 1 м3 при 0° С равно….. кПа: а) 1544,0; б) 1133,0; в) 273,0; г) 8,3. 20. Объём 1 моль кислорода при 0° С и давлении 1 атм. равен: а) 1 л; б) 22,4 л; в) 1 м3; г) 10 л. Тема: Первое начало термодинамики. 21. Энергия – это: мера движения и взаимодействия; 22. Системы бывают: а) изолированные (не обмениваются энергией с внешней средой); б) закрытые (обмениваются только энергией); в) открытые (обмениваются только массой); 23. Теплота, подведённая к системе, идёт на: б) увеличение внутренней энергии и на работу; 24. Изохорные процессы идут при: б) постоянном объёме; 25. Изобарные процессы идут при: а) постоянном объёме; б) постоянном давлении; в) постоянной температуре; г) отсутствии теплообмена. 26. Изотермические процессы идут при… а) постоянном объёме; б) постоянном давлении; в) постоянной температуре; г) отсутствии теплообмена. 27. Теплота, подведённая к системе в изобарном процессе, идёт на изменение… а) свободной и связанной энергии; б) внутренней энергии системы и на работу против сил внешнего давления; в) внутренней и внешней энергии; г) температуры системы. 28. Энтальпия – функция состояния и равна… а) внутренней энергии и работе; б) сумме связанной и свободной энергии; в) внутренней энергии; г) тепловому эффекту химической реакции. 29. Теплота изохорного процесса равна изменению… а) энтальпии; б) свободной энергии; в) внутренней энергии; г) потенциальной энергии. 30. Тепловой эффект химической реакции зависит от… а) состояния реагирующих веществ; б) состояния продуктов реакции; в) состояния реагирующих веществ и продуктов реакции; г) пути процесса. Тема: Второе начало термодинамики. 31. Свободная энергия – часть… а) внутренней энергии, способная переходить в теплоту; б) внутренней энергии, способная переходить в работу; в) тепловой энергии, выделяющейся во внешнюю среду; г) связанной энергии, переходящая в работу. 32. Самопроизвольные процессы идут: а) спонтанно, без воздействия внешних сил; б) под воздействием внешних сил; в) необратимо; г) обратимо. 33. Энтропия и свободная энергия Гиббса определяют… а) вероятность и направление самопроизвольных процессов; б) направление несамопроизвольных процессов; в) полноту обратимых процессов; г) вероятность и направление всех процессов. 34. Изменение энтропии рассчитывается по формуле: а) DS = DH/T; б) DS = Qобр./T; в) DS = DU/T; г) DS = DG/T. 35. Энтропия повышается при… а) переходе вещества из твёрдого состояния в жидкое и парообразное; б) повышении количества связей в системе; в) уменьшении числа частиц в системе; г) понижении температуры. 36. Изменение свободной энергии Гиббса имеет вид… а) DG = DH – TDS; б) DG = DU – TDS; в) DG = A – DQ; г) DG = DQ + TDS.
37. Внутренняя энергия системы… а) совокупность всех видов потенциальной энергии; б) сумма всех видов кинетической энергии; в) сумма всех видов свободной энергии; г) сумма всех видов энергии. 38. Внутренняя энергия системы зависит от: а) температуры; б) положения системы; в) скорости движения системы; г) упорядоченности её структуры. 39. В самопроизвольных процессах свободная энергия… а) возрастает; б) понижается; в) не меняется; г) вначале растёт, потом понижается. 40. В изолированных системах самопроизвольно идут процессы, если повышается… а) температура; б) энтропия; в) энтальпия; г) давление. Тема: Законы Рауля. 41. Насыщенный пар – это пар… а) находящийся в равновесии с жидкостью; б) полученный при нагревании жидкости до t° кипения; в) способный конденсироваться; г) способный совершать работу. 42. Если в воде растворить нелетучее вещество, то давление насыщенного пара… а) повысится; б) понизится; в) не изменится; г) или понизится, или повысится. 43. Зависимость давления насыщенного от концентрации раствора имеет вид: а) P = P0 C; б) DP = P0 N; в) P = P0 CT; г) DP = P0 CRT. 44. При температуре кипения: а) давление пара максимально; б) давление пара равно атмосферному; в) летучая жидкость начинает испаряться; г) пар становится насыщенным.
45. Температура кипения зависит от: а) природы жидкости; б) атмосферного давления; в) формы поверхности жидкости; г) количества жидкости. 46. Если в воде растворить нелетучее вещество, то температура кипения: а) повысится; б) понизится; в) не изменится; г) или повысится, или понизится. 47. Зависимость температуры кипения от концентрации раствора имеет вид: а) t = KЭC; б) t = KЭCR; в) Dt = KЭC; г) Dt = KЭCR. 48. При температуре замерзания: а) давление пара минимально; б) жидкость не испаряется; в) давление пара над твёрдой и жидкой фазами равно атмосферному; г) давление пара над твёрдой и жидкой фазами одинаково. 49. В присутствии нелетучего вещества температура замерзания жидкости… а) понижается; б) повышается; в) не меняется; г) или повышается, или понижается. 50. Зависимость температуры замерзания от концентрации раствора имеет вид… а) t = KКC; б) t = KКCR; в) Dt = KКC; г) Dt = KКCR. Тема: Осмос, осмотическое давление. 51. Диффузия: а) процесс перемещения частиц; б) процесс выравнивания температуры во всех частях системы; в) самопроизвольное выравнивание концентрации во всех частях системы за счёт теплового движения частиц; г) самопроизвольное упорядоченное движение частиц из одной части системы в другую за счёт собственной теплоты. 52. Осмос – это: а) односторонняя самопроизвольная диффузия молекул растворителя через полупроницаемую мембрану из раствора с меньшей концентрацией в раствор с большей концентрацией; б) диффузия молекул растворителя через полупроницаемую мембрану под действием внешнего давления; в) самопроизвольная диффузия молекул растворённых веществ через полупроницаемую мембрану из раствора с большей концентрацией в раствор с меньшей концентрацией; г) Односторонняя диффузия молекул растворителя и растворённых веществ через полупроницаемую мембрану с целью выравнивания концентраций. 53. Осмотическое давление зависит… а) от природы растворителя и растворённых веществ; б) от давления насыщенного пара растворителя; в) от концентрации раствора; г) от температуры кипения. 54. Осмотическое давление рассчитывается по формуле: а) p = CDT; б) p = CRT; в) p = KRT; г) p = CRK. 55. Растворы, имеющие одинаковые осмотические давления называютс |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-06; просмотров: 4237; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.174.4 (0.02 с.) |








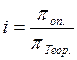





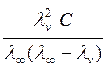


 κ
κ





