
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Функциональная организация иммунной системыСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Виды иммунитета
Функциональная организация иммунной системы
Организация и правила техники безопасности Правила работы в микробиологической лаборатории Основные правила работы в базовой лаборатории включают: • запрет работ с пипеткой при помощи рта; • запрет приема пищи, питья, курения, хранения пищи и применения косметических средств в рабочих помещениях; • поддержание чистоты и порядка; • дезинфекцию рабочих поверхностей не реже 1 раза в день и после каждого попадания на них заразного материала; • мытье рук персоналом после работы с заразным материалом, животными, перед уходом из лаборатории; • проведение всех работ таким образом, чтобы свести к минимуму возможность образования аэрозоля; • обеззараживание всех инфицированных материалов перед выбросом или повторным использованием. Антигены понятие химическая структура
10.
11. Специфичность – структурные особенности, отличающие один антиген от другого. Способность вызывать развитие иммунного ответа и определять его специфичность обладает фрагмент молекулы антигена – антигенная детерминанта (эпитоп), избирательно реагирующая с антигенраспознающими рецепторами и антителами. Молекула антигена может иметь несколько эпитопов, то есть быть поливалентной. Чем сложнее молекула антигена и чем больше у нее эпитопов, тем больше вероятность развития иммунной ответа. Структура, обладающая индивидуальной антигенной специфичностью, называется антигенным детерминантом, или эпитопом. Последнее название отражает то, что антигенной активностью обладают только структуры лежащие на поверхности молекулы, а глубокие проявляют антигенность лишь при изменении конформации или разрушении молекулы. Разнообразие белковых эпитопов достигается за счет мозаики аминокислотных остатков, расположенных на глобулярной поверхности молекулы белка. Специфичность определяют структурные особенности антигена, в частности структура антигенной детерминанты, или эпитопа. Практически в любой молекуле антигена есть несколько антигенных детерминант, или эпитопов, определяющих ее специфичность. Иммунная система через TCR или антитело распознает не весь антиген, а часть молекулы, определяемую как доминантный эпитоп. 12.
Персистенция, вирусная персистенция - сохранение вируса в функционально активном состоянии в клетках организма или культур ткани за пределами тех сроков, которые характерны для острой инфекции. Механизмы персистенции антигенов в организме: Пути проникновения: В результате фагоцитоза, через поврежденный эпителий, через цитоплазму эпителиальных клеток, через ходы в эпителии. Локализация: Аккумуляция в местах максимального скопления макрофагов(печень,почки, костный мозг, селезенка) Аккумулируются в регионарных лимфатических узлах. В слизистой оболочке. Элиминация антигенов: 1 фаза- диффузия растворимого аг и его распределение в сосудистом русле и тканях. 2 фаза- ферментативное расщепление аг. 3 фаза- иммунная элиминация. 13. Механизмы врожденного иммунитета: Врождённый иммунитет - наиболее ранний защитный механизм как в эволюционном плане (он существует практически у всех многоклеточных), так и по времени ответа, развивающегося в первые часы и дни после проникновения чужеродного материала во внутреннюю среду, т.е. задолго до развития адаптивной иммунной реакции. Значительную часть патогенов инактивируют именно врождённые механизмы иммунитета, не доводя процесс до развития иммунного ответа с участием лимфоцитов. И только если механизмы врождённого иммунитета не справляются с проникающими в организм патогенами, в «игру» включаются лимфоциты. При этом адаптивный иммунный ответ невозможен без вовлечения механизмов врождённого иммунитета. Кроме того, врождённый иммунитет играет главную роль в удалении апоптотических и некротических клеток и реконструировании повреждённых органов. В механизмах врождённой защиты организма важнейшую роль играют первичные рецепторы для патогенов, система комплемента, фагоцитоз, эндогенные пептиды-антибиотики и факторы защиты от вирусов - интерфероны. 14-15 Антигенпредставляющие клетки или антигенпрезентирующие клетки (АПК, англ. antigen-presenting cell, APC) — клетки, которые экспонируют чужеродный антиген в комплексе с молекулами главного комплекса гистосовместимости (англ. MHC) на своей поверхности. Т-лимфоциты могут распознавать такие комплексы при помощи Т-клеточных рецепторов (англ. TCR). Антигенпредставляющие клетки процессируют антиген и представляют его Т-клеткам. основные антигенпрезентирующие клетки: макрофаги, дендритные клетки, В-лимфоциты. Процессы переработки и презентации антигенных пептидов природы антигенов: эндогенных (вирусы, внутриклеточные бактерии, опухоли, в том числе аутоантигены, и др.) и экзогенных (микроорганизмы, токсины, аллергены, разнообразные белки и др.). Эндогенные антигены после ферментативной деградации в протеасоме транспортируются в эндоплазматический ретикулум с участием переносчиков ТАР-1 и ТАР-2, где образуют комплекс с молекулой HLA класса I» синтезируемой в ретикулуме. Затем комплекс с помощью транспортной системы аппарата Гольджи транспортируется на клеточную поверхность АПК и презентируется CD8+ Т-лимфоцитам. Экзогенные пептиды презентируются в комплексе с молекулами HLA класса II. В эндоплазматическом ретикулуме синтезируются молекулы HLA класса II, которые вначале стабилизируются с помощью шаперона калнексина, а затем с помощью инвариантной цепи. Фрагмент этой цепи CLIP встраивается в бороздку молекулы HLA класса II. Везикулы, содержащие такие молекулы HLA (без антигенного пептида), сливаются с ранними эндосомами или первичными лизосомами, которые содержат экзогенные белки.
16\ Фагоцитоз-это комплекс клеточных событий, в основе которых лежит распознавание, опсонизация, поглощение и элиминация из организма корпускулярных частиц размером меньше 0,5 мкм. Моноциты Моноциты – одно их первых названий, которые всплывают в памяти при упоминании о фагоцитозе. Эти осуществляющие фагоцитоз лейкоциты непрерывно перемещаются в крови, «сканируя» окружающее пространство на предмет наличия в нем вредоносных объектов. Найдя «обидчика», они захватывают и уничтожают его. После этого, избавившись от продуктов расщепления бактерии, микропаразита или вируса, они продолжают свою работу в аналогичном направлении. При фагоцитозе моноцит справляется с вредными объектами всего за 9 минут. Иногда он поглощает и расщепляет клетки и субстраты, превышающие его по размерам в несколько раз.
Нейтрофилы Фагоцитоз нейтрофилов осуществляется похожим образом, с той лишь разницей, что они работают по принципу «Светя другим, сгораю сам». Это значит, что, захватив патоген и уничтожив его, нейтрофил погибает.
Макрофаги Макрофаги – это осуществляющие фагоцитоз лейкоциты, образовавшиеся из моноцитов крови. Они располагаются в тканях: как непосредственно под кожей и слизистыми, так и в глубине органов. Существуют особые разновидности макрофагов, которые находятся в конкретных органах. Например, в печени «живут» клетки Купфера, задача которых состоит в разрушении старых компонентов крови. В легких располагаютсяальвеолярные макрофаги. Эти клетки, способные к фагоцитозу, захватывают вредные частицы, проникшие в легкие с вдыхаемым воздухом, и переваривают их, разрушая своими ферментами: протеазами, лизоцимом, гидролазами, нуклеазами и т.д. Обычные тканевые макрофаги обычно погибают после встречи с патогенами, то есть в этом случае происходит то же, что и при фагоцитозе нейтрофилов.
Дендритные клетки Эти клетки – угловатые, ветвистые – совершенно не похожи на макрофаги. Тем не менее, они являются их родственниками, так как тоже образуются из моноцитов крови. К фагоцитозу способны только молодые дендритные клетки, остальные в основном «работают» слимфоидной тканью, обучая лимфоциты правильно реагировать на некоторые антигены.
Тучные клетки Помимо того, что тучные клетки запускают реакцию воспаления, эти лейкоциты способны к фагоцитозу. Особенность их работы состоит в том, что они уничтожают только грамотрицательные бактерии. Причины такой «разборчивости» не совсем понятны, видимо, у тучных клеток есть к этим бактериям особое сродство. Они могут уничтожить сальмонеллу, кишечную палочку, спирохету, многих возбудителей ЗППП, но совершенно равнодушно воспримут возбудителя сибирской язвы, стрептококка и стафилококка. Борьбой с ними займутся другие лейкоциты. Перечисленные выше клетки – это профессиональные фагоциты, об «опасных» свойствах которых известно всем. А теперь несколько слов о тех клетках, для которых фагоцитоз – не самая типичная функция.
Тромбоциты Тромбоциты, или кровяные пластинки, занимаются главным образом тем, что отвечают за свертываемость крови, прекращают кровотечения, формируют тромбы. Но, помимо этого, у них обнаружены и фагоцитарные свойства. Тромбоциты могут образовывать ложноножки и уничтожать некоторые вредные компоненты, попавшие в организм.
Клетки эндотелия Оказывается, клеточная выстилка сосудов тоже представляет опасность для бактерий и прочих «захватчиков», проникших в организм. В крови с чужеродными объектами борются моноциты и нейтрофилы, в тканях их поджидают макрофаги и другие фагоциты, и даже в стенках сосудов, находясь между кровью и тканями, «враги» не могут «чувствовать себя в безопасности». Воистину, возможности защиты организма чрезвычайно велики. При увеличении содержания в крови и тканях гистамина, что происходит при воспалении, фагоцитирующая способность клеток эндотелия, почти незаметная до этого, возрастает в несколько раз!
Гистиоциты Под этим собирательным названием объединяют все клетки тканей: соединительной ткани, кожи, подкожной клетчатки, паренхимы органов и так далее. Раньше этого никто не мог предположить, но оказывается, при определенных условиях многие гистиоциты способны менять свои «жизненные приоритеты» и тоже приобретать способность к фагоцитозу! Повреждения, воспаление и другие патологические процессы пробуждают в них эту способность, которая в норме отсутствует.
17\ Методика определения фагоцитарной активности лейкоцитов Принцип метода. Некоторые клетки белой крови (гранулоциты и в меньшей степени моноциты) способны in vitro и in vivo поглощать, а часто и разрушать чужеродные частицы с помощью своих ферментов. Причем сам процесс проходит несколько стадий, которые включают хемотаксис, фагоцитоз, разрушение микробов и переваривание поглощенных веществ. При повторном контакте или специфической иммунизации клетки опсонируются, т. е. эта способность усиливается. Разработано большое число методик определения фагоцитарной активности клеток крови. Для этих целей используют определенную тест-систему (конкретный вид микробов, зимозан). В одних случаях реакцию проводят в пробирках или чашках Петри на агаре, а в других — внутри организма животного (внутрисосудисто, интраперитенально или методом «окошка рога»). Сокращенный вариант: Определение фагоцитарной активности лейкоцитов. Определение С-реактивного белка крови Берут 0,05 мл 2% лимоннокислого натрия, 0,1 мл крови, 0,05 мл взвеси микробов убитых или живых бактериальной флоры стафилококка. Можно взять и в следующих пропорциях: 0,25 мл 2% лимоннокислого натрия, 0,5 мл крови из вены, 0,25 мл взвеси микробов. Пробирку помещают на 30 минут в термостат при температуре 37°. После извлечения из термостата встряхивают и готовят мазки, фиксируют спиртом и окрашивают по Романовскому — Гимза 20—30 минут. Подсчитывают микробы, фагоцитированные 25 нейтрофилами. Максимальный показатель составляет 75, если фагоцитоз всех 25 лейкоцитов оценен тремя плюсами, т. е. если каждым лейкоцитом поглощен 41 микроб.
18\ Гуморальное звено иммунитета характеризуют уровни CD3-CD19+, CD3-CD20+, CD3-CD21+ и CD3-CD22+-клеток (В-лимфоцитов в разные фазы созревания), а также уровни иммуноглобулинов разных классов (IgМ, IgG, IgE, сывороточного и секреторного IgA). Поскольку синтез антител является Т-зависимым процессом, для надлежащей оценки гуморального звена иммунитета следует учитывать уровень
19\
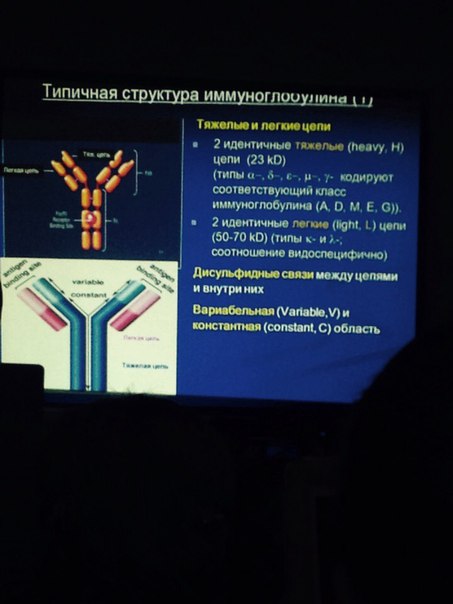
Для гуморального иммунитета характерна выработка специфических антител (иммуноглобулинов). Антитела - специфические белки гамма- глобулиновой природы, образующиеся в организме в ответ на антигенную стимуляцию и способные специфически взаимодействовать с антигеном (in vivo, in vitro). В соответствии с международной классификацией совокупность сывороточных белков, обладающих свойствами антител, называют иммуноглобулинами. Уникальность антител заключается в том, что они способны специфически взаимодействовать только с тем антигеном, который вызвал их образование. Иммуноглобулины (Ig) разделены в зависимости от локализации на три группы: - сывороточные (в крови); - секреторные (в секретах- содержимом желудочно- кишечного тракта, слезном секрете, слюне, особенно- в грудном молоке) обеспечивают местный иммунитет (иммунитет слизистых); - поверхностные (на поверхности иммунокомпетентных клеток, особенно В- лимфоцитов). Любая молекула антител имеет сходное строение (Y- образную форму) и состоит из двух тяжелых (Н) и двух легких (L) цепей, связанных дисульфидными мостиками. Каждая молекула антител имеет два одинаковых антигенсвязывающих фрагмента Fab (fragment antigen binding), определяющих антительную специфичность, и один Fc (fragment constant) фрагмент, который не связывает антиген, но обладает эффекторными биологическими функциями. Он взаимодействует со “своим” рецептором в мембране различных типов клеток (макрофаг, тучная клетка, нейтрофил). Концевые участки легких и тяжелых цепей молекулы иммуноглобулина вариабельны по составу (аминокислотным последовательностям) и обозначаются как VL и VH области. В их составе выделяют гипервариабельные участки, которые определяют структуру активного центра антител (антигенсвязывающий центр или паратоп). Именно с ним взаимодействует антигенная детерминанта (эпитоп) антигена. Антигенсвязывающий центр антител комплементарен эпитопу антигена по принципу “ключ - замок” и образован гипервариабельными областями L- и Н- цепей. Антитело свяжется антигеном (ключ попадет в замок) только в том случае, если детерминантная группа антигена полностью вместится в щель активного центра антител. Легкие и тяжелые цепи состоят из отдельных блоков- доменов. В легких (L) цепях - два домена- один вариабельный (V) и один константный (C), в тяжелых (H) цепях- один V и 3 или 4 (в зависимости от класса иммуноглобулина) C домена. Существуют легкие цепи двух типов- каппа и лямбда, они встречаются в различных пропорциях в составе различных (всех) классов иммуноглобулинов. Выявлено пять классов тяжелых цепей- альфа (с двумя подклассами), гамма (с четырьмя подклассами), эксилон, мю и дельта. Соответственно обозначению тяжелой цепи обозначается и класс молекул иммуноглобулинов- А, G, E, M и D. Именно константные области тяжелых цепей, различаясь по аминокислотному составу у различных классов иммуноглобулинов, в конечном результате и определяют специфические свойства иммуноглобулинов каждого класса. Известно пять классов иммуноглобулинов, отличающихся по строению тяжелых цепей, молекулярной массе, физико- химическим и биологическим характеристикам: IgG, IgM, IgA, IgE, IgD. В составе IgG выделяют 4 подкласса (IgG1, IgG2, IgG3, IgG4), в составе IgA- два подкласса (IgA1, IgA2). Структурной единицей антител является мономер, состоящий из двух легких и двух тяжелых цепей. Мономерами являются IgG, IgA (сывороточный), IgD и IgE. IgM- пентамер (полимерный Ig). У полимерных иммуноглобулинов имеется дополнительная j (joint) полипептидная цепь, которая объединяет (полимеризует) отдельные субъединицы (в составе пентамера IgM, ди- и тримера секреторного IgA). Основные биологические характеристики антител. 1. Специфичность - способность взаимодействия с определенным (своим) антигеном (соответствие эпитопа антигена и активного центра антител). 2. Валентность- количество способных реагировать с антигеном активных центров (это связано с молекулярной организацией- моно- или полимер). Иммуноглобулины могут быть двухвалентными (IgG) или поливалентными (пентамер IgM имеет 10 активных центров). Двух- и более валентные антитела навывают полными антителами. Неполные антитела имеют только один участвующий во взаимодействии с антигеном активный центр (блокирующий эффект на иммунологические реакции, например, на агглютинационные тесты). Их выявляют в антиглобулиновой пробе Кумбса, реакции угнетения связывания комплемента. 3. Афинность - прочность связи между эпитопом антигена и активным центром антител, зависит от их пространственного соответствия. 4. Авидность - интегральная характеристика силы связи между антигеном и антителами, с учетом взаимодействия всех активных центров антител с эпитопами. Поскольку антигены часто поливалентны, связь между отдельными молекулами антигена осуществляется с помощью нескольких антител. 5. Гетерогенность - обусловлена антигенными свойствами антител, наличием у них трех видов антигенных детерминант: - изотипические - принадлежность антител к определенному классу иммуноглобулинов; - аллотипические- обусловлены аллельными различиями иммуноглобулинов, кодируемых соответствующими аллелями Ig гена; - идиотипические- отражают индивидуальные особенности иммуноглобулина, определяемые характеристиками активных центров молекул антител. Даже тогда, когда антитела к конкретному антигену относятся к одному классу, субклассу и даже аллотипу, они характеризуются специфическими отличиями друг от друга (идиотипом). Это зависит от особенностей строения V- участков H- и L- цепей, множества различных вариантов их аминокислотных последовательностей. Понятие о поликлональных и моноклональных антителах будет дано в следующих разделах. 27. · РЕАКЦИЯ ПРЕЦИПИТАЦИИ – это агрегация антителами (преципитинами) растворимых (молекул) АГ (преципитиногенов), проявляющаяся в помутнении прозрачной жидкости, в появлении преципитата в виде осадка, кольца и т.д. Антиген для реакции преципитации обязательно должен быть в молекулярном виде. Механизм реакции преципитации аналогичен реакции агглютинации, т.е. по «теории решетки». Осаждение из раствора комплексов АГ – АТ происходит в диапазоне эквивалентных соотношений концентраций взаимодействующих молекул. В случае большого избытка одного из реагентов образуется растворимый комплекс АГ–АТ и феномен реакции не проявляется. Поскольку преципитиноген имеет ультрамикроскопическое строение и его концентрация в единице объема выше, чем АТ в таком же объеме сыворотки, то для осаждения более легких частичек АГ с образованием видимого преципитата необходимо значительно большее количество АТ. Поэтому диагностические преципитирующие сыворотки выпускают с высоким титром АТ. Реакцию преципитации можно проводить в жидкой и твердой среде. Реакция преципитации и ее варианты. Сущность данной реакции состоит в осаждении (преципитации) антигена, находящегося в дисперсном коллоидном состоянии, воздействием специфических антител в растворе электролита. Механизмы реакций агглютинации и преципитации аналогичны и описываются теорией «решетки». Реакция преципитации является высокочувствительным тестом, так как позволяет обнаружить малые количества антигена или гапте-на. Высокая чувствительность реакции преципитации позволяет использовать ее для выявления антигенов с помощью известных антисывороток. В одном из вариантов последовательные разведения антигена наслаивают на стандартное разведение диагностической сыворотки в пробирках, при этом осадок образуется в виде кольца на границе двух сред (кольцепреципитация). Реакцию оценивают по максимальному разведению антигена, при котором наблюдается кольцо преципитации визуально. Кроме того, помутнение может быть зафиксировано инструментальными методами - нефелометрией и др. Реакция преципитации применяется в лабораторной практике при диагностике инфекционных заболеваний, а также в судебной медицинской экспертизе для определения видовой принадлежности белков, в частности белков кровяных пятен, спермы и т.д. С помощью этой реакции в санитарной практике определяют фальсификацию рыбных и сных изделий. В биологии реакция прециации используется для установления степени филогенетического родства различных ядов животных и растений. Реакция преципитации. В реакции преципитации (РП) в результате взаимодействия антител с высокодисперсными растворимыми антигенами (белки, полисахариды) образуются комплексы с участием комплемента — преципитаты. Это чувствительный тест, используемый для выявления и характеристики разнообразных антигенов и антител. Простейшим примером качественной РП является образование непрозрачной полосы преципитации в пробирке на границе наслоения антигена на иммунную сыворотку — реакция кольцепреципитации. Широко применяют различные разновидности РП в полужидких гелях агара или агарозы (метод двойной иммунодиффузии, метод радиальной иммунодиффузии, иммуноэлектрофорез). · Реакция агглютинации и ее варианты. Реакция агглютинации (agglutinacio - склеивание) внешне проявляется в склеивании и выпадении в осадок корпускулярных антигенов: бактерий, эритроцитов, а также частиц с адсорбированными на них антигенами под влиянием антител в среде с электролитом. Реакция протекает в две фазы. В первой фазе происходит специфическая адсорбция антител на поверхности клетки или частицы, несущей соответствующие антигены, во второй - образование агрегата (агглютината) и выпадение его в осадок, причем этот процесс происходит только в присутствии электролита (раствор хлорида натрия). Механизм реакции агглютинации описывается теоpией «решетки», согласно которой агглютинат образуется при соединении одного активного центра двухвалентного антитела с детерминантной группой одного антигена, а второго активного центра - с детерминантной группой другого антигена. Избыток или недостаток антител препятствует проявлению агглютинации. Для постановки реакции агглютинации используют корпускулярные антигены (суспензии бактерий, эритроцитов). Характер и скорость реакции зависят от антигенного строения. бактериальной клетки. Мелкозернистую О-агглютинацию дают бактерии, лишенные жгутиков. О-агглютинация протекает медленно. При наличии Н-антигена реакция проявляется в образовании крупно-хлопьевидного осадка и протекает значительно быстрее. Реакция агглютинации недостаточно специфична и чувствительна. По данным признакам она уступает другим серологическим реакциям (преципитации, связывания комплемента и т.д.). Повысить специфичность и чувствительность реакции можно путем разведения исследуемой сыворотки до ее титра или половины титра. Титром сыворотки называется то ее максимальное разведение, в котором обнаруживается агглютинация антигена. Чем выше титр сыворотки, тем достовернее результаты реакции. Чтобы дифференцировать причину положительной реакции (ранее перенесенная инфекция, вакцинация или текущее заболевание), оценивают динамику нарастания титра антител, которое наблюдается только при текущей инфекции. При наличии у разных бактерий одинаковых или сходных групповых антигенов они могут агглютинироваться одной и той же антисывороткой, что затрудняет их идентификацию. В таких случаях применяют реакцию адсорбции антител по Кастеллани. Данная реакция основана на способности родственных групп бактерий адсорбировать из антисыворотки групповые антитела при сохранении в ней типос-пецифических антител. Полученные сыворотки называются моноре-цепторными, так как содержат антитела только к одному определенному антигену. Они применяются для детального изучения антигенной структуры бактерий с целью определения их серовара. Реакция непрямой, или пассивной, агглютинации (РПА). Под непрямой, или пассивной, агглютинацией понимают реакцию, в которой антитела взаимодействуют с антигенами, предварительно адсорбированными на клетках или частицах. В качестве сорбентов чаще всего применяют эритроциты различных животных, частицы целлюлозы, бентонита или латекса. В некоторых случаях пользуются обратным вариантом, т.е. адсорбируют на эритроцитах или иных частицах не антигены, а антитела. Реакция агглютинации (РА) основана на применении корпускулярного антигена (взвесь бактерий, сенсибилизированных эритроцитов, частиц латекса и др.), взаимодействующего со специфическими антителами, в результате чего образующийся комплекс антиген — антитело выпадает в виде осадка. Эту реакцию широко применяют в лабораторной практике для серологической диагностики бактериальных инфекций и для идентификации выделенных микроорганизмов.
28. · Реакция нейтрализации Реакция биологической нейтрализации вируса (РН), основанная на способности специфических антител достаточно прочно соединяться с вирусной частицей, начала применяться еще на заре вирусологии. В результате взаимодействия между вирусом и антителом происходит нейтрализация инфекционной активности вируса вследствие блокады антигенных детерминант, ответственных за соединение вирусных частиц с чувствительными клетками. В результате вирус утрачивает способность размножаться в чувствительных к нему биологических системах in vitro и in vivo. Несмотря на внедрение в вирусологических лабораториях многих современных методов изучения биологической активности вируса и процессов его взаимодействия с антителами, реакция нейтрализации остается одним из основных серологических тестов. Она позволяет идентифицировать, а затем определить типовую принадлежность выделенного вируса. Результаты реакции нейтрализации становятся очевидными после того, как смесь вируса с гомологичными ему антителами после определенной по времени экспозиции будет внесен в чувствительную биологическую систему (тканевая культура клеток, куриный эмбрион, организм восприимчивого животного), где вирус может размножаться и вызывать поддающиеся учету изменения и которые будут подавлены частично или полностью в присутствии антител. В диагностике вирусных респираторных инфекций крупного рогатого скота реакция нейтрализации нашла широкое распространение и до сих пор остается классическим методом как для идентификации выделенных вирусов, так и для обнаружения вируснейтрализующих антител. Для постановки реакции нейтрализации при диагностике пневмоэнтеритов телят в качестве биологических объектов используют те же культуры клеток, что и для выделения вирусов. Реакцию нетрализации для идентификации вирусов ставят с заранее известными противирусными сыворотками, а для выявления антител в биологическом материале - с заранее известными вирусами. Постановка реакции нейтрализации при идентификации вируса инфекционного ринотрахеита крупного рогатого скота требует наличия: -специфической сыворотки против инфекционного ринотрахеита; -вируссодержащего испытуемого материала, свободного от микробов; - культуры клеток ПЭК, ПТ, ТБ или МДБК; - контрольной отрицательной сыворотки; -питательной вирусологической среды и вспомогательных растворов. Перед постановкой реакции сыворотки разводят питательной средой до 1:10 и инактивируют в течение 30 мин. при температуре 56°С. Все манипуляции осуществляют в строго стерильных условиях. В первый ряд стерильных пробирок (7 шт) вносят по 2 мл специфической сыворотки, во второй ряд - по 2 мл отрицательной. После приготовления десятикратных разведений вируссодержащего материала (конечное разведение 10-7) с использованием питательной среды вносят по 2 мл каждого разведения в два ряда с сыворотками. Пробирки тщательно встряхивают и выдерживают при 37°С в течение двух часов. Затем из каждой пробирки со смесью вируса и сыворотки по 1 мл переносят в 4 пробирки с культурой клеток и после адсорбции вируса на клеточном монослое инкубируют их при 37°С, ежедневно просматривают на наличие ЦПД. Окончательный учет результатов реакции осуществляют на 5—7 день. Видовую принадлежность вируса и его титр определяют по разности показателей между отрицательной и положительной сыворотками. Разница должна быть не менее чем на 2 lg. · Реакция иммобилизации (РИ) Способность иммунной сыворотки вызывать иммобилизацию подвижных микроорганизмов связана со специфическими антителами, которые проявляют свое действие в присутствии комплемента. Иммобилизирующие антитела обнаружены при сифилисе, холере и некоторых других инфекционных заболеваниях. Это послужило основанием для разработки реакции иммобилизации трепонем, которая по своей чувствительности и специфичности превосходит другие серологические реакции, используемые при лабораторной диагностике сифилиса. Реакции иммобилизации Реакции иммобилизации основаны на способности специфических AT, циркулирующих в сыворотке больных, подавлять (нейтрализовать) подвижность различных микроорганизмов. На практике применение нашли реакции иммобилизации бледной трепонемы и холерного вибриона. · Реакция клеточной цитотоксичности. При совместном культивировании лимфоцитов реципиента (отвечающих клеток) и отличающихся от них по антигенам HLA класса II стимулирующих клеток среди отвечающих клеток появляются цитотоксические T-лимфоциты. Они способны разрушать клетки-мишени, несущие антигены, которые присутствуют на стимулирующих клетках. Изучение клеточной цитотоксичности в смешанной культуре лимфоцитов в ряде случаев позволяет предсказать, будет трансплантат стимулировать образование цитотоксических T-лимфоцитов или нет. Для этого готовится смешанная культура лимфоцитов, где отвечающими клетками служат лимфоциты реципиента, а стимулирующими - инактивированные лимфоциты донора. После 6 сут инкубации в смешанной культуре лимфоцитов к отвечающим клеткам добавляют свежие клетки того же донора, меченные 51Cr. Клетки реципиента и меченые клетки донора смешиваются в соотношениях 100:1, 50:1 и 10:1. После инкубации в течение 4 ч отбирают надосадочную жидкость и измеряют содержание в ней радиоактивной метки, вышедшей из разрушенных клеток донора. Отрицательным контролем служат меченые клетки донора. Метод можно использовать как до, так и после трансплантации. В последнем случае повышение активности цитотоксических T-лимфоцитов свидетельствует об отторжении трансплантата. Иммуноферментный анализ (ИФА) Иммуноферментный анализ (ИФА) проводят в два этапа: первый — взаимодействие антител с антигеном, второй — ферментативная индикация комплекса антиген — антитело за счет появления окрашивания реакционной смеси и регистрации окрашивания визуально либо спектрофотометрическим методом. Существуют два варианта ИФА: твердофазный и жидко-фазный, различающиеся по способу разделения компонентов иммунохимической реакции. По сравнению с описанными ранее методами выявления антигенов и антител ИФА обладает существенными преимуществами: — высокой чувствительностью, позволяющей определять до 0,05 нг/мл вещества; — возможностью использования минимальных объемов исследуемого материала (1—2 мкл); — возможностью инструментального или визуального учета реакции; — экспрессностью и возможностью автоматизации всех этапов реакции. ИФА в настоящее время широко используют в практике для диагностики многих инфекционных болезней бактериальной, гр
|
||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 509; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.208.189 (0.012 с.) |






















 Основными формами иммунного ответа на попадание антигена в организм являются: биосинтез антител, образование клеток иммунной памяти, реакция гиперчувствительности немедленного типа, реакция гиперчувствительности замедленного типа, иммунологическая толерантность, идиотип- антиидиотипические отношения.
Основными формами иммунного ответа на попадание антигена в организм являются: биосинтез антител, образование клеток иммунной памяти, реакция гиперчувствительности немедленного типа, реакция гиперчувствительности замедленного типа, иммунологическая толерантность, идиотип- антиидиотипические отношения.


