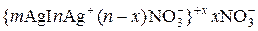Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение мицеллы гидрофобного золяСодержание книги
Поиск на нашем сайте Дисперсная фаза и прилегающий двойной электрический слой составляют мицеллу гидрофобного золя (micella – уменьшительное от лат. mica – крошка, крупица). Основу мицеллы составляет агрегат, состоящий из большого числа частиц нерастворимого в воде вещества и имеющий кристаллическое строение. Комбинация агрегата с потенциалопределяющими ионами – ядро мицеллы. Ядро имеет заряд, знак и величина которого определяются природой и количеством потенциалопределяющих ионов. Вокруг ядра концентрируются противоионы. Ядро совместно с адсорбционным слоем противоионов образует частицу, которая окружена диффузным слоем. Рассмотрим строение мицеллы на примере гидрофобного золя иодида серебра, полученного в результате реакции AgNO3 + KI = AgI + KNO3. При смешении AgNO3 и KI в эквимолярном соотношении AgI выпадает в осадок. Устойчивый золь можно получить при соблюдении двух условий: 1) растворы реагентов должны быть разбавленными; 2) одно из реагирующих веществ берется в избытке; вещество, взятое в избытке, является стабилизатором золя. На рис. 28 представлена схема мицеллы отрицательного золя иодида серебра, стабилизированного KI.
Разумеется, мицелла не имеет строго определенного состава. Тем не менее, ее состав можно представить условной формулой. Для положительного золя иодида серебра формула мицеллы имеет вид
 , ,
где m – количество частиц, входящих в состав агрегата, n – количество потенциалопределяющих ионов, x – количество противоионов в диффузионном слое. Число противоионов, входящих в адсорбционный слой, определяется из условия электронейтральности мицеллы.
Факторы, влияющие на электрокинетический потенциал Электрокинетический потенциал – важнейшая характеристика ДЭС: он определяет возможность и скорость относительного перемещения дисперсной фазы и дисперсионной среды, интенсивность электрокинетических явлений, устойчивость золей. Поэтому весьма важно рассмотреть влияние на него различных факторов. Величина z-потенциала зависит от величины j0-потенциала (поскольку z-потенциал – часть поверхностного потенциала) и толщины ДЭС: чем выше j0-потенциал и шире ДЭС (чем больше противоионов сконцентрировано в диффузионной части), тем больше z-потенциал. На величину z-потенциала влияют: – температура; – добавки электролитов; – рН среды; – природа дисперсионной среды. Влияние температуры С ростом температуры, с одной стороны, усиливается диффузия противоионов, ДЭС расширяется, z-потенциал по абсолютному значению возрастает; с другой стороны – усиливается десорбция потенциалопределяющих ионов, j0-потенциал уменьшается, а, следовательно, уменьшается и Влияние электролитов По характеру воздействия на потенциал ядра (j0-потенциал) электролиты подразделяют на индифферентные и неиндифферентные. Индифферентные (безразличные) электролиты не имеют ионов, способных достраивать кристаллическую решетку коллоидной частицы. Поэтому такие электролиты не могут сколько-нибудь существенно изменить потенциал ядра коллоидной частицы (j0-потенциал). Электролиты, добавление которых к золю, вызывает изменение потенциала ядра, называются неиндифферентными. Один из ионов неиндифферентных электролитов (неиндифферентный ион) способен достраивать кристаллическую решетку коллоидной частицы. Это ион либо входит в состав кристаллической решетки агрегата, либо образует малорастворимое соединение с потенциалопределяющим ионом. Например, для положительного золя AgI
индифферентными электролитами являются KNO3, NaNO2, неиндифферентными – NaCl, KI, AgNO3.
|
||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 1669; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.41 (0.009 с.) |

 Агрегат мицеллы образуют кристаллики AgI размером 10-9-10-7 м. Потенциалопределяющими ионами являются ионы I–, противоионами – ионы K+. Если в избытке берется AgNO3, получается положительный золь, в котором потенциалопределяющими ионами являются ионы Ag+, противоионами – NO3-.
Агрегат мицеллы образуют кристаллики AgI размером 10-9-10-7 м. Потенциалопределяющими ионами являются ионы I–, противоионами – ионы K+. Если в избытке берется AgNO3, получается положительный золь, в котором потенциалопределяющими ионами являются ионы Ag+, противоионами – NO3-.