
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дефекты в диоксиде кремния, отвечающие за накопление зарядаСодержание книги
Поиск на нашем сайте
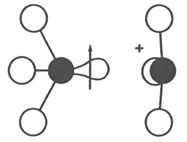
Основную роль в накоплении заряда в диоксиде кремния играют точечные парамагнитные дефекты, которые обычно связываются с наличием оборванных связей в структуре Si/SiO2 [8, 15–17]. Из них наиболее важными с точки зрения накопления заряда в диэлектрике являются Е’-центры. Как правило, E’-центры являются донороподобными центрами, которые могут находиться в нейтральном состоянии или быть положительно заряженными. Большинство E’-центров характеризуются неспаренным электроном, локализованным на атоме кремния, связанном с тремя атомами кислорода. Химическое обозначение для В настоящее время выделяют порядка 10 видов E’-центров, которые различаются по наличию или отсутствию дополнительных комплексов +SiºO3 или по наличию дополнительных атомов, главным образом О или Н. Ниже рассмотрены некоторые наиболее распространенные виды данных дефектов. E’s-центр представляет собой соединение типа ·SiºO3 [16]. Этот дефект может быть нейтральным или перейти в положительно заряженное состояние при потере электрона, превращаясь в +SiºO3. При подаче на структуру Si/SiO2 отрицательного смещения электроны могут туннелировать с нейтральных образований ·SiºO3 в валентную зону кремния, что приводит к образованию нестабильных растянутых положительно заряженных комплексов +SiºO3. Экспериментально было обнаружено [16], что для этого требуется энергия, соответствующая уровню дефекта, отстоящему от дна зоны проводимости SiO2 на 5 эВ. После потери электрона дефект переходит в свою наиболее энергетически выгодную приблизительно плоскую конфигурацию. При этом он отдает решетке часть энергии. В результате энергетический уровень дефекта занимает в запрещенной зоне SiO2 положение Ec – 4,5 эВ. Для разрядки дефекта необходимо подать смещение противоположного знака такое, чтобы совместить потолок валентной зоны кремния с уровнем дефекта. После разрядки нейтральный центр вновь перейдет в наиболее энергетически выгодную выпуклую форму, вновь отдавая решетке часть энергии. Одним из наиболее распространенных видов E’-центра, структура которого известна наиболее достоверно, является E’g-центр, представляющий собой соединение, состоящее из двух комплексов O3ºSi· +SiºO3. Наличие этих дефектов обусловлено тем, что в оксидах с избыточным содержанием кремния изначально содержатся нестехеометрические структуры O3ºSi–SiºO3, являющиеся предшественниками E’g-центров. При захвате дырки на вакантное место одного из атомов кремния центр становится парамагнитным и положительно заряженным. На рис. 3.2 схематично изображен предшественник E’g-центра и его ЭПР-активное состояние [13]. В термических оксидах предшествующие состояния присутствуют до облучения. Обычно в наибольшей концентрации они наблюдаются вблизи границы Si/SiO2 вследствие несоответствия решеток кремниевой подложки и оксида или вследствие диффузии кислорода из оксида в кремний.
Рис. 3.2. Схематическое изображение предшественника (а) и ЭПР-активного состояния (б) E’g-центра [13] Энергетические уровни E’g-центров практически совпадают с уровнями E’s-центров, несмотря на то, что E’s-центр в состоянии с наименьшей энергией имеет оборванную орбиталь, а E’g-центр разорван поперек связи Si–Si [16]. Связи Si–Si, являющиеся предшественниками для E’g-центров, могут образовываться вследствие различных причин. Если вакансия кислорода образовалась в результате смещения или ионизации в SiO2, то расстояние между атомами кремния в связи Si–Si будет составлять 0,31 нм [16]. Если же вакансия является результатом недостатка кислорода в процессе получения SiO2 или избытка кремния (например, вследствие имплантации его в SiO2), то расстояние Si–Si будет составлять 0,25 нм. С ростом расстояния уменьшается прочность связи. В результате энергетические уровни дефектов занимают в запрещенной зоне SiO2 различные положения: Ec – 5,9 эВ для «длинной» связи и Ec – 7,7 эВ для «короткой». При этом данные дефекты будут различаться по способности перезаряжаться. Три других типа E’-центров, которые определены в облученных термических оксидах, это E’d-центры, а также диполи E’74-G и E’10.4-G [13]. E’d-центр скорее всего является результатом захвата дырки комплексом междуузельный кремний / кислородная вакансия. Также как и E’g, E’d-центр имеет положительное парамагнитное зарядовое состояние. Диполи E’74-G и E’10.4-G — это E’-центры, связанные с водородом [13]. Структура диполя E’74-G была определена как неспаренный спин атома кремния, связанного с двумя атомами кислорода и одним атомом водорода. Химическая формула для него записывается в виде H–Si=O2· +SiºO3. Он имеет положительно заряженное парамагнитное состояние. Чтобы наблюдались диполи E’74-G необходимо облучать термические оксиды до очень больших уровней (~ 108 рад) или обрабатывать их водородом после облучения. Структура диполей E’10.4-G до сих пор остается не ясной. Их предшественником считается атом кремния с оборванной орбиталью, связанный с двумя атомами кислорода и одной гидроксильной группой [13]. Впервые корреляция между количеством E’-центров и величиной радиационно-индуцированного положительного заряда (заряда, накопленного в оксиде) для некоторых термических оксидов была показана Ленаханом и Дрессендорфером. Ими была проведена серия экспериментов по измерению ЭПР-спектров, вольт-фарадных характеристик (ВФХ) МОП-структур, с использованием термического отжига и стравливания. При этом они наблюдали корреляцию приблизительно один к одному между положительным зарядом и числом E‘-центров как при облучении, так и при отжиге. Данная корреляция в зависимости от дозы изображена на рис. 3.3 [13].
Рис. 3.3. Рост числа E’-центров и захваченного оксидом заряда (аппроксимируется выражением D VmgCox / q) по мере накопления дозы [13]:? — концентрация E’-центров; p — величина D VmgCox / q Здесь показаны дозовые зависимости количества E’-центров, приходящегося на единицу площади затвора, измеренного с помощью ЭПР, и величины D VmgCox / q, измеренной на МОП-конденсаторах (D Vmg — сдвиг напряжения середины зоны; Cox — емкость оксида; q — заряд электрона). В предположении, что при напряжении середины зоны заряд поверхностных ловушек нейтрален, а накопленный оксидом заряд локализован очень близко к границе Si/SiO2, величина D VmgCox / q приблизительно равна поверхностной концентрации заряженных центров, определяющих накопленный в оксиде заряд. Из рис. 3.3 видно, что между увеличением по мере накопления дозы количества E’-центров и концентрацией накопленного заряда наблюдается корреляция практически один к одному. С помощью экспериментов по стравливанию было обнаружено, что пространственные распределения в оксиде числа E’-центров и накопленного заряда практически совпадают. Было определено, что большая часть E’-центров и накопленного в оксиде заряда локализована вблизи границы Si/SiO2 (в пределах 10 нм для 1100-нанометрового толстого оксида). Дополнительные исследования показали, что путем селективного введения в оксид электронов и дырок с помощью ультрафиолетового облучения можно изменить знак заряда E’-центра (а также положительного накопленного заряда в оксиде). Следует отметить, что корреляция между числом E’-центров и накопленным зарядом наблюдается не во всех оксидах. В последних исследованиях толстых захороненных оксидов КНИ-структур и термически выращенных подзатворных оксидов возник ряд вопросов по поводу общей корреляции между числом E’-центров и зарядом, накопленным в оксиде. Работы, выполненные на SIMOX, BESOI и термически выращенных оксидах [13], показали отсутствие корреляции между числом E’-центров и накопленным в оксиде зарядом. Из встроенных оксидов это особенно сбивает с толку в случае BESOI-материалов, которые представляют два «склеенных» термически выращенных оксида. Следовало ожидать, что в BESOI-материалах будут наблюдаться те же спектроскопические свойства, что и в стандартных термически выращенных подзатворных оксидах, за исключением области вблизи границы склеивания. 3.1.2 Особенности строения границы раздела Si/SiO2 Структура границы раздела Схематично строение границы раздела Si/SiO2 представлено на рис. 3.4. По мере приближения со стороны кремния к границе раздела Si/SiO2 кристаллическая структура нарушается, и вблизи границы раздела она может сильно отличаться от объемной: в пределах нескольких атомных слоев образуется слой разупорядоченного кремния. Этот слой является структурно неоднородным: в верхней части он аморфизирован, ниже — поликристаллический, далее приближается к монокристаллическому. В результате область приграничного кремния будет характеризоваться большими механическими напряжениями и высокой концентрацией активных центров [8, 15–17]. Наличие разупорядоченного слоя кремния обусловлено процессом окисления. Разрыв связей Si–Si и образование более прочных связей
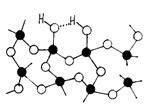
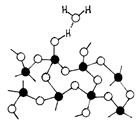
Рис. 3.4. Схематическое изображение строения границы раздела Si/SiO2 [17] Далее следует переходная область SiO x, в которой свойства меняются от присущих кремнию до присущих диоксиду кремния. В [17] указывается, что состав этой области может меняться по схеме Si – Si2O – Si2O3 – SiO2. Изменение стехиометрии здесь обусловлено или недостатком кислорода, или избытком кремния. От свойств этой области во многом будут зависеть электрофизические параметры МОП-приборов, так как здесь могут накапливаться электрически активные дефекты. Толщина этой области сравнительно небольшая, порядка 0,2–0,3 нм [16] (хотя в некоторых работах указывается, что она может доходить до нескольких нанометров), и она содержит порядка 1015 см–2 атомов кремния, связанных в конфигурациях SiO x. Область приграничного Si также характеризуется большими механическими напряжениями и высокой концентрацией электрически активных дефектов. В результате большая часть встроенного положительного заряда, который образуется в SiO2 при окислении и при облучении, сосредоточена именно в этой области [15]. Граница области с переходным слоем условно проводится на таком расстоянии от полупроводника, что обменом носителями заряда с кремнием посредством туннелирования можно пренебречь. Объем SiO2 характеризуется свойствами, описанными выше (см. п. 3.1.1), однако в МОП-структурах вблизи границы с электродом затвора структура диоксида кремния может отличаться от объемной. Химический состав SiO2 в этой области постоянен, концентрация дефектов максимальна вблизи области приграничного SiO2, а энергетические уровни электрически активных центров дискретны [15]. Дефекты на границе раздела Si/SiO2, отвечающие за накопление заряда Заряд, накопленный на границе раздела кремний-диэлектрик принято характеризовать плотностью поверхностных состояний (ПС). Основным видом точечных электрически активных дефектов на границе раздела Si/SiO2, отвечающих за величину плотности ПС, является Pb-центр [8, 13, 16], который может быть представлен как атом кремния на границе, связанный с тремя другими атомами кремния и имеющий одну оборванную связь. Химическое обозначение Pb-центра записывается в виде ·SiºSi3. На поверхности кремния (111) оборванная связь ориентирована перпендикулярно границе (Pb-центры с оборванными связями, ориентированными под другими углами были обнаружены только на специально изготовленных образцах). Кроме того, Pb-центр располагается в пределах одного атомного слоя от границы в сторону Si или SiO2. На поверхности (110) оборванные связи Pb-центра ориентированы вдоль двух тетраэдрических направлений [111], причем оборванных связей, лежащих в плоскости границы, обнаружено не было [16]. Наиболее сложную структуру Pb-центры имеют на поверхности кремния (100). Здесь было идентифицировано два различных типа Pb-центров, каждый из которых может иметь оборванные связи, ориентированные в двух направлениях. Первый вид — Pb0-центр, представляющий собой соединение ·SiºSi3, оборванная связь которого может быть ориентировано вдоль двух направлений [111]. Второй вид — Pb1-центр, представляющий собой частично окисленное соединение ·SiºSi2O с оборванной связью, ориентированной в тех же направлениях [16]. Во многих работах указывается, что величина плотности ПС, определенная, например, по результатам измерения ВФХ, коррелирует с плотностью Pb-центров в пределах погрешности, равной коэффициенту 2. Остальные ловушки, возможно, представляют собой напряженные связи, углы и длины которых немного отличаются от присущих неповрежденному кремнию, что приводит к разбросу по энергии. Но в отличие от этих ловушек, Pb-центры наблюдались даже в образцах с очень низкой плотностью ПС [16]. Обычно энергетическое распределение Pb-центров имеет пик в середине запрещенной зоны и спадает по мере приближения к зоне проводимости или валентной зоне [13]. Это распределение согласуется с предположением о том, что в середине запрещенной зоны ПС парамагнитны или нейтральны. В верхней части запрещенной зоны ПС акцептороподобны (могут принять электроны), отрицательно заряжены, содержат два электрона, и Pb-центры — диамагнитные. В нижней части запрещенной зоны ПС донороподобны (могут отдавать электроны), положительно заряжены, не содержат электронов и диамагнитны. В середине зоны ПС нейтральны, содержат один электрон и парамагнитны. Следует, однако, отметить, что далеко не всегда пик распределения плотности Pb-центров приходится на середину запрещенной зоны кремния. В частности в [16] указывается, что максимальная плотность приходится на энергетические уровни Ev + 0,38 эВ и Ev + 0,8 эВ. Расчеты, проведенные с помощью метода молекулярных орбиталей, показали, что 3.1.3 Влияние водорода и водородсодержащих соединений на свойства структуры Si/SiO2 Водород, протоны и соединения ОН (гидроксильные группы) оказывают значительное влияние на свойства структуры Si/SiO2 [8, 16]. В термически выращенном диоксиде кремния, даже в случае окисления в сухом кислороде, всегда содержится водород в достаточно больших количествах (концентрация водорода может доходить до 1018 см–3). Водород попадает в SiO2 или непосредственно из среды, в которой проводится окисление, или за счет диффузии из кремниевой подложки [15]. Большая часть водорода и гидроксильных групп в термическом диоксиде кремния находится в связанном состоянии в виде соединений типа O3ºSi–OH или O3ºSi–H. Если два соединения O3ºSi–OH находятся рядом, то образуется так называемая молекула «химически сорбированной» воды [16]. При нагреве от 100 до 500 С молекула химически сорбированной воды высвобождается, а остаточный атом кислорода своей оборванной связью соединяется с атомом кремния, от которого оторвалась группа ОН. В результате образуется свободная молекула воды и соединение типа O2=Si=O2=Si=O2. Если в диоксиде кремния имеется избыточная молекулярная вода, то она может присоединиться к изолированным или смежным соединениям O3ºSi–OH, образуя так называемую «физически сорбированную» воду [16]. Такая вода легко высвобождается при температуре порядка 100 °С. Кроме того, в [16] указывается, что второй ряд молекул H2O, адсорбированный на первый физически сорбированный ряд, имеет большую энергию связи. Таким образом, возможно образование кластеров из молекул воды. Образование и высвобождение молекул химически и физически сорбированной воды проиллюстрировано на рис. 3.5 [16].
Рис. 3.5. Водородные примеси в аморфном диоксиде кремния: а — молекула физически сорбированной воды, присоединенная к двум смежным соединениям ºSi–OH; б — молекула химически сорбированной воды; в — высвобождение молекулы химически сорбированной воды с образованием соединения Si=O2=Si; г — молекула физически сорбированной воды, присоединенная к изолированному соединению ºSi–OH;? — атом Si; š — атом О Изолированные соединения O3ºSi–OH устойчивы при температурах вплоть до 1200 К, а при больших температурах они распадаются с образованием атомарного водорода: O3ºSi–OH ® O3ºSi–O· + Н. (3.1) В качестве механизма диффузии можно предложить следующий [16]. Свободная молекула воды вступает в реакцию H2O + ºSi–O–Siº ® ºSi–OH…HO–Siº (3.2) с образованием химически сорбированной воды. Далее миграция воды происходит посредством последовательных перескоков фрагментов соединений O3ºSi–OH. Коэффициент
Данный механизм хорошо подходит для описания высокотемпературной диффузии молекул воды в тонких пленках термического SiO2. Однако даже при температуре менее 100 °С вода достаточно хорошо проникает в тонкие пленки диоксида кремния. Например, водяной пар при температуре 60 °С всего за 10 мин образует в оксиде толщиной 90 нм вблизи границы Si/SiO2 обогащенную водородом область толщиной порядка 10 нм с поверхностной плотностью водорода порядка 3×1012 см–2 [16]. Исследования диффузии воды при таких температурах показали, что энергия активации этого процесса составляет порядка 0,3 эВ. Столь малое значение энергии активации говорит о том, что механизм диффузии воды отличен от описанного выше. Возможно, здесь оказывают влияние имеющиеся в оксиде микропоры, по которым диффундирующие соединения могут быстро проникать на достаточную глубину. В ряде исследований было обнаружено, что при нагреве структуры Si/SiO2 до температуры порядка 300–400 °С и/или подаче отрицательного электрического поля напряженностью порядка нескольких мегавольт на сантиметр происходит увеличение плотности ПС и фиксированного заряда в оксиде. Данное явление приписывается влиянию водородных соединений [16]. Считается, что присутствующие в оксиде соединения ºSi–H вступают в реакцию с водородными соединениями и дырками с образованием Pb-центров или E’-центров, т.е. идет реакция ºSi–H + A + h + ® ºSi· + AH+, (3.4) где А — это некоторое водородное соединение, а h + — дырка. При подаче отрицательного электрического поля дырки будут стягиваться к границе раздела Si/SiO2, а поскольку там сосредоточена большая часть всех дефектов, в том числе и соединений ºSi–H, то протекание реакции (3.4) будет облегчаться. Для скорости реакции (3.4) можно записать выражение d [AH+]/ dt = d [ºSi·]/ dt = kf [ºSiH][A][ h +] – kr [ºSi·][AH+], (3.5) где kf и kr — константы скоростей прямой и обратной реакций соответственно, которые увеличиваются с температурой по закону Аррениуса. Чаще всего в роли соединения А выступает Н2О. В этом случае обратной реакцией можно пренебречь [16]. Тогда реакция (4.4) запишется в виде ºSi–H + H2O + h + ® ºSi· + H3O+. (3.6) Механизм генерации заряда вблизи границы Si/SiO2 под действием молекул воды можно описать следующим образом [16]. Молекула Н2О располагается вблизи соединения ºSi–H. Под действием электрического поля она ориентируется атомом кислорода к атому водорода данного соединения. Этот атом водорода захватывается молекулой воды с образованием соединения Н3О+, которое удаляется от границы электрическим полем, а на границе остается электрически активный центр ºSi·. Таким образом, происходит рост плотности ПС и заряда диэлектрика.
|
||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-27; просмотров: 1340; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.198.181 (0.011 с.) |






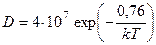 . (3.3)
. (3.3)


