
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 2. Определение глюкозы по методу Вильштеттера и Шудля
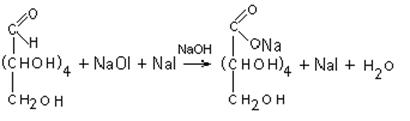
В основе этого метода лежит способность молекулярного йода в щелочной среде окислять только альдегидоспирты, не влияя на кетоспирты. Реакция идет в 2 стадии:
2 NaOH + I2 → NaOI + NaI + H2O При внесении излишка йода непрореагировавший йод можно определить в кислой среде титрованием тиосульфатом натрия: NaOI + NaI + 2HCl → I2 + 2NaCl + H2O I2 + 2Na2S2O3 → 2NaI + Na2S4O6 Приборы и реактивы: конические колбы на 100 мл; бюретка для титрования; 0,1м раствор йода; 0,1 м раствор гидроксида натрия; 0,1 м раствор серной кислоты; 0,1 м раствор тиосульфата натрия; 1 % раствор крахмала.
Методика выполнения работы В 2 колбы на 100 мл внести по 10 мл раствора йода. В одну из колб (опытный вариант) добавить 20 мл экстракта, приготовленного в опыте 2.3.1.1, в другую колбу (контрольный вариант) прилить 20 мл дистиллированной воды. Затем медленно добавить 15 мл раствора гидроксида натрия и оставить стоять при комнатной температуре 15 минут. После этого раствор подкислить 20 мл раствора серной кислоты и остаток йода оттитровать раствором тиосульфата натрия в присутствии растворимого крахмала (3 капли). Массовую концентрацию глюкозы в растительном сырье (г, %) рассчитать по формуле: Г =
Оформление результатов опыта Полученные результаты записывают в таблицу 7.
Таблица 7.
Опыт 3. Определение сахарозы Приборы и реактивы: мерная колба на 100 мл; мерный цилиндр; 5 % раствор соляной кислоты; 0,1 н раствор гидроксида натрия. Методика выполнения работы Отобрать 50 мл экстракта пипеткой в мерную колбу на 100 мл, добавить 5 мл раствора соляной кислоты, поместить в кипящую водяную баню на 30 минут для инверсии сахарозы. Затем колбу охладить, добавить до метки раствор гидроксида натрия, перемешать и в 10 мл гидролизата определить редуцирующие сахара по Иссекутцу. Массовую долю сахарозы (С, %) в растительном сырье найти по формуле: С = (х – Рв) 0,95, где х, Рв – массовая доля редуцирующих сахаров в экстракте после и до инверсии, %;
0,95 – коэффициент пересчета редуцирующих веществ на сахарозу. Пример расчета. При определении Рв в экстракте методом Иссекутца на титрование контроля и опыта пошло соответственно 9,5 и 3,4 мл тиосульфата. Остаток не вошедшего в реакцию с сахарами железосинеродистого калия определяют по пропорции: 10:9,5 = х:3,4 х = 3,58 мл Объем К3Fe(СN)6, пошедший на реакцию с редуцирующими сахарами, составляет 10 – 3,58 = 6,42 мл По таблице 7 находят количество редуцирующих сахаров: 6,40 мл – 10,41 мг 0,02 мл – 0,03 мг 6,42 мл – 10,44 мг Рв Тогда массовая доля Рв в растительном сырье составит: Рв = По методу Вильштеттера и Шудля на титрование контроля и опыта пошло соответственно 10,0 и 8,0 мл тиосульфата натрия. Вычисляем массовую долю глюкозы в растительном материале по формуле: Г = Массовая доля фруктозы (Ф, %) в растительном сырье равна: Ф = Рв – Г В нашем примере это составит: Ф = 10,44 – 4,5 = 5,94 % Для определения количества редуцирующих сахаров в экстракте после инверсии известно, что на титрование контроля и опыта пошло соответственно 9,5 и 2,8 мл. Остаток железосинеродистого калия составляет х = 2,94 мл; пошедшего на реакцию с сахарами: 10 – 2,94 = 7,06 мл По таблице 7 находим количество редуцирующих сахаров – 11,57 мг. Следовательно, массовая доля их в экстракте после инверсии составляет: х = Массовая доля сахарозы в растительном сырье равна: С = (11,57 – 10,44) 0,95=1,07 % Оформление результатов опыта Полученные результаты записывают в таблицу 8. Таблица 8
2.4 Контрольные вопросы 1. Какие сахара называют редуцирующими? 2. На чем основан метод Иссекутца? Какие сахара можно определить этим методом? 3. Каким методом можно определить глюкозу в присутствии других сахаров? 4. Почему для определения сахарозы проводят инверсию? 5. Что такое инверсия сахарозы? Как проводят инверсию сахарозы? 6. Расскажите схему дифференцируемого определения сахаров в растительном сырье. 7. Отличается ли содержание редуцирующих сахаров в сырье и готовом продукте? Чем объяснить различие?
Литература [1, с.255-281]; [2]
|
||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 482; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.140.108 (0.007 с.) |
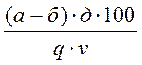 ,
, - объемы раствора тиосульфата натрия, пошедшие на титрование, соответственно контроля и опыта, мл;
- объемы раствора тиосульфата натрия, пошедшие на титрование, соответственно контроля и опыта, мл;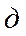 - масса глюкозы, мг, эквивалентная 1 мл раствора йода;
- масса глюкозы, мг, эквивалентная 1 мл раствора йода;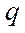 - навеска сырья (мг) в 1 мл экстракта;
- навеска сырья (мг) в 1 мл экстракта; - объем экстракта, взятый для определения, мл.
- объем экстракта, взятый для определения, мл. , мл
, мл
 , мл
, мл
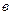 , мл
, мл
 ,
,




