
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Внутренняя энергия. Первый закон термодинамики. Применение первого закона к изопроцессам. Адиабатный процесс.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Каждое тело имеет вполне определенную структуру, оно состоит из частиц, которые хаотически движутся и взаимодействуют друг с другом, поэтому любое тело обладает внутренней энергией. Внутренняя энергия — это величина, характеризующая собственное состояние тела, т. е. энергия беспорядочного хаотического движения микрочастиц системы (молекул, атомов, электронов и т. д.) и энергия взаимодействия этих частиц. Внутренняя энергия одноатомного идеального газа определяется по формуле Внутренняя энергия тела может изменяться только в результате его взаимодействия с другими телами. Существует два способа изменения внутренней энергии: теплопередача и совершение механической работы (например, нагревание при трении или при сжатии, охлаждение при расширении). Закон сохранения и превращения энергии, распространенный на тепловые явления, называется первым законом термодинамики, который формулируется так: изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме количества теплоты, переданного системе, и работы внешних сил, совершенной над системой: Если система сама совершает работу, то ее условно обозначают При изобарном нагревании газ совершает работу над внешними силами
Применение первого закона термодинамики к изопроцессам, происходящим с идеальным газом:
Адиабатным называют процесс, протекающий без теплообмена с окружающей средой, т.е. процесс в теплоизолированной системе. При адиабатном процессе Q = 0, следовательно, изменение внутренней энергии происходит только за счет совершения работы:
|
||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 1938; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.006 с.) |

 , двухатомного газа -
, двухатомного газа - 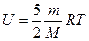 .
.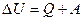 , где
, где  - изменение внутренней энергии, Q — количество теплоты, переданное системе, А — работа внешних сил.
- изменение внутренней энергии, Q — количество теплоты, переданное системе, А — работа внешних сил.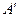 . Тогда первый закон термодинамики можно записать так:
. Тогда первый закон термодинамики можно записать так:  , т.е. количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии.
, т.е. количество теплоты, переданное системе, идет на совершение системой работы и изменение ее внутренней энергии. , где V1 и V2 — начальный и конечный объемы газа.
, где V1 и V2 — начальный и конечный объемы газа.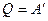 , т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.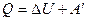 .
. , т. е. переданное количество теплоты идет на увеличение внутренней энергии газа.
, т. е. переданное количество теплоты идет на увеличение внутренней энергии газа.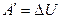 .
.


