
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: Строение и структура биополимеров.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Первый Московский Государственный Медицинский Университет им. И. М. Сеченова Лечебный факультет Кафедра общей химии
ЛАБОРАТОРНАЯ ТЕТРАДЬ ПО КУРСУ ХИМИИ БИОПОЛИМЕРОВ
СТУДЕНТА __________ ГРУППЫ
______________________ФАКУЛЬТЕТА
__________________________________ОТДЕЛЕНИЯ
__________________________________________________
__________________________________________________
Учебный год
Настоящая лабораторная тетрадь по курсу химии биополимеров предназначена для самостоятельной работы студентов лечебного и педиатрического факультетов, выполняющих практические \и теоретические задания на лабораторных занятиях. Темы занятий включают лабораторные работы, выполнение и оформление которых студенты проводят самостоятельно. Это дает возможность студентам закрепить пройденный материал и подготовиться к беседе с преподавателем, который должен оценить правильность полученных результатов и выводов. Данная лабораторная тетрадь соответствует учебному плану и включает материал интегрированного курса химии в соответствии с программой лечебного и педиатрического факультетов.
© ММА им. И. М. Сеченова
© Н. В. Головина, Д. А. Доброхотов, А. А. Лузин
Под редакцией академика РАО, профессора В. А. Попкова
Москва, 2012.
Тема: Строение и структура биополимеров. Способы получения, специфические свойства (семинар). Дата:_________ Занятие № 1 Классификация биополимеров (белки, полисахариды, нуклеиновые кислоты). Способы получения (реакции полимеризации и поликонденсации). Структура макромолекул (линейные, плоскостные, пространственные). Специфические свойства: молекулярная масса, асимметричность, гибкость, эластичность. Цель работы: усовершенствовать знания о принципах строения биополимеров и показать влияние состава и химической природы компонентов макромолекул на их физико-химические свойства. Сущность работы: разобрать классификацию биополимеров; на конкретных примерах рассмотреть структуру белков, полисахаридов, нуклеотидов; изучить способы получения биополимеров и их специфические свойства. Задание №1. Заполнить данную таблицу:
Классификация полимеров.
* Биополимеры - это высокомолекулярные вещества, обеспечивающие жизнедеятельность живых систем. Задание № 2. На конкретных примерах приведите способы получения биополимеров: 1. Реакция полимеризации:
2. Реакция поликонденсации: Задание № 3. Приведите структурные формулы фрагментов:
______________________________________ Полипептидной цепи полинуклеотидной цепи ________________________ Гликозидной связи Задание №4 Приведите структурные формулы гетероциклических оснований:
_____________ _____________ __________ Тимина аденина гуанина _______________ _________________ Цитозина урацила Задание № 5. Приведите схематично четыре морфологические организации белковых структур: ______________________ _________________ Первичная структура вторичная Структура _______________________________________ Третичная структура четвертичная Специфические свойства биополимеров: Высокая молекулярная масса- Асимметричное строение- 3. Гибкость – Эластичность - Домашнее задание: 1. Приведите строение любого трипептида и назовите его _________________
2. Приведите строение фрагментов следующих полисахаридов: крахмала, гликогена.
3. Приведите фрагмент полинуклеотида с пуриновым основанием, укажите сложноэфирные и гликозидные связи, назовите его:
4.Охарактеризуйте природу связей между отдельными звеньями в макромолекулах полисахаридов
5. Напишите структуру гексапептида: глицил-тирозил-валил-лизил- треонил- лейцин. Сколько в нем пептидных связей?
Классификация п о ПОЛИНУКЛЕОТИДЫ БЕЛКИ ПОЛИСАХАРИДЫ Составу
Биополимеров Разветвленная няются в одну
Полуацеталей частицу складчат ая Стержнеобразная
Занятие № 2 Целевые задачи: в ре зультате изучения данной темы студенты должны иметь представление: - о биологических функциях полисахаридов и их роли в жизнедеятельности; - об особенностях физмико-химических свойств полисахаридов; - о классификации полисвахаридов. Студенты должны знать: 1. Особенности строения гомополисахаридов: крахмала (амилазы, амилопектина), гликогена, целлюлозы, хитина. 2. Особенности строения гетерополисахаридов: гепарина, гиалуроновой кислоты, агар-агара. 3. Химические свойства полисахаридов, обусловленные их строением. Сущность работы: дать определение полисахаридам, разобрать классификацию полисахаридов, на примерах крахмала и целлюлозы рассмотреть структуру полисахаридов; изучить специфические свойства полисахаридов. Блок информации (по указанию преподавателя): Амилозы амилопектина __________________________ ______________________ Целлюлозы хондроитин-4- Сульфата __________________________ ________________________ Гомополисахаридам ________________________________________________________ Гетерополисахаридам _________________________________________________________ Олигосахаридам Занятие № 2 Блок информации (по указанию преподавателя):
ЛАБОРАТОРНАЯ РАБОТА. Качественные реакции на полисахариды, Гидролиз полисахаридов. Цель работы: изучить основные свойства полисахаридов, обусловленные их строением. Сущность работы: провести реакции, характеризующие свойства крахмала и целлюлозы. Опыт 1. Цветная реакция на крахмал: Характерной реакцией на крахмал служит реакция с раствором йода в йодиде калия (иод - крахмальная реакция). Реактивы: крахмал 1%-ный раствор, раствор Люголя (в 100 мл воды растворено 20 г йодида калия и 10 г йода). Ход работы. В пробирку помещают 1 – 2 мл раствора крахмала, приливают одну каплю раствора Люголя (J2 + КJ); отмечают окраску раствора, затем нагревают и охлаждают.
Опыт 2. Гидролиз крахмала: Реактивы: крахмал (1%-ный раствор), соляная кислота (конц.), раствор Люголя, лакмус, 10%-ный раствор гидроксида натрия, раствор Фелинга. Ход работы: в пробирку наливают 5 мл 1 %-го раствора крахмала и 6 капель концентрированной соляной кислоты. Перемешивают и кипятят на пламени горелки. Через 1-2 мин после кипения берут несколько капель раствора пипеткой и приливают в пробирку, в которой находится 6мл дистиллированной воды, сюда же приливают 2 капли раствора Люголя. Отмечают полученное окрашивание. Пробирку с остатками крахмала кипятят еще 1-2 мин и снова проводят такую же пробу с раствором йода в йодиде калия. Отмечают полученное окрашивание. Затем кипятят еще 4 мин и проводят пробу с реактивом Люголя, после чего должно получиться желтое окрашивание. Это значит, что крахмал расщепился до глюкозы. Гидролизованный раствор крахмала нейтрализуют с поьощью лакмуса раствором гидроксида натрия, добавляют реактив Фелинга и нагревают.
Опыт 3. Гидролиз целлюлозы: Ход работы: в пробирку помещают кусочек ваты, заливают его крепким раствором серной кислоты (72 %-ный). После полного растворения (приблизительно через 15 – 20 мин) раствор осторожно разводят водой в 10 – 15 раз и кипятят. После окончания гидролиза нейтрализуют крепким раствором щелочи до сильно- щелочной реакции (по лакмусу) и по каплям добавляют СuSО4.
Домашнее задание. 1. Напишите структурные фрагменты: ________________________ _____________________ Амилозы амилопектина __________________________ ______________________ Целлюлозы хондроитин-4- Сульфата __________________________ ________________________ Гомополисахаридам ________________________________________________________ Гетерополисахаридам _________________________________________________________ Олигосахаридам Занятие № 3 Блок информации (по указанию преподавателя): ЛАБОРАТОРНАЯ РАБОТА. Качественные реакции на аминокислоты.
Цель работы: изучить основные свойства аминокислот, обусловленные их строением и наличием функциональных групп. Сущность работы: провести опыты, указывающие на различное строение аминокислот. Занятие № 4 Дата: _________ Блок информации (по указанию преподавателя): Лабораторная работа. Качественная реакция на пептидную связь. Количественное определение белка. Цель работы: изучить свойства белков, обусловленные их строением. Сущность работы: провести опыты, подтверждающие наличие пептидной связи, определить содержание белка в исследуемом растворе. Реактивы: растворов яичного белка, 1%-ный раствор сульфата меди(II), 10%-ный раствор щелочи. 1. Биуретовая реакция на пептидную связь:
2. Количественное определение белка в растворе: В основе метода лежит биуретовая реакция! Для построения калибровочного графика из раствора белка с точно известной массовой долей (ω = 1,00%) готовят четыре раствора методом последовательного разведения. В пять пробирок помещают по 1,00 мл растворов белка: в четыре пробирки – растворы для построения калибровочного графика, в пятую пробирку – исследуемый раствор. Содержимое пробирок перемешивают стеклянными палочками и оставляют на 20 минут при комнатной температуре. Измеряют оптическую плотность раствора на спектрофотометре ПЭ – 5300 В. Стандартный раствор готовят смешиванием 1,00 мл дистиллированной воды, 1,00 мл раствора гидроксида натрия и 0,10 мл раствора сульфата меди(II). Длина волны светофильтра – 540 нм. Записывают результаты измерений. !!! (эту часть работы делать не надо, в таблице представлены данные для построения калибровочного графика). В чистую пробирку помещают 2мл исследуемого раствора, добавляют по 2,00 мл раствора гидроксида натрия и 0,20 мл раствора сульфата меди(II). Содержимое пробирок перемешивают стеклянной палочкой и оставляют на 15 минут при комнатной температуре. Измеряют оптическую плотность раствора на спектрофотометре ПЭ – 5300 В. Длина волны светофильтра – 540 нм. Строят калибровочный график D = f (ω, %) (на миллиметровой бумаге) по готовым данным из таблицы и определяют массовую долю белка в исследуемом растворе. Делают вывод о содержание белка в исследуемом растворе.
Калибровочный график D = f (ω, %):
28 Домашнее задание.
1. Приведите фрагменты простых и сложных белков:
__________________________ ____________________________
простой сложный
2. Приведите примеры глобулярных и фибриллярных белков:
_________________________________________________________________________
глобулярные
_______________________________________________________
фибриллярные
3. Какие факторы влияют на денатурацию белка? Какие явления называют необратимой денатурацией?
______________________________________________________________________________
________________________________________________________________________________
_______________________________________________________________________________
__________________________________________________________________________________
4. Приведите две резонансные формы пептидной связи в белках: ____________________ _______________________ Кето-форма енольная форма
5. За счет чего стабилизируются вторичная и третичная структуры белка?
_____________________________________________________________________________________
_____________________________________________________________________________________
_____________________________________________________________________________________
6. Напишите цепь гептапептида, состоящего из последовательности аминокислот: серин, валин, тирозин, глутаминовая кислота, валин, аланин, гистидин. Укажите N- и С- концевые остатки. Назовите данный гептапептид.
_______________________________________________________________________________________
__________________________________________________________________________________________
______________________________________________________________________________________
_________________________________________________________________________________________
«Полинуклеотиды». Семинар. Занятие №5. Целевые задачи: иметь представление: - о биологических функциях полинуклеотидов и их роли в организме; - о физико-химических свойствах полинуклеотидов, обусловленных особенностями их строения. Знать: 5. Химический состав и строение ДНК и РНК.Уровни их структурной организации (первичная и вторичная структуры). 6. Строение нуклеотидов и нуклеозидов. 7. Свойства полинуклеотидов: кислотно-основные, хелатирующую способность, способность к денатурации, жидкокристаллическое состояние нуклеиновых кислот. Блок информации (по указанию преподавателя):
. . Домашнее задание.
1. Приведите фрагменты полинуклеотидной цепи:
__________________________ ____________________________
РНК ДНК
2. Приведите примеры:
________________________ _______________________
Рибонуклеозида (назовите его) дезоксирибонуклеозида (назовите)
3. Напищите формулу аденозинтрифосфата, укажите сложноэфирные и гликозидные связи:
/
__________________________________________________________________
4. Покажите схематично образование водородных связей
в комплементарной паре: цитозин-гуанин.
______________________________________________________-
Рекомендуется сделать домашнее задание на занятии.
Занятие № 7 Лабораторная работа. «Определение молекулярной массы биополимера вискозиметрическим методом». Цель работы: освоить вискозиметрический метод для определения молекулярной массы ВМС. Выполнение эксперимента: Оборудование: вискозиметр ВПЖ-2м, секундомер, цилиндры вместимостью 25, 50 мл. Реактивы: водные растворы крахмала четырех концентраций, дистиллированная вода. Выполнение эксперимента: Для измерения времени истечения жидкости на отводную трубку (6) вискозиметра надевают резиновый шланг. Далее, зажав пальцем колено (5) и перевернув вискозиметр, опускают колено (1) в сосуд с раствором биополимера и засасывают её с помощью груши до отметки М2 резервуара, следя за тем, чтобы в жидкости не образовывалось пузырьков воздуха. В тот момент, когда уровень жидкости достигнет отметки М2 резервуара (3), вискозиметр вынимают из сосуда и быстро переворачивают в нормальное положение. Снимают с внешней стороны конца колена (1) избыток жидкости и надевают на него резиновую трубку. Далее засасывают жидкость в колено (1) примерно до одной трети резервуара (2). Сообщают колено (1) с атмосферой и определяют время опускания мениска жидкости от отметки М1 до отметки М2. (Т)
Рис. Вискозиметр ВПЖ-2м. Вязкость вычисляют по формуле, по среднему (из нескольких измерений) времени истечения жидкости:
где: η – кинетическая вязкость жидкости, мм2/с L – постоянная вискозиметра, мм2/с2 T – время истечения жидкости, с g – ускорение свободного падения, мм/с2 По данным вискозиметрических измерений рассчитывают молярную массу ВМС выразив её из уравнения Штаудингера:
M – молярная масса ВМС, г/моль K – константа, характерная для полимеров одного гомологического ряда (для гомологического ряда полисахаридов К = 6.1х 10-4 ) α – константа, характеризующая гибкость макромолекул и их взаимодействие с молекулами растворителя (α= 0,63)
Расчеты:
M =
Вывод: __________________________________________________________________________
__________________________________________________________________________
__________________________________________________________________________ Домашнее задание. 1. Определите молярную массу рибонуклеазы, если результаты вискозиметрического метода для водных растворов рибонуклеазы следующие: характеристическая вязкость водного раствора полимера = 0,033 м3| кг; К= 5,1х10-5; α = 0,68 2. Рассчитайте удельную и относительную вязкость раствора белка, если время истечения этого раствора равно 600 сек., а время истечения воды – 240 сек. Плотность раствора белка равна 1,008 г/ см 3. 3. Молярная масса биополимера 230000 г/моль. Вычислить характеристическую вязкость раствора биополимера, используя следующие эмпирические констнты: К=1.15 х 10-4; α = 0,72.
4. Относительные вязкости ряда водных растворов биополимера определены вискозиметрическим методом при температуре 298К:
Результаты определения представлены в таблице:
Определите характеристическую вязкость раствора биополимера.
Лабораторная работа. Лабораторная работа. Экспериментальные данные
Вывод: __________________________________________________________________________
____________________________________________________________________________________________________________________________________________________
Занятие № 11 Тема: «Гели. Структурообразование в растворах биополимеров» Целевые задачи: Иметь представление: - о классификации гелей; - о свойствах лиогелей; -о факторах,влияющих на желатинирование. Знать: 16. Определения понятия «гель», «студень». 17. Сущность тиксотропии и синерезиса. 18. Процессы диффузии в гелях. Блок информации (по указанию преподавателя): Лабораторная работа. Цель работы: изучить получение гелей и студней методами желатинирования и набухания, а также процессы диффузии в студнях. Сущность работы: провести опыты, с помощью которых можно получить гели и студни. Опыт 1. Получение геля желатина. Приборы, оборудование: водяная баня, горелка, химический стакан на 250 – 500 мл, стеклянная палочка, штатив с пробирками, мерный цилиндр. Реактивы: желатин сухой, вода. Ход работы: 0,3 г желатина, высыпают в пробирку и заливают 6 мл холодной воды. Выдерживают в течение 20 – 30 мин для набухания желатина, после чего содержимое пробирки осторожно нагревают, непрерывно помешивая стеклянной палочкой до полного растворения желатина. Образуется золь желатина, его наливают в другую пробирку, охлаждают и помещают в стакан с холодной водой или кусочками льда. Описать наблюдения:
_______________________________________________________________
Занятие № 12 (СЕМИНАР) Занятие № 13 Семинар и практическое занятие по теме: «Ферменты. Кинетика ферментативных реакций». Целевые задачи: Иметь представление: - об особенностях каталитической активности ферментов; -о строении и механизме действия ферментов; - о ферментативном катализе; - о коферментной функции витаминов; Знать: 1.Классификацию ферментов. 2.Что такое активный центр фермента. 3.Характеристику аллостерических ферментов. 4.Что такое коферменты и коферментную функцию некоторых витаминов. 5.Уравнение Михаэлиса-Ментен. Его анализ. 6.Ингибирование действия ферментов. Литература: по ферментам: (Пузаков.9.5 – 9.9, стр.193 – 206;Ершов, Попков. 9.8, стр.416 – 421.)
Блок информации (по указанию преподавателя):
.
Домашнее задание. 1. Перечислите особенности действия ферментов по сравнению с обычными катализаторами? Какие условия необходимы для работы фермента?
_____________________________________________________________________________________________
2.Что представляет собой активный центр фермента?
3. Приведите примеры конкурентного и неконкурентного ингибирования.
4.К какому классу (подклассу) относится фермент, если при его действии: а) отщепляется карбоксильная группа; б) переносится аминогруппа; в) разрывается пептидная связь и происходит присоединение воды?
5.Каков характер связи биотина с белком –ферментом?
6.Какие соединения относятся к производным никотинамида? Приведите их структуру.
Занятие № 14 Семинар по теме: «Гормоны и биополимеры важнейших физиологических процессов». Целевые задачи: Иметь представление: - о гормонах, их структуре и физиологической роли; - о биополимерах важнейших физиологических процессов (гемоглобине и его производных, иммуноглобулинах, интерферонах) - о химическом механизме ощущений (вкус, запаха); . Знать: 1. Гормоны – производные аминокислот (адреналин, норадреналин, тироксин), их получение и физиологическую роль. 2.Белковые и пептидные гормоны (тиролиберин, вазопрессин, окситоцин), строение и физиологическая роль. 3. Строение и свойства гемоглобина, метгемоглобина, миоглобина, карбоксигемоглобина. 4. Функции цитохромов. 5. Химическую природу антител и антигенов. (лекция № 13) 6. Химическую при роду нейромедиаторов (эндорфины и энкефалины). (Пузаков стр. 593) 7. Соединения, которые вызывают ощущения кислого, горького, сладкого пряного вкуса. 8. Соединения, которые обладают определенным запахом.
Литература: по гормонам: (Пузаков. 24.3.1. – 24.3.3., стр. 576 – 584) гемоглобин, его производные: (Пузаков. 13.2.2 – 13. 2.3., стр.286-293, Ершов, Попков стр.280-282,199, 356) цитохромы: (Пузаков. Стр. 287, 321. Ершов, Попков.Стр.280)
Блок информации (по указанию преподавателя):
NH2
АСПАРТАМ
.
Домашнее задание. 1. В чем заключается специфика химического действия гормонов, производных аминокислот? _________________________________________________________
_____________________________________________________________
2. Какова особенность строения вазопрессина? В чем его физиологическая роль?
3. 3. Назовите основные группы гормонов в зависимости от химического строения и приведите примеры. 4. ____________________________________________________
4.В чем заключается специфика химического действия гормонов, производных аминокислот? _________________________________________________________
_____________________________________________________________
5. Какова особенность строения вазопрессина? В чем его физиологическая роль?
6. 6. Назовите основные группы гормонов в зависимости от химического строения и приведите примеры. 7. ____________________________________________________
7.Перечислите актуальные проблемы в медицине, связанные с иммунодефицитом?
8.Что такое ВИЧ? Каков химический механизм летального действия ВИЧ?
9.Какова химическая структура антител?
Первый Московский Государственный Медицинский Университет им. И. М. Сеченова Лечебный факультет Кафедра общей химии
ЛАБОРАТОРНАЯ ТЕТРАДЬ ПО КУРСУ ХИМИИ БИОПОЛИМЕРОВ
СТУДЕНТА __________ ГРУППЫ
______________________ФАКУЛЬТЕТА
__________________________________ОТДЕЛЕНИЯ
__________________________________________________
__________________________________________________
Учебный год
Настоящая лабораторная тетрадь по курсу химии биополимеров предназначена для самостоятельной работы студентов лечебного и педиатрического факультетов, выполняющих практические \и теоретические задания на лабораторных занятиях. Темы занятий включают лабораторные работы, выполнение и оформление которых студенты проводят самостоятельно. Это дает возможность студентам закрепить пройденный материал и подготовиться к беседе с преподавателем, который должен оценить правильность полученных результатов и выводов. Данная лабораторная тетрадь соответствует учебному плану и включает материал интегрированного курса химии в соответствии с программой лечебного и педиатрического факультетов.
© ММА им. И. М. Сеченова
© Н. В. Головина, Д. А. Доброхотов, А. А. Лузин
Под редакцией академика РАО, профессора В. А. Попкова
Москва, 2012.
Тема: Строение и структура биополимеров.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 609; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.208.243 (0.015 с.) |




 БИОПОЛИМЕРЫ
БИОПОЛИМЕРЫ





 Методы поликонденсации полимеризации
Методы поликонденсации полимеризации получения
получения










 Структура первичная вторичная третичная четвертичная
Структура первичная вторичная третичная четвертичная цепь циклических глобулярная крупную
цепь циклических глобулярная крупную
 В четыре пробирки помещают по 1 мл растворов яичного белка. В каждую пробирку добавляют по 1 мл раствора гидроксида натрия (c(NaOH) = 1 моль/л). По стенке пробирки по 2 мл раствора сульфата меди(II). Наблюдают появление красно-фиолетовой окраски.
В четыре пробирки помещают по 1 мл растворов яичного белка. В каждую пробирку добавляют по 1 мл раствора гидроксида натрия (c(NaOH) = 1 моль/л). По стенке пробирки по 2 мл раствора сульфата меди(II). Наблюдают появление красно-фиолетовой окраски. Вывод:
Вывод: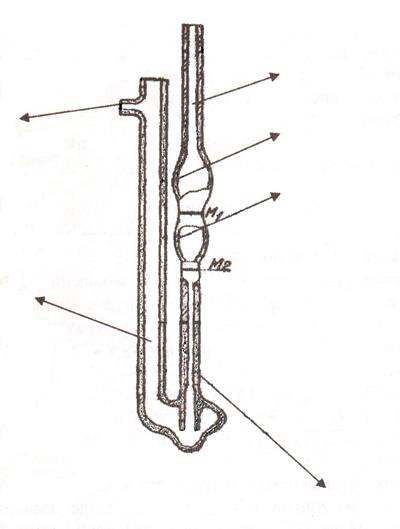
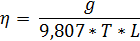
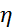 = K * Mα , отсюда M =
= K * Mα , отсюда M = 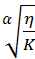
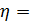 --------------
--------------
 во второй пробирке раствор (Na2SO4)=0,5 моль/л
во второй пробирке раствор (Na2SO4)=0,5 моль/л
 СН2 – СН- СООН
СН2 – СН- СООН

 NH
NH
 C=O
C=O
 CH- CH2 - COOH
CH- CH2 - COOH


