
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение атома и атомного ядраСодержание книги Похожие статьи вашей тематики
Поиск на нашем сайте Каждый атом состоит из ядра и атомной оболочки, в состав которых входят различные элементарные частицы – нуклоны и электроны (рис. 5.1). Ядро – центральная часть атома, содержащая практически всю массу атома и обладающая положительным зарядом. Ядро состоит из протонов и нейтронов, которые являются двухзарядными состояниями одной элементарной частицы – нуклона. Заряд протона +1; нейтрона 0. Заряд ядра атома равен Z . ē, где Z – порядковый номер элементов (атомный номер) в периодической системе Менделеева, равный числу протонов в ядре; ē – заряд электрона. Число нуклонов в ядре называется массовым числом элемента (A): A = Z + N, где Z – число протонов; N – число нейтронов в атомном ядре. Для протонов и нейтронов массовое число принимают равное 1, для электронов равное 0.
Рис. 5.1. Строение атома
Общеприняты следующие обозначения для какого-нибудь химического элемента X: Атомные ядра одного и того же элемента могут содержать разное число нейтронов N. Такие разновидности атомных ядер называются изотопами данного элемента. Таким образом, изотопы имеют: одинаковый атомный номер, но различные массовые числа A. Большинство химических элементов представляют собой смесь различных изотопов, например изотопы урана:
Атомные ядра различных химических элементов могут иметь одинаковое массовое число А (с разным числом протонов Z). Такие разновидности атомных ядер называются изобарами. Например:
Атомная масса
Тогда атомную массу элемента можно определить как:
где М – атомная масса изотопов рассматриваемого элемента. Это выражение облегчает определение массы ядер элементов, элементарных частиц, частиц – продуктов радиоактивных превращений и т. д. Дефект массы ядра и энергия связи ядра Энергия связи нуклона – физическая величина, численно равная работе, которую нужно совершить для удаления нуклона из ядра без сообщения ему кинетической энергии. Нуклоны связаны в ядре благодаря ядерным силам, которые значительно превосходят силы электростатического отталкивания, действующие между протонами. Для расщепления ядра необходимо преодолеть эти силы, т. е. затратить энергию. Соединение нуклонов с образованием ядра, напротив, сопровождается высвобождением энергии, которую называют энергией связи ядра Δ W св:
где Энергия связи ядра – физическая величина, равная работе, которую нужно совершить для расщепления ядра на отдельные нуклоны без сообщения им кинетической энергии. При образовании ядра происходит уменьшение его массы, т. е. масса ядра меньше, чем сумма масс составляющих его нуклонов, эта разница называется дефектом масс Δ m:
где mp – масса протона; mn – масса нейтрона; m ядр – масса ядра. При переходе от массы ядра m ядр к атомным массам элемента m а, это выражение можно записать в следующем виде:
где m H – масса водорода; mn –масса нейтрона и m а – атомная масса элемента, определенные через атомную единицу массы (а.е.м.). Критерием устойчивости ядра является строгое соответствие в нем числа протонов и нейтронов. Для устойчивости ядер справедливо следующее соотношение:
где Z – число протонов; A – массовое число элемента. Из известных к настоящему времени примерно 1700 видов ядер, только около 270 являются стабильными. Причем в природе преобладают четно-четные ядра (т. е. с четным числом протонов и нейтронов), которые являются особенно стабильными.
Радиоактивность Радиоактивность – превращение неустойчивых изотопов одного химического элемента в изотопы другого химического элемента с выделением некоторых элементарных частиц. Различают: естественную и искусственную радиоактивность. К основным видам относят: – α-излучение (распад); – β-излучение (распад); – спонтанное деление ядра. Ядро распадающегося элемента называется материнским, а ядро образующегося элемента – дочерним. Самопроизвольный распад атомных ядер подчиняется следующему закону радиоактивного распада:
где N 0 – число ядер в химическом элементе в начальный момент времени; N – число ядер в момент времени t; Величина обратная «постоянной» распада
Связь между
При радиоактивном распаде выполняется закон сохранения заряда:
где
где 5.4.1. α и β-распад α-распад представляет собой излучение ядер гелия Правило смещения при α-распаде имеет следующий вид (происходит образование нового элемента):
Пример:
Отметим, что α-распад (излучение) обладает наибольшей ионизирующей способностью, но наименьшей проницаемостью. Различают следующие виды β-распада: – электронный β-распад (β–-распад); – позитронный β-распад (β+-распад); – электронный захват (k-захват). β–-распад происходит при избытке нейтронов
β+-распад происходит при избытке протонов
Для электронного захвата (k -захвата) характерно следующее превращение:
Правило смещения при β-распаде имеет следующий вид (происходит образование нового элемента): для β–-распада: для β+-распада: β-распад (излучение) обладает наименьшей ионизирующей способностью, но наибольшей проницаемостью. α и β-излучения сопровождаются γ-излучением, которое представляет собой излучение фотонов и не является самостоятельным видом радиоактивного излучения. γ-фотоны выделяются при уменьшении энергии возбужденных атомов и не вызывают изменение массового числа A и изменение заряда Z. γ-излучение обладает наибольшей проникающей способностью. Активность радионуклидов Активность радионуклидов – мера радиоактивности, характеризующая число распадов ядер в единицу времени. Для определенного количества радионуклидов в определенном энергетическом состоянии в заданный момент времени активность А задается в виде:
где Самопроизвольное ядерное превращение называют радиоактивным распадом. Единицей измерения активности радионуклидов является обратная секунда ( Беккерель равен активности радионуклида в источнике, в котором за время 1 сек. происходит одно спонтанное ядерное превращение. Внесистемная единица активности – кюри (Ku). Кюри – активность радионуклида в источнике, в котором за время 1 сек. происходит 3,7. 1010 спонтанных ядерных превращений, т. е. 1 Ku = 3,7. 1010 Бк. Например, примерно 1 г чистого радия дает активность 3,7. 1010 ядерных распадов в секунду. Не все ядра радионуклида распадаются одновременно. В каждую единицу времени самопроизвольное ядерное превращение происходит с определенной долей ядер. Доля ядерных превращений для разных радионуклидов различна. Например, из общего числа ядер радия ежесекундно распадается 1,38. Из приведенных определений следует, что активность А связана с числом радиоактивных атомов N в источнике в данный момент времени соотношением:
С течением времени число радиоактивных атомов уменьшается по закону:
где Отсюда следует, что и активность радионуклида также уменьшается за время t по экспоненциальному закону:
где По прошествии определенного времени
У различных радионуклидов период полураспада варьируется в очень широких пределах: от миллиардов лет до миллионных долей секунды. Например, период полураспада урана равен 4,5 млрд лет, радия – 1622 года, цезия После подстановки выражения (5) в формулы (3) и (4) получим:
Различают также следующие разновидности радионуклида. Отношение активности радионуклида в источнике к его массе или объему (для объемных источников) называется удельной или объемной активностью, соответственно:
где Если отношение активности берется к площади поверхности или к длине источника, то эти отношения называют соответственно поверхностной или линейной активностью. Выбор единиц удельной активности определяется конкретной задачей. Например, активность в воздухе выражают в беккерелях на кубический метр (Бк/м3) – объемная активность. Активность в воде, молоке и других жидкостях также выражается как объемная активность, так как количество воды и молока измеряется в литрах (Бк/л). Активность в хлебе, картофеле, мясе и других продуктах выражается как удельная активность (Бк/кг). Очевидно, что биологический эффект воздействия радионуклидов на организм человека будет зависеть от их активности, т. е. от количества радионуклида. Поэтому объемная и удельная активность радионуклидов в воздухе, воде, продуктах питания, строительных и других материалах нормируются. Поскольку в течение определенного времени человек может облучаться различными путями (от поступления радионуклидов в организм до внешнего облучения), то все факторы облучения связывают определенной величиной, которая называется дозой облучения.
|
||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 6492; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.62 (0.01 с.) |


 , здесь A – массовое число, Z – атомный номер элемента.
, здесь A – массовое число, Z – атомный номер элемента. .
. –
– 
 –
– 
 –
–  ;
;  –
– 
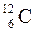 Для характеристики массы атомов и молекул используют понятие атомной массы M – это относительная величина, которая определяется по отношению
Для характеристики массы атомов и молекул используют понятие атомной массы M – это относительная величина, которая определяется по отношению 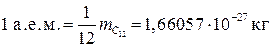 .
.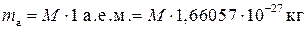 ,
, ,
, – так называемый дефект массы ядра; с ≈ 3. 108 м/с – скорость света в вакууме.
– так называемый дефект массы ядра; с ≈ 3. 108 м/с – скорость света в вакууме. ,
, ,
, ,
, ,
, – так называемая «постоянная» распада, которая представляет собой долю ядер, распавшихся в единицу времени.
– так называемая «постоянная» распада, которая представляет собой долю ядер, распавшихся в единицу времени. , характеризует среднюю продолжительность жизни изотопа. Характеристикой устойчивости ядер относительно к распаду является период полураспада
, характеризует среднюю продолжительность жизни изотопа. Характеристикой устойчивости ядер относительно к распаду является период полураспада 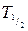 , т. е. время, в течение которого первоначальное количество ядер уменьшается вдвое:
, т. е. время, в течение которого первоначальное количество ядер уменьшается вдвое: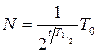 .
.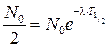 ,
, 
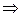
 .
.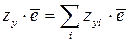 ,
,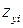 – заряд распавшихся или получившихся (образовавшихся) «осколков»; и правило сохранения массовых чисел:
– заряд распавшихся или получившихся (образовавшихся) «осколков»; и правило сохранения массовых чисел: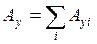 ,
,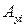 – массовое число образовавшихся (распавшихся) «осколков».
– массовое число образовавшихся (распавшихся) «осколков».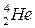 . Характерен для «тяжелых» ядер с большими массовыми числами A > 200 и зарядом z > 82.
. Характерен для «тяжелых» ядер с большими массовыми числами A > 200 и зарядом z > 82. .
.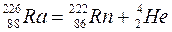 ;
;  .
. с выделением электронов
с выделением электронов 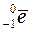 и антинейтрино
и антинейтрино 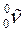 :
: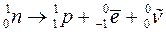 .
.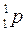 с выделением позитронов
с выделением позитронов 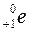 и нейтрино
и нейтрино  :
: .
.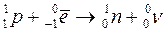 .
.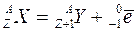 ;
;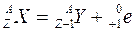 .
.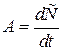 , (1)
, (1) – ожидаемое число спонтанных ядерных превращений (число распадов ядер), происходящих в источнике ионизирующего излучения за интервал времени
– ожидаемое число спонтанных ядерных превращений (число распадов ядер), происходящих в источнике ионизирующего излучения за интервал времени  .
.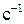 ), имеющая специальное название беккерель (Бк).
), имеющая специальное название беккерель (Бк).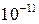 часть, а из общего количества ядер радона – 2,1.
часть, а из общего количества ядер радона – 2,1.  часть. Доля ядер, распадающихся в единицу времени, называется постоянной распада λ.
часть. Доля ядер, распадающихся в единицу времени, называется постоянной распада λ.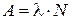 . (2)
. (2) , (3)
, (3) – число оставшихся радиоактивных атомов по прошествии времени t;
– число оставшихся радиоактивных атомов по прошествии времени t; 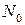 – число радиоактивных атомов радионуклида в начальный момент времени: t = 0.
– число радиоактивных атомов радионуклида в начальный момент времени: t = 0. , (4)
, (4) – активность радионуклида в начальный момент времени t = 0.
– активность радионуклида в начальный момент времени t = 0.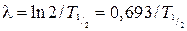 . (5)
. (5) – 30 лет, радона
– 30 лет, радона 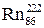 – 3,8 дня и т. д.
– 3,8 дня и т. д.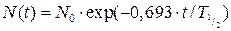 ; (6)
; (6)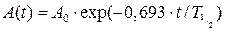 . (7)
. (7)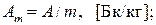
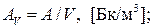 (8)
(8)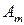 ,
, 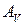 – удельная и объемная активность вещества; А – активность радионуклида в источнике; m, V – масса и объем вещества, носителя радионуклида.
– удельная и объемная активность вещества; А – активность радионуклида в источнике; m, V – масса и объем вещества, носителя радионуклида.


