
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Перед решением задач рекомендуетсяСодержание книги
Поиск на нашем сайте I. Уяснить следующие основные понятия: 1) комплексное соединение; номенклатура комплексных соединений; 2) центральный атом (комплексообразователь), лиганд; 3) координационное число, дентатность; 4) константа образования и константа нестойкости комплексных соединений; их математическое выражение.
II. Обратить внимание на то, что: 1) индекс приведенных в справочнике значений К н указывает по какому числу ступеней идет диссоциация; совпадает с координационным числом (к.ч.) центрального атома. Например, К 1-2 - означает, что диссоциация протекает по двум ступеням, координационное число центрального атома равно 2; 2) комплексы металлов с цитрат- ионом и этилендиаминтетраацетат-ионом в большинстве случаев имеют состав 1:1; 3) d - элементы с биолигандами образуют комплексные соединения как состава 1:1 (в таблице отмечены (*)), так и состава 1:2. Следовательно, для первых приведены значения К 1, для вторых - значения К 1-2. Примеры решения типовых задач Пример 1 Расчет концентрации комплексообразователя в растворе комплексного соединения, содержащем избыток лиганда. Вычислите концентрацию иона цинка в растворе тетрацианоцинката натрия с концентрацией 0,3 моль/л при избытке цианид-ионов, равном 0,01 моль/л. Решение. Ионы цинка в свободном виде в растворе могут находится только при полной диссоциации комплекса: Диссоциация по внешней координационной сфере протекает практически полностью: Na2[Zn(CN)4] ® 2Na+ + [Zn(CN)4]2- Диссоциация комплексной частицы по внутренней координационной сфере: [Zn(CN)4]2- Û Zn2+ + 4CN- Запишем для этого процесса выражение константы химического равновесия, она равна константе нестойкости[Zn(CN)4]2: с (Zn2+) c 4(CN-) К н = ¾¾¾¾¾¾¾¾ с (компл.иона) Преобразуем это выражение относительно Кн: К н с (компл.иона) с (Zn2+)= ¾¾¾¾¾¾¾ c 4(CN-) где Кн - табличная величина (см. справочник табл.); К н = 2,4×10-20. Поскольку концентрация цианид-ионов, образующихся в результате диссоциации комплексного иона, значительно меньше концентрации введенного избытка, можно считать, что с (CN-) = 0,01 моль/л, т.е. концентрацией цианид-ионов, образующихся в результате диссоциации комплексного иона пренебрегаем. Таким образом, подстановка в полученное выражение дает следующий результат: 2,40×10-20× 0,3 с (Zn2+) = ¾¾¾¾¾¾ = 7,2 × 10-13 моль/л (0,01)4 Ответ: 7,2 × 10-13 моль/л.
Пример 2 Расчет массы комплексообразователя в растворе комплексного соединения известного объема, содержащем избыток лиганда. Вычислите массу серебра, содержащегося в виде ионов в растворе хлорида диамминсеребра(I) с концентрацией 0,03 моль/л объемом 750 мл. Раствор содержит аммиак, концентрация которого равна 0,1 моль/л. Решение. Ионы серебра в свободном виде в растворе могут находиться при полной диссоциации комплекса: [Ag(NH3)2]+ Û Ag+ + 2NH3 Запишем для этого процесса константу химического равновесия, она будет равна константе нестойкости диамминсеребра: с (Ag+) с 2(NН3) К н = ¾¾¾¾¾¾¾¾¾ с (компл.иона) В данном выражении используют значение с (NH3) = 0,1 моль/л, т.к. концентрация аммиака, образующегося при диссоциации комплексного иона, значительно меньше этой величины и,следовательно, ею можно пренебречь. Отсюда, К н с (компл.иона) 5,89 ×10 –8× 0,3 с (Ag+) = ¾¾¾¾¾¾¾¾ = ¾¾¾¾¾¾¾ = 1,77 ×10 –6 моль/л с 2(NН3) 0,12
m(Ag+) = M(Ag) Vc (Ag+) = 108 г/моль × 0,75 л ×1,77× 10-6 моль/л = 1,43 ×10-4 г Ответ: 1,43 × 10-4 г.
Пример 3 Расчет концентрации иона металла в растворе после введения избытка лиганда. Во сколько раз изменится концентрация иона железа(Ш) при введении в раствор хлорида железа(Ш) с концентрацией 0,5 моль/л тартрат-ионов до концентрации 0,05 моль/л? Решение. Концентрация ионов Fe3+ в исходном растворе равна молярной концентрации (0,5 моль/л). После введения татрат -ионов ионы железа связываются в комплекс. Молярная концентрация образовавшегося комплексного иона будет равна молярной концентрации исходного раствора хлорида железа, т.к. тартрат-ион был введен в избытке, а стехиометрическое соотношение между ионом железа(Ш) и его комплексом равно 1:1. Обозначим двухзарядный анион винной кислоты Tartr2-. Концентрация ионов железа(Ш) будет определяться теперь нестойкостью образовавшегося дитартратного комплекса: [Fe(Tartr)2]- Û Fe3+ + 2 Tartr2- Аналогично решению предыдущей задачи: К н с (компл.иона) 1,38×10-12× 0,5 c (Fe3+) = ¾¾¾¾¾¾¾¾¾ = ¾¾¾¾¾¾ = 2,76× 10-10 моль/л с2(Tartr2-) (0,05)2 0,5 Ответ: отношение концентраций ¾¾¾¾¾ = 1,8 ×109 т.е. концентрация ионов железа уменьшится в 1,8 млрд. раз. 2,76 ×10-10
Пример 4 Расчет концентрации и массы иона металла в растворе после введения избытка лиганда. К хлориду кальция массой 1,11 г добавили аммиачный буферный раствор и раствор объемом 1 л этилендиаминтетраацетата натрия с концентрацией 0,05 моль/л. Вычислите массу кальция, содержащегося в виде ионов в таком растворе. Вычислите, какая часть ионов кальция находится в свободном состоянии, а какая - в связанном виде. Решение. Вычислим количество веществ хлорида кальция и этилендиаминтетраацетата натрия: m 1,11 г n(CаСl2) = ¾¾ = ¾¾¾¾¾ = 0,01 моль M111г/моль n(Nа2Н2ЭДТА) = сV = 0,05× 1 = 0,05 моль СаСl2 + Nа2Н2ЭДТА = СаН2ЭДТА + 2NаСl Хлорид кальция вступает в реакцию полностью, поэтому n(СаН2ЭДТА) = n(СаСl2) = 0,01 моль n(NаН2ЭДТА)ост =0,05 – 0,01 моль = 0,04 моль соответственно, с (NаН2ЭДТА) = 0,04 моль/л. Ионы кальция в свободном виде в растворе могут находиться только при полной диссоциации комплекса: СаН2ЭДТА Û Ca2+ + ЭДТА4- + 2Н+ Применяемый аммиачный буфер нейтрализует образовавшиеся в результате реакции ионы водорода. Концентрация ионов кальция (свободная часть ионов кальция) определяется из выражения константы нестойкости: К н с (компл.иона) с (Са2+)своб = ¾¾¾¾¾¾¾¾ с (ЭДТА4-) Подставив в это выражение значения К н (СаЭДТА2-)(табл.), концентрации комплексного иона и лиганда, вычислим концентрацию свободных ионов кальция: 2,57× 10-11×0,01 с (Са2+)своб = ¾¾¾¾¾¾¾ = 6,43× 10-12 моль/л 0,04 m(Са2+) = c M V = 6,43 ×10-12 моль/л ×40 г ×1л = 2,57×10-10 г Концентрация ионов кальция в связанном виде определяется разностью концентраций комплексного иона и свободных ионов кальция: с (Са2+)связ = 0,01 - 6,43 ×10-11 с (Са2+) связ 0,01 моль/л ¾¾¾¾ = ¾¾¾¾¾¾¾¾¾ = 1,56×109 с (Са2+) своб 6,43× 10-12 моль/л Ответ: масса ионов кальция равна 2,57×10-10 г; на одну часть свободных ионов приходится 1,56×109 частей связанных.
Пример 5. Определение направления смещения лигандообменных процессов. В каком направлении сместится равновесие реакции, если смешать реагенты в указанных концентрациях:
Тетраамминмедь(П)-ион Û медь(П)-ион + аммиак 0,1 моль/л 0,0000001 моль/л 2 моль/л
Решение: Для ответа на вопрос задачи воспользуемся уравнением изотермы химической реакции: DG = - RTln K н + RTlnПс.
Вычислим Пс и сравним его с табличным значением константы, которое найдем в табл. Поскольку записанный процесс представляет собой полную диссоциацию комплексного иона, Пс надо сравнить с константой нестойкости [Cu(NH3)4]2+. В случае Пс< К н пойдет прямой процесс, т.е. положение равновесия сместится вправо; в случае Пс> К н - влево. с (Сu 2+) с 4(NH3) 0,0000001×24 Пс = ¾¾¾¾¾¾¾¾ = ¾¾¾¾¾¾¾¾ = 1,60×10 -5 с (компл.иона) 0,1 Табличное значение константы нестойкости иона равно 9,33 ×10-13. Ответ: поскольку Пс> Кн, положение равновесия сместится влево.
Пример 6 Сравнение концентраций катионов металлов в растворах комплексных соединений в отсутствие избытка лиганда. Во сколько раз концентрация ионов кальция будет больше концентрации ионов марганца в растворах их комплексов с глицином одинаковых концентраций? Решение. Ионы кальция в свободном виде в растворе могут находиться при полной диссоциации комплекса: [Са-Gly]+ Û Са2+ + Gly – где Gly = глицин Запишем для этого процесса константу химического равновесия, она будет равна константе нестойкости: с (Са2+) с (Gly –-) К н = ¾¾¾¾¾¾¾ с (Ca-Gly) Обозначим за х концентрацию ионов кальция в растворе, тогда с (Са2+) = с (Gly –) = х; х2 К н = ¾¾¾¾¾; с (Ca-Gly –) Откуда ¾¾¾¾¾¾ х = с (Са2+) = Ö К н с (Ca-Gly)
Аналогично рассуждая, выразим концентрацию ионов марганца: ¾¾¾¾¾¾ с (Мn2+) = Ö К н с (Mn-Gly) Учитывая, что концентрации комплексов одинаковы, выразим и вычислим отношение концентраций ионов кальция и марганца:
¾¾¾¾¾¾ ¾¾¾¾¾¾¾¾¾ ¾¾¾¾ ¾¾¾¾¾ с (Са2+) Ö К н с (Ca-Gly) К н (Ca-Gly) с (Ca-Gly) К н(Ca-Gly) 4,17×10-2 ¾¾¾ = ¾¾¾¾¾¾¾ = Ö ¾¾¾¾¾¾¾¾¾ = Ö ¾¾¾ = Ö ¾¾¾¾¾ = 10,72 с (Мn2+) Ö К н с (Mn-Gly) К н (Mn-Gly) с (Mn-Gly) К н(Mn-Gly) 3,63×10-4
Ответ: концентрация ионов кальция больше в 11 раз концентрации ионов марганца в растворах их комплексов с глицином.
Пример 7 Расчет константы нестойкости с использованием стандартного изменения энергии Гиббса совмещенного лигандообменного процесса. Реакция замещения Са2+ на Ве2+ в составе комплекса с ЭДТА 4- характеризуется DG° = 11,8 кДж/моль. Вычислите константу нестойкости комплекса ВеЭДТА2-. Решение. Запишем уравнение замещения Са2+ на Ве2+ в составе комплекса с ЭДТА 4-: СаЭДТА2- + Ве2+Û ВеЭДТА2- + Са2+ Константы совмещенного лигандообменного процесса равна отношению константы нестойкости комплексного соединения, стоящего в левой части уравнения, на константу нестойкости комплексного соединения вещества, стоящего в правой части уравнения. Таким образом: К н(СаЭДТА2-) К = ¾¾¾¾¾¾¾; К н(ВеЭДТА2-) Величины DG° и К связаны между собой соотношением: DG0 = - RTln К. Вычислм константу равновесия:
К = е -DG0/RT
К = е-11800/8,31×298 = 8,52×10-3
Выразим и вычислим К н(ВеЭДТА2-): К н(СаЭДТА2-) 2,57×10-11 К н(ВеЭДТА2-) = ¾¾¾¾¾¾ = ¾¾¾¾¾¾¾ = 3,02×10-9 К 8,52×10-3 Ответ: 3,02×10-9 Задания для самостоятельной работы из «Сборника задач и упражнений по общей химии». 7.9;7.10; 7.45; 7.53; 7.39; 7.657.70; 7.72
Изучение реакций комплексообразования с неорганическими лигандами. Цель: Изучить реакции ионов-биометаллов и ионов-токсикантов с неорганическими лигандами на примере образования аммино- и гидроксокомплексов. Задание: выполнить серию опытов, связанных с изучением возможности образования аммин- и гидроксокомплексов. Оборудование и реактивы: Штатив с пробирками. Растворы растворимых солей железа(Ш), кобальта (П), никеля(П), меди (П), цинка, алюминия, свинца(П) (с=0,1моль/л); раствор гидроксида натрия (с=0,1моль/л) и концентрированный; раствор аммиака концентрированный, тиоцианида калия (с=0,1моль/л). Сущность работы: визуальное наблюдение за изменениями, происходящими в пробирках. На первом этапе получают гидроксиды изучаемых ионов металлов. К полученным гидроксидам добавляют концентрированные растворы щелочи и аммиака. Об образовании прочного комплексного соединения судят по растворению осадка гидроксида. Выполнить опыт по изучению влияния природы растворителя на устойчивость комплексов. Выполнение эксперимента: Опыт 1. Получают нерастворимые гидроксиды. Изучают возможность образования гидроксокомплексов. Уравнения реакций:
Опыт 2. Изучают возможность образования амминкомплексов Уравнения реакций:
Опыт 3. Образование амминокомплексов кобальта. Опыт 4. Изучение влияния природы растворителя на устойчивость комплексного иона (лаб.работа опыт 2). Уравнение реакции:
Наблюдения:
Вывод: Экспериментальные данные
Вывод оформляют в виде перечисления: - ионы, образующие прочные и аммино- и гидроксокомплексы … - ионы, образующие прочные только амминокомплексы … - ионы, образующие прочные только гидроксокомплексы … - ионы, не образующие прочные ни аммино- ни гидроксокомплексы …
|
||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-14; просмотров: 694; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.62 (0.008 с.) |

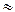 0,01 моль/л
0,01 моль/л


