
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Элементарные и фундаментальные частицы. Обменный механизм взаимодействий.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Элемента́рная части́ца — собирательный термин, относящийся к микрообъектам в субъядерном масштабе, которые невозможно расщепить (или пока это не доказано) на составные части. Их строение и поведение изучается физикой элементарных частиц. Понятие элементарных частиц основывается на факте дискретного строения вещества. Ряд элементарных частиц имеет сложную внутреннюю структуру, однако разделить их на части невозможно. Другие элементарные частицы являются бесструктурными и могут считаться первичными фундаментальными частицами. Со времён первого открытия элементарной частицы (электрона) в 1897 году обнаружено уже более 400 элементарных частиц. Фундаментальные (бесструктурные) частицы: лептоны — фермионы, которые имеют вид точечных частиц (т. е. не состоящих ни из чего) вплоть до масштабов порядка 10−18 м. Не участвуют в сильных взаимодействиях. Участие в электромагнитных взаимодействиях экспериментально наблюдалось только для заряженных лептонов (электроны, мюоны, тау-лептоны) и не наблюдалось для нейтрино. Известны 6 типов лептонов. кварки — дробнозаряженные частицы, входящие в состав адронов. В свободном состоянии не наблюдались. Как и лептоны, делятся на 6 типов и являются бесструктурными, однако, в отличие от лептонов, участвуют в сильном взаимодействии. калибровочные бозоны — частицы, посредством обмена которыми осуществляются взаимодействия: фотон — частица, переносящая электромагнитное взаимодействие; восемь глюонов — частиц, переносящих сильное взаимодействие; три промежуточных векторных бозона W+, W− и Z0, переносящие слабое взаимодействие; гравитон — гипотетическая частица, переносящая г гравитационное взаимодействие. Существование гравитонов, хотя пока не доказано экспериментально в связи со слабостью гравитационного взаимодействия, считается вполне вероятным; однако гравитон не входит в Стандартную модель. Фундаментальные взаимодействия. Процессы, в которых участвуют различные элементарные частицы, сильно различаются по энергиям и характерным временам их протекания. Согласно современным представлениям, в природе осуществляется четыре вида взаимодействий, которые не могут быть сведены к другим, более простым видам:сильное, электромагнитное, слабое и гравитационное. Эти виды взаимодействий называют фундаментальными. Сильное (или ядерное) взаимодействие – наиболее интенсивное. Оно обуславливает исключительно прочную связь между протонами и нейтронами в ядрах атомов. В сильном взаимодействии могут принимать участие только тяжелые частицы – адроны (мезоны и барионы). Сильное взаимодействие проявляется на расстояниях порядка10–15 м и менее. Поэтому его называют короткодействующим. Электромагнитное взаимодействие. В нем могут принимать участие любые электрически заряженные частицы, а так же фотоны – кванты электромагнитного поля. Электромагнитное взаимодействие ответственно, в частности, за существование атомов и молекул. Оно определяет многие свойства веществ в твердом, жидком и газообразном состояниях. Кулоновское отталкивание протонов приводит к неустойчивости ядер с большими массовыми числами. Электромагнитное взаимодействие обуславливает процессы поглощения и излучения фотонов атомами и молекулами вещества и многие другие процессы физики микро- и макромира. Слабое взаимодействие – определяет ход наиболее медленных процессов, протекающих в микромире. В нем могут принимать участие любые элементарные частицы, кроме фотонов. Слабое взаимодействие ответственно за протекание процессов с участием нейтрино или антинейтрино, например, β-распад нейтрона
а также безнейтринные процессы распада частиц с большим временем жизни (τ ≥ 10–10 с). Гравитационное взаимодействие присуще всем без исключения частицам, однако из-за малости масс элементарных частиц силы гравитационного взаимодействия между ними пренебрежимо малы и в процессах микромира их роль несущественна. Гравитационные силы играют решающую роль при взаимодействии космических объектов (звезд, планет и т. п.) с их огромными массами. В 30-е годы XX века возникла гипотеза о том, что в мире элементарных частиц взаимодействия осуществляются посредством обмена квантами какого-либо поля. Эта гипотеза первоначально была выдвинута нашими соотечественниками И. Е. Таммом и Д. Д. Иваненко. Они предположили, что фундаментальные взаимодействия возникают в результате обмена частицами, подобно тому, как ковалентная химическая связь атомов возникает при обмене валентными электронами, которые объединяются на незаполненных электронных оболочках. Взаимодействие, осуществляемое путем обмена частицами, получило в физике название обменного взаимодействия. Так, например, электромагнитное взаимодействие между заряженными частицами, возникает вследствие обмена фотонами – квантами электромагнитного поля. Теория обменного взаимодействия получила признание после того, как в 1935 г. японский физик Х. Юкава теоретически показал, что сильное взаимодействие между нуклонами в ядрах атомов может быть объяснено, если предположить, что нуклоны обмениваются гипотетическими частицами, получившими название мезонов. Юкава вычислил массу этих частиц, которая оказалась приблизительно равной 300 электронным массам. Частицы с такой массой были впоследствии действительно обнаружены. Эти частицы получили название π-мезонов (пионов). В настоящее время известны три вида пионов: π+, π– и π0 (см. табл. 6.9.1). В 1957 году было теоретически предсказано существование тяжелых частиц, так называемых векторных бозонов W+, W– и Z0, обуславливающих обменный механизм слабого взаимодействия. Эти частицы были обнаружены в 1983 году в экспериментах на ускорителе на встречных пучках протонов и антипротонов с высокой энергией. Открытие векторных бозонов явилось очень важным достижением физики элементарных частиц. Это открытие ознаменовало успех теории, объединившей электромагнитное и слабое взаимодействия в единое так называемое электрослабое взаимодействие. Эта новая теория рассматривает электромагнитное поле и поле слабого взаимодействия как разные компоненты одного поля, в котором наряду с квантом участвуют векторные бозоны.
5.1 Молекурярно-кинетические представления о строении вещества в различных агрегатных состояниях. Статистический метод описания состояния и поведения систем многих частиц. Распределение молекул идеального газа по состояниям.: Тела, которые нас окружают (твердые, жидкие, газообразные) воспринимаются нашими органами чувств как сплошные. Однако, тела не сплошные, а состоят из мельчайших невидимых невооруженным глазом частичек, расположенных не вплотную друг к другу, а на некотором расстоянии. Называют эти мельчайшие частицы вещества молекулами (уменьшительное от латинского слова "масса"). Демокрит (V в. до н. э.) назвал мельчайшие частицы, из которых состоят все тела в мире, атомами (неделимыми). Согласно Демокриту атомы имеют разные размеры, вес, форму и т.п 1) Все вещества состоят из мельчайших частиц - молекул. Молекула - наименьшая частица вещества, сохраняющая все его химические свойства. Все молекулы, образующие данное вещество, совершенно одинаковы. Молекулы состоят из атомов. Атом - мельчайшая частица химического элемента (105 шт.- 94 природных и 11 искусственных). 2) Между молекулами тела одновременно действуют силы взаимного притяжения и отталкивания. 3) Молекулы, образующие тела находятся в состоянии непрерывного беспорядочного движения (осцилляции). Скорость движения молекул тем выше, чем выше температура тела. Температура - мера средней кинетической энергии молекул тела. Скорость движения молекул тела, определяющих кинетическую энергию, определяет тепловое состояние тела, величину его внутренней энергии. Хаотическое движение молекул называют тепловым. Расщепление молекулы на атомы называется диссоциацией. Диссоциация происходит под действием 1) высокой температуры, 2) химических реакций, 3) облучения. В основу термодинамики входят два метода исследования частиц: термодинамический и статический. Поведение громадного числа молекул, составляющих макротела, изучается статистическим методом, который основан на том, что свойства макротел определяются свойствами молекул, особенностями их движения (скоростью, энергией, импульсом и т.д.) и взаимодействия. Например, температура может быть выражена через среднее значение кинетической энергии движения молекул. Статистический метод дает представление о механизме тепловых процессов, рассматривая их как бы изнутри макротел, он существенно дополняет термодинамический метод. Основные законы термодинамики также имеют статистический смысл. В газе, находящемся в состоянии равновесия, установится некоторое стационарное (не меняющееся со временем) распределение молекул по скоростям, которое подчиняется вполне определенному статистическому закону. Такой закон был теоретически выведен Максвеллом. При выводе этого закона Максвелл предполагал, что газ состоит из очень большого числа N тождественных молекул, находящихся в состоянии беспорядочного теплового движения при одинаковой температуре. Предполагалось также, что внешние поля на газ не действуют. Закон Максвелла описывается некоторой функцией f(v), называемой функцией распределения молекул по скоростям. Различают три формы записи распределения Максвелла. 5.2 Термодинамический метод описания состояния и поведения систем многих частиц. Термодинамические параметры, их связь по средним значениям характеристик молекул: Основное уравнение молекулярно-кинетической теории идеального газа, внутренняя энергия идеального газа, температура. Для изучения тепловых процессов в естествознании сформировался термодинамический метод исследования. Он заключается в том, что термодинамическая система рассматривается как один целостный объект (а не как множество ее элементов, молекул), и ее состояние системы задается термодинамическими параметрами (параметрами системы), характеризующими ее свойства. В качестве таковых обычно выбирают абсолютную температуру(температуру по шкале Кельвина – Т), давление(Р), молярный объем (объем одного моля вещества – VМ). Параметры связаны друг с другом, поэтому состояние системы можно представить в виде уравнения. Например, для идеального газа массой в один моль эту связь выражает уравнение Менделеева-Клапейрона: PVМ = RT, (5.1).где R = 8,314 Дж/моль * К – универсальная газовая постоянная. ОСНОВНОЕ УРАВНЕНИЕ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
Определение температуры в кинетической теории газов. В кинетической теории газов доказывается, что если две подсистемы (из одинаковых или разных молекул) могут обмениваться энергией, то в состоянии равновесия оказываются равными средние кинетические энергии поступательного движения их молекул. Исходя из этого, кинетическая теория газов определяет температуру как величину, пропорциональную средней кинетической энергии поступательного движения молекулы: где k — постоянная Больцмана, которая выражается через универсальную газовую постоянную и число Авогадро (см. разд. 2.1): k = R/Na ~1,38•10 -23 Дж/К. Коэффициент пропорциональности выбран так, чтобы уравнение состояния идеального газа. Внутренняя энергия данной массы идеального газа зависит только от его температуры и не зависит ни от давления, ни от объема. 5.3 Уравнение состояния идеального газа. Уравнения изопроцессов идеального газа. Соотношение Изотермический процесс (T = const) Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. pV = const Изохорный процесс (V = const) Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным.
Изобарный процесс (p = const) Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p.
5.4 Внутренняя энергия, способы ее изменения. Способы теплообмена. Количество теплоты. Первый закон термодинамики как закон сохранения энергии. Газ, находящийся в состоянии термодинамического равновесия, можно характеризовать внутренней энергией. Внутренней энергией называют полную энергию его молекул. В термодинамике она включает в себя суммарную кинетическую энергию теплового движения молекул и потенциальную энергию их взаимодействия. Существует два способа изменения внутренней энергии системы – механическая работа и теплопередача (теплообмен). Процесс передачи энергии от одного тела к другому без совершения работы называется теплообменом (теплопередачей). Существует три вида теплообмена: 1. теплопроводность; 2. конвекция; 3. излучение. Первый закон термодинамики - это закон сохранения энергии, распространенный на тепловые явления. Он показывает, от каких причин зависит изменение внутренней энергии. термодинамике рассматриваются тела, положение центра тяжести которых практически не меняется. Механическая энергия таких тел остается постоянной, изменяться может лишь внутренняя энергия каждого тела. В общем случае при переходе системы из одного состояния в другое внутренняя энергия изменяется одновременно как за счет совершения работы, так и за счет передачи теплоты. Первый закон термодинамики формулируется именно для таких общих случаев: Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
Если система является изолированной, то работа внешних сил равна нулю (А = 0) и система не обменивается теплотой с окружающими телами (Q = 0). В этом случае согласно первому закону термодинамики Внутренняя энергия термодинамической системы может изменяться двумя способами: посредством совершения работы над системой и посредством теплообмена с окружающей средой. Энергия, которую получает или теряет тело в процессе теплообмена с окружающей средой, называется коли́чеством теплоты́ или просто теплотой. 5.5 Работа газа, теплоемкость, изменение внутренней энергии, первый закон термодинамики при изопроцессах. Работой газа называется его неквазистатическое расширение, а также последующее давление на определенную поверхность (как правило данный закон выполним для газа, находящегося в закрытом пространстве, например, поршне) под действием внешних сил.Теплоемкость– свойство материала поглощать определенное количество тепла при нагревании и выделять его при охлаждении.Газ, находящийся в состоянии термодинамического равновесия, можно характеризовать внутренней энергией. Внутренней энергией называют полную энергию его молекул. В термодинамике она включает в себя суммарную кинетическую энергию теплового движения молекул и потенциальную энергию их взаимодействия.Закон Генри — закон, по которому при постоянной температуре растворимость газа в данной жидкости прямо пропорциональна давлению этого газа над раствором. Закон пригоден лишь для идеальных растворов и невысоких давлений.
|
||||||
|
Последнее изменение этой страницы: 2016-07-11; просмотров: 1300; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.75.147 (0.008 с.) |


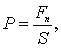 где S - площадь этой поверхности; - сумма приложенных перпендикулярно сил. При неравномерном распределении сил по поверхности равенство определяет среднее давление на данную площадку, а в пределе, при стремлении S к кулю, - давление в данной точке:
где S - площадь этой поверхности; - сумма приложенных перпендикулярно сил. При неравномерном распределении сил по поверхности равенство определяет среднее давление на данную площадку, а в пределе, при стремлении S к кулю, - давление в данной точке: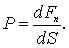 По кинетической теории давление газа на стенки сосуда возникает в результате непрерывных ударов о них отдельных молекул. Эти удары молекул о стенки приводят к некоторым смешениям частиц материала стенки и, значит, к ее деформации. Деформированная же стенка действует на газ упругой силой, направленной в каждой точке перпендикулярно к стенке. Сила эта равна по абсолютному значению и противоположна по направлению силе, с которой газ действует на стенку.
По кинетической теории давление газа на стенки сосуда возникает в результате непрерывных ударов о них отдельных молекул. Эти удары молекул о стенки приводят к некоторым смешениям частиц материала стенки и, значит, к ее деформации. Деформированная же стенка действует на газ упругой силой, направленной в каждой точке перпендикулярно к стенке. Сила эта равна по абсолютному значению и противоположна по направлению силе, с которой газ действует на стенку.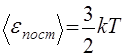
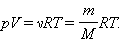 называется уравнением состояния идеального газа. Для одного моля любого газа это соотношение принимает вид: pV=RT.
называется уравнением состояния идеального газа. Для одного моля любого газа это соотношение принимает вид: pV=RT.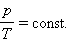


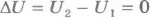 или U1=U2. Внутренняя энергия изолированной системы остается неизменной (сохраняется).
или U1=U2. Внутренняя энергия изолированной системы остается неизменной (сохраняется). Собственно, закон Генри констатирует достаточно простой факт: чем выше давление газа над поверхностью жидкости, тем труднее растворенному в ней газу высвободиться. И это совершенно логично с точки зрения молекулярно-кинетической теории, поскольку молекуле газа, чтобы вырваться на свободу с поверхности жидкости, нужно преодолеть энергию соударений с молекулами газа над поверхностью, а чем выше давление и, как следствие, число молекул в приграничной области, тем сложнее растворенной молекуле преодолеть этот барьер.
Собственно, закон Генри констатирует достаточно простой факт: чем выше давление газа над поверхностью жидкости, тем труднее растворенному в ней газу высвободиться. И это совершенно логично с точки зрения молекулярно-кинетической теории, поскольку молекуле газа, чтобы вырваться на свободу с поверхности жидкости, нужно преодолеть энергию соударений с молекулами газа над поверхностью, а чем выше давление и, как следствие, число молекул в приграничной области, тем сложнее растворенной молекуле преодолеть этот барьер.


