
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Двойной электрический слой и электрокинетические явленияСодержание книги
Поиск на нашем сайте
При рассмотрении строения мицеллы было показано, что на поверхности лиофобных коллоидов образуется двойной электрический слой. Первая теория строения ДЭС была развита Гельмгольцем и Перреном; в их представлении двойной электрический слой подобен плоскому конденсатору, внутренняя обкладка которого находится в твердой фазе, а внешняя – в жидкости параллельно поверхности ядра на расстоянии порядка диаметра иона. Потенциал электрического поля внутри ДЭС φ в этом случае линейно уменьшается с увеличением расстояния от поверхности r (рис. 4.12а). Позднее Гуи и Чепмен предложили другую модель, согласно которой противоионы, благодаря тепловому движению, образуют вблизи твердой поверхности ядра диффузную ионную атмосферу. Уменьшение электрического потенциала ДЭС φ с увеличением расстояния r в этом случае происходит нелинейно (рис. 4.12б).
Рис. 4.12 Строение ДЭС: а) – по Гельмгольцу и Перрену, б) – по Гуи и Чепмену, в) – по Штерну. Вверху – схема расположения противоионов, внизу – зависимость потенциала от расстояния Предложенная Штерном модель строения ДЭС объединяет ранние модели, учитывая как адсорбцию противоионов, так и их тепловое движение. Согласно этой модели, являющейся в настоящее время общепринятой, часть противоионов находится на расстояниях порядка диаметра иона от поверхности ядра, образуя т.н. слой Гельмгольца (адсорбционный слой противоионов), а другая часть образует диффузный слой (т.н. слой Гуи). Потенциал диффузной части двойного электрического слоя называют электрокинетическим потенциалом (см. рис.4.12в). Электрокинетический потенциал обычно обозначают греческой буквой ζ (дзета) и называют поэтому дзета-потенциалом. Поскольку ζ-потенциал пропорционален заряду коллоидной частицы, агрегативная устойчивость золя пропорциональна его величине. Если поместить золь в постоянное электрическое поле, то, как и в растворах электролитов, заряженные частицы будут двигаться к противоположно заряженным электродам: коллоидная частица с адсорбированными на ней противоионами – в одну сторону, противоионы диффузного слоя – в другую. Сила, с которой электрическое поле действует на частицы и, следовательно, скорость движения частиц, очевидно, будет пропорциональна ζ-потенциалу. Движение частиц дисперсной фазы в электрическом поле называется электрофорезом. Явление электрофореза можно наблюдать, поместив в U-образную трубку какой-либо окрашенный золь, поверх которого налит не смешивающийся с золем бесцветный электролит. Если опустить в электролит электроды и наложить разность потенциалов, то граница окрашенного золя в одном из колен трубки будет подниматься, в другом – опускаться (рис. 4.13). Если поместить в U-образную трубку пористую перегородку (например, мелкий кварцевый песок) и заполнить её водой, то при наложении разности потенциалов в одном колене будет наблюдаться подъем уровня жидкости, в другом – его опускание (рис. 4.14). Движение дисперсной среды в электрическом поле относительно неподвижной дисперсной фазы (в рассмотренном случае – относительно поверхности пористых тел) называется электроосмосом. Явления электрофореза и электроосмоса получили общее название электрокинетических явлений.
Скорость движения частиц дисперсной фазы при электрофорезе, а также скорость движения дисперсной среды при электроосмосе прямо пропорциональны напряженности электрического поля E и диэлектрической проницаемости дисперсионной среды ε и обратно пропорциональны вязкости среды η. Скорость движения частиц дисперсной фазы при электрофорезе U связана с величиной ζ-потенциала уравнением Гельмгольца-Смолуховского (К – постоянная, зависящая от формы частиц дисперсной фазы; для сферических частиц К = 6):
Обратные электрофорезу и электроосмосу электрокинетические явления (т.н. электрокинетические явления второго рода) называются соответственно потенциал седиментации и потенциал протекания. Потенциал седиментации (эффект Дорна) – возникновение разности потенциалов при вынужденном движении дисперсной фазы относительно неподвижной дисперсионной среды (например, под действием силы тяжести). Потенциал протекания (эффект Квинке) есть явление возникновения разности потенциалов при движении дисперсионной среды относительно неподвижной дисперсной фазы (например, при продавливании электролита через пористое тело). 28. Состояние воды и гидрофобные взаимодействия. Так как большинство белков функционирует в водной среде, то взаимодействие составляющих их мономеров с водой определяет пространственную конформацию макромолекулы белка в целом. Рассмотрим свойства воды более подробно. Молекула воды является диполем из-за своей асимметрии. В водном растворе атом О2 располагается как бы в центре тетраэдра, в двух вершинах которого находятся атомы Н.
Рис. 3.2. Тетраэдрические свойства полностью координированной воды. Две пары электронов кислорода, не участвующие в образовании валентной связи, находятся на вытянутых орбиталях, оси которых направлены к двум вершинам тетраэдра. Эти электронные пары несут отрицательный заряд и притягивают атомы водорода двух соседних молекул, то есть образуют водородные связи. Благодаря этим взаимодействиям в жидкой воде формируются ассоциации молекул, называемые кластерами. Структура кластеров сходна со структурой льда. Однако эта кристаллическая решетка отличается определенной "рыхлостью" (именно этим объясняется невысокая плотность льда). Вместе с тем, даже после полного таяния льда в жидкой фазе воды сохраняются льдоподобные структуры - кластеры (расчеты показывают, что если бы их не было, то плотность жидкой воды была бы =1.8 г/мл, вместо 1.0 г/мл). Наличие в воде кластеров подтверждается данными рентгенографических исследований. Между неструктурированной водой и кластерами постоянно осуществляется обмен молекулами, так что в среднем время жизни кластера составляет 10-10 с. При 20 оС в воде доля несвязанных в кластеры молекул составляет 29.5%. С увеличением температуры средний размер кластера уменьшается, и доля несвязанных молекул возрастает (именно плавлением кластеров объясняется аномально высокая теплоемкость воды). В воде хорошо растворяются такие органические соединения, которые содержат полярные группы и способны вступать в диполь-дипольное взаимодействие с молекулами воды или образовывать с ними водородные связи. Такими, в частности, являются группы:
Напротив, неполярные соединения плохо растворимы в воде. Физические причины этих явлений были выяснены после измерения термодинамических параметров процессов растворения. Было установлено, что в случае плохой растворимости углеводорода в воде изменение свободной энергии положительно, и, следовательно, энтропия системы уменьшается.
Что же означает уменьшение энтропии при растворении? Прямыми физическими исследованиями было показано, что при этом происходит увеличение доли кластеров. При растворении молекулы углеводов втискиваются в полости внутри тетраэдрических ячеек кластеров и вытесняют оттуда неструктурированную воду. Последняя образует новые кластеры, и упорядоченность системы увеличивается, а значит, энтропия уменьшается. Поэтому гидрофобные взаимодействия являются результатом свойств воды, а не каких-то особых сил, связывающих неполярные группы друг с другом. Таким образом, ассоциация неполярных молекул в воде за счет гидрофобных взаимодействий определяется выталкивающим действием воды на неполярные соединения, что обусловлено тенденцией молекул воды к достижению состояния максимальной неупорядоченности. 29. Потенциал действия (изменение электропроводной мембраны, потоки ионов натрия и калия, схема функционирования натриевого канала при возбуждении). Распространение возбуждения. В нервных волокнах сигналы передаются с помощью потенциалов действия, которые представляют собой быстрые изменения мембранного потенциала, быстро распространяющиеся вдоль мембраны нервного волокна. Каждый потенциал действия начинается со стремительного сдвига потенциала покоя от нормального отрицательного значения до положительной величины, затем он почти так же быстро возвращается к отрицательному потенциалу. При проведении нервного сигнала потенциал действия движется вдоль нервного волокна вплоть до его окончания. На рисунке показаны изменения, возникающие на мембране во время потенциала действия, с переносом положительных зарядов внутрь волокна вначале и возвращением положительных зарядов наружу в конце. В нижней части рисунка графически представлены последовательные изменения мембранного потенциала в течение нескольких 1/10000 сек, иллюстрирующие взрывное начало потенциала действия и почти столь же быстрое восстановление. Стадия покоя. Эта стадия представлена мембранным потенциалом покоя, который предшествует потенциалу действия. Мембрана во время этой стадии поляризована в связи с наличием отрицательного мембранного потенциала, равного -90 мВ. Фаза деполяризации. В это время мембрана внезапно становится высокопроницаемой для ионов натрия, позволяя огромному числу положительно заряженных ионов натрия диффундировать внутрь аксона. Нормальное поляризованное состояние в -90 мВ немедленно нейтрализуется поступающими внутрь положительно заряженными ионами натрия, в результате потенциал стремительно нарастает в положительном направлении. Этот процесс называют деполяризацией, В крупных нервных волокнах значительный избыток входящих внутрь положительных ионов натрия обычно приводит к тому, что мембранный потенциал «проскакивает» за пределы нулевого уровня, становясь слегка положительным. В некоторых более мелких волокнах, как и в большинстве нейронов центральной нервной системы, потенциал достигает нулевого уровня, не «перескакивая» его. Фаза реполяризации. В течение нескольких долей миллисекунды после резкого повышения проницаемости мембраны для ионов натрия, натриевые каналы начинают закрываться, а калиевые — открываться. В результате быстрая диффузия ионов калия наружу восстанавливает нормальный отрицательный мембранный потенциал покоя. Этот процесс называют реполя-ризацией мембраны.
Для более полного понимания факторов, являющихся причиной деполяризации и реполяризации, необходимо изучить особенности двух других типов транспортных каналов в мембране нервного волокна: электроуправляемых натриевых и калиевых каналов. Электроупавляемые натриевые и калиевые каналы. Необходимым участником процессов деполяризации и реполяризации во время развития потенциала действия в мембране нервного волокна является электроуправляемый натриевый канал. Электроуправляемый калиевый канал также играет важную роль в увеличении скорости реполяризации мембраны. Оба типа электроуправляемых каналов существуют дополнительно к Na+/K+ -насосу и каналам К*/Na+-утечки. Электроуправляемый натриевый канал. В верхней части рисунка показан электроуправляемый натриевый канал в трех различных состояниях. Этот канал имеет двое ворот: одни вблизи наружной части канала, которые называют активационными воротами, другие — у внутренней части канала, которые называют инактивационными воротами. В верхней левой части рисунка изображено состояние этих ворот в покое, когда мембранный потенциал покоя равен -90 мВ. В этих условиях активационные ворота закрыты и препятствуют поступлению ионов натрия внутрь волокна. Активация натриевого канала. Когда мембранный потенциал покоя смещается в направлении менее отрицательных значений, поднимаясь от -90 мВ в сторону нуля, на определенном уровне (обычно между -70 и -50 мВ) происходит внезапное конформационное изменение актива-ционных ворот, в результате они переходят в полностью открытое состояние. Это состояние называют активированным состоянием канала, при котором ионы натрия могут свободно входить через него внутрь волокна; при этом натриевая проницаемость мембраны возрастает в диапазоне от 500 до 5000 раз. Инактивация натриевого канала. В верхней правой части рисунке показано третье состояние натриевого канала. Увеличение потенциала, открывающее активационные ворота, закрывает инактивационные ворота. Однако инактивационные ворота закрываются в течение нескольких десятых долей миллисекунды после открытия активационных ворот. Это значит, что конформационное изменение, приводящее к закрытию инактивационных ворот, — процесс более медленный, чем конформационное изменение, открывающее активационные ворота. В результате через несколько десятых долей миллисекунды после открытия натриевого канала инактивационные ворота закрываются, и ионы натрия не могут более проникать внутрь волокна. С этого момента мембранный потенциал начинает возвращаться к уровню покоя, т.е. начинается процесс реполяризации. Существует другая важная характеристикая процесса инактивации натриевого канала: инактивационные ворота не открываются повторно до тех пор, пока мембранный потенциал не вернется к значению, равному или близкому к уровню исходного потенциала покоя. В связи с этим повторное открытие натриевых каналов обычно невозможно без предварительной реполяризации нервного волокна. 30. Роль гидрофобных взаимодействий в формировании структуры белков. Переход спираль-клубок. Переход глобула-клубок. Все аминокислотные остатки, входящие в состав полипептидной цепи условно разделяются на две группы: -неполярные (гидрофобные) -полярные (гидрофильные) Степень гидрофобности остатка определяют по разности свободных энергий растворения аминокислоты в слабополярном растворителе и воде (обычно используют этиловый спирт). Полученные таким образом величины разностей свободных энергий, приходящихся на белковую группу аминокислоты при переносе из спирта в воду, приведены в таблице:
Названия остатков: глицил, аланил, валил, лейцил, изолейцил (иле), фенилаланил (фен), пролил, тритофонил (три), серил (сер), треонил (тре), метионил (мет), аспарагинил (асп), глутаминил (глн), цистинил, аспаргил, глутамил (глу), тирозил, гистидил (гис), лизил (лиз), аргинил (арг). Гипотеза об определяющей роли гидрофобных взаимодействий была доказана в 1944 году. Идея состояла в том, что гибкая молекула белка в воде сворачивается в глобулу (поскольку полярные остатки белка стремятся к максимальному контакту с водным окружением, а неполярные - к минимальному контакту). Из геометрии известно, что минимальной поверхностью при заданном объеме обладает шар. Стремление неполярных остатков образовать внутри белковой части некое подобие шарообразной капли, а полярных - сосредоточиться на ее поверхности, и приводит к образованию компактного тела - глобулы с гидрофобным ядром и гидрофильной поверхностью.
1 - гидрофобное ядро 2 - гидрофильная оболочка В 1964 году Фишер установил, что, зная общее число аминокислотных остатков в ядре и отношение полярных остатков к неполярным, можно предсказать форму глобулы. Для простоты будем считать, что все остатки имеют одинаковые объемы. Найдем отношение числа полярных остатков к неполярным, которое обозначим bs. Будем считать, что радиус глобулы r0, и глобула покрыта мономолекулярным слоем полярных остатков толщиной d (Фишер считал, что d ~4-5A). При сделанных допущениях отношение числа полярных и неполярных остатков равно отношению объемов сферического слоя и центрального ядра:
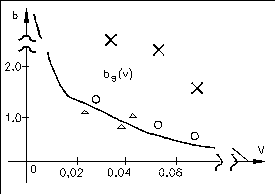
Следовательно, чем меньше r0 , тем больше должна быть относительная гидрофильность белка. На рисунке приведена теоретическая кривая (кривая Фишера) значений параметра b от объема глобулы (V=4/3r03), а также экспериментальные значения.
Глобула может быть сферической, строго говоря, лишь при b=bs (соответствует кривой Фишера на графике). Если b>bs, то есть число полярных остатков в белке больше, чем необходимо для того, чтобы покрыть гидрофобное ядро гидрофильным слоем, то глобула вытягивается в виде эллипсоида и имеет большую поверхность, чем в случае сферы.
b>>bs возникают фибриллярные структуры (обозначено x на графике) b<bs гидрофильные остатки не полностью закрывают гидрофобное ядро и гидрофобное взаимодействие между такими открытыми участками приводит к агрегации белков и возникновению надмолекулярных структур (обозначено на графике).
Таким образом, белки, для которых значения b лежат выше кривой Фишера, представляют собой эллипсоиды и фибриллы, значения лежат на кривой представляют собой глобулы. Под кривой располагаются белки, образующие надмолекулярную структуру. Формирование гидрофобного ядра в глобулярных белках имеет принципиальное значение для их функционирования. Белки при их огромной молекулярной массе обладают сравнительно компактной структурой прежде всего, благодаря гидрофобным взаимодействиям. линейные молекулы (нуклеиновые кислоты, полипептиды), претерпевающие переход спираль — клубок, разбиваются на чередующиеся спиральные и клубкообразные участки (рис. 3). Переход спираль — клубок в ДНК наблюдается при повышении температуры, добавлении в раствор кислоты или щёлочи, а также под влиянием других денатурирующих агентов. Этот переход в гомополинуклеотидах происходит при нагревании в интервале десятых долей °С, в фаговых и бактериальных ДНК — в интервале 3—5°С (рис. 3), в ДНК высших организмов — в интервале 10—15 °С. Чем выше гетерогенность ДНК, тем шире интервал перехода и меньше способность молекул ДНК к ренатурации. Переход спираль — клубок в различных видах РНК носит менее кооперативный характер (рис. 4) и происходит в более широком интервале температурных или других денатурирующих воздействий.
Переход клубок—глобула Как правило, в растворе гомополимера при ухудшении качества растворителя (обычно при понижении температуры) полимерная цепь испытывает переход клубок—глобула. Физически это происходит потому, что плохой растворитель соответствует притягивающему объемному взаимодействию звеньев. Сначала чуть ниже θ-температуры (на величину порядка N − 1 / 2, где N — степень полимеризации цепи, то есть количество звеньев в ней) клубок коллапсирует в рыхлую глобулу, близкую по размеру к клубку; при дальнейшем ухудшении качества растворителя глобула становится плотной. Фазовый переход клубок-глобула был феноменологически изучен П. Дж. Флори в 1949 году[1], часто используются модификации подхода Флори, предложенные Птицыным и Эйзнером, Бирштейн и Прямицыным (1986). Значительно более строгий, но сложный метод был предложен в 1979 году И. М. Лифшицем, А. Ю. Гросбергом и А. Р. Хохловым на основе подхода, представляющего конформационную энтропию цепи в виде функционала плотности (формула Лифшица)[2]. Одним из примеров глобулы могут служить белки. Однако они демонстрируют сложное поведение при денатурации-ренатурации: хотя некоторые из вышеназванных методов разрабатывались именно ввиду перехода нативная-денатурированная конформация в белках, они оказались неприменимыми к столь непростому объекту. 31. Транспорт неэлектролитов (проницаемость мембран для воды, роль коллоидно-осмотического давления плазмы в переносе воды).
1.2 Транспорт неэлектролитов путем простой и облегченной диффузии
Всякая живая клетка окружена мембраной, которая служит для защиты и регуляции внутренней среды. Мембрана действует как дискриминирующее устройство, позволяющее питательным и другим необходимым веществам входить внутрь клетки, а продуктам обмена удаляться наружу. Белки мембран выполняют функции трех типов: поддерживают общую структурную целостность мембран; действуют как ферменты, например, при синтезе молекул АТФ в митохондриальных мембранах или в различных стадиях фотосинтеза в мембране хлоропласта; кроме того, они служат переносчиками ионов и молекул через мембраны. Различные вещества переносятся через мембраны по двум основным механизмам: путем диффузии (пассивного транспорта) и путем активного транспорта. Проницаемость мембран для различных растворенных веществ зависит от размеров и заряда этих молекул. Поскольку внутренняя область мембран состоит из углеводородных цепей, многие малые нейтральные и неполярные молекулы могут проходить через бимолекулярную мембрану путем обычной диффузии. Иначе можно сказать, что эти молекулы растворимы в мембране. Наиболее важное из этих веществ – глюкоза, которая переносится через мембраны только в комплексе с молекулой-переносчиком. В этой роли обычно выступает белок. Комплекс глюкозы с переносчиком легко растворяется в мембране и может поэтому диффундировать через мембрану. Такой процесс называется облегченной диффузией. Суммарная скорость транспорта глюкозы резко повышается в присутствии гормона инсулина. Пока не совсем ясно, состоит ли действие инсулина в повышении концентрации переносчика или этот гормон стимулирует образование комплекса между глюкозой и переносчиком. Основным механизмом пассивного транспорта веществ, обусловленным наличием концентрационного градиента, является диффузия. Диффузия - это самопроизвольный процесс проникновения вещества из области большей в область меньшей его концентрации в результате теплового хаотического движения молекул. Математическое описание процесса диффузии дар Рик. Согласно закона Рика, скорость диффузии
Знак минус в правой части уравнения показывает, что диффузия происходит из области большей концентрации в область меньшей концентрации вещества. «D» называется коэффициентом диффузии. Коэффициент диффузии численно равен количеству вещества, диффундирующего в единицу времени через единицу площади при градиенте концентрации, равном единице. «D» зависит от природы вещества и от температуры. Он характеризует способность вещества к диффузии. Так как концентрационный градиент клеточной мембраны определить трудно, то для описания диффузии веществ через клеточные мембраны пользуются более простым уравнением, предложенным Коллеидером и Берлундом:
где С1 и С2 – концентрации вещества по разные стороны мембраны, Р - коэффициент проницаемости, аналогичный коэффициенту диффузии. В отличие от коэффициента диффузии, который зависит только от природы вещества и температуры, «Р» зависит еще и от свойств мембраны и от ее функционального состояния. Проникновение растворенных частиц, обладающих электрическим зарядом, через клеточную мембрану зависит не только от концентрационного градиента мембраны. В связи с этим перенос ионов может осуществляться в направлении, противоположном концентрационному градиенту, при наличии противоположно направленного электрического градиента. Совокупность концентрационного и электрического градиентов называется электрохимическим градиентом. Пассивный транспорт ионов через мембраны всегда происходит по электрохимическому градиенту. Основными градиентами, присущими живым организмам, являются концентрационные, осмотические, электрические и градиенты гидростатического давления жидкости. В соответствии с этим градиентом имеются следующие виды пассивного транспорта веществ в клетках и тканях: диффузия, осмос, электроосмос и аномальный осмос, фильтрация. Большое значение для жизнедеятельности клеток имеет явление сопряженного транспорта веществ и ионов, которое заключается в том, что перенос одного вещества (иона) против электрохимического потенциала («в гору») обусловлен одновременным переносом другого иона через мембрану в направлении снижения электрохимического потенциала («под гору»). Схематически это представлено на рисунке. Работу транспортных АТФ-аз и перенос протонов при работе дыхательной цепи митохондрий часто называют первичным активным транспортом, а сопряженный с ним перенос веществ – вторичным активным транспортом. 32. Электропроводность биосистем (закономерности происхождения постоянного тока через биологические объекты; явления поляризации). 33. Сокращение мышцы (схема взаимодействия актина и миозина по А.Хаксли). 34. Электропроводность биосистем (закономерности происхождения переменного тока через биологические объекты; дисперсия электропроводности). Переменный ток – это такой ток, направление и числовое значение которогоменяются с течением времени (знакопеременный ток).В медицинской практике применяются следующие виды токов по форме кривой тока:· Синусоидальный· Прямоугольный · Треугольный· Трапециевидный · Игольчато-экспоненциальныйСамым простым является периодический синусоидальный ток. Он легко описываетсяматематически и графически, форма его не искажается в электрических цепях сR, C, L элементами. При пропускании тока через живую ткань, её можно рассматривать какэлектрическую цепь, состоящую из определенных элементов.Экспериментально установлено, что это цепь обладает свойствами активногосопротивления и ёмкости. Это доказывается выделением тепла и уменьшениемполного сопротивления ткани с возрастанием частоты. Свойств индуктивности уживой ткани практически не обнаруживается. Таким образом, живая тканьпредставляет собой сложную, но не полную электрическую цепь.Импеданс живой ткани можно рассматривать как для последовательного, так и дляпараллельного соединения её элементов.При последовательном соединении токи через элементы равны, общее приложенноенапряжение будет векторной суммой напряжений на R и C элементах и формулаимпеданса последовательной цепи будет иметь вид: Z_ - импеданс последовательной цепи,R - её активное сопротивление,XC - ёмкостное сопротивление.При параллельном соединении напряжения на R и C элементах равны, общий токбудет векторной суммой токов каждого элемента, а фомула импеданса будетследующей: Z_ - импеданс последовательной цепи,R - её активное сопротивление,XC - ёмкостное сопротивление.При параллельном соединении напряжения на R и C элементах равны, общий токбудет векторной суммой токов каждого элемента, а фомула импеданса будетследующей: 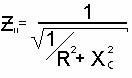 Теоретические формулы импеданса живой ткани при параллельном ипоследовательном соединении её элементов от экспериментальных отличаютсяследующим:1.При последовательной схеме соединения практические данные дают большиеотклонения на низких частотах.2.При параллельной схеме эти измерения показывают конечное значение Z, хотятеоретически оно должно стремиться к нулю. Эквивалентная электрическая схема живой ткани – э то условная модель,приближенно характеризующая живую ткань, как проводник переменного тока. Схема позволяет судить: 1.Какими электрическими элементами обладает ткань2.Как соединены эти элементы.3.Как будут меняться свойства ткани при изменении частоты тока. В основе схемы лежат три положения: 1.Внеклеточная среда и содержимое клетки есть ионные проводники с активнымсопротивлением среды Rср и клетки Rк.2.Клеточная мембрана есть диэлектрик, но не идеальный, а с небольшой ионнойпроводимостью, а, следовательно, и сопротивлением мембраны Rм.3.Внеклеточная среда и содержимое клетки, разделённые мембраной, являютсяконденсаторами См определенной ёмкости (0,1 – 3,0 мкФ/см2).Если в качестве модели живой ткани взять жидкую тканевую среду – кровь,содержащую только эритроциты, то при составлении эквивалентной схемы нужноучитывать пути электрического тока.Их два:1.В обход клетки, через внеклеточную среду.2.Через клетку.Путь в обход клетки представлен только сопротивлением средыRср.Путь через клетку сопротивлением содержимого клетки Rк, а такжесопротивлением и ёмкостью мембраны.Rм, См. Теоретические формулы импеданса живой ткани при параллельном ипоследовательном соединении её элементов от экспериментальных отличаютсяследующим:1.При последовательной схеме соединения практические данные дают большиеотклонения на низких частотах.2.При параллельной схеме эти измерения показывают конечное значение Z, хотятеоретически оно должно стремиться к нулю. Эквивалентная электрическая схема живой ткани – э то условная модель,приближенно характеризующая живую ткань, как проводник переменного тока. Схема позволяет судить: 1.Какими электрическими элементами обладает ткань2.Как соединены эти элементы.3.Как будут меняться свойства ткани при изменении частоты тока. В основе схемы лежат три положения: 1.Внеклеточная среда и содержимое клетки есть ионные проводники с активнымсопротивлением среды Rср и клетки Rк.2.Клеточная мембрана есть диэлектрик, но не идеальный, а с небольшой ионнойпроводимостью, а, следовательно, и сопротивлением мембраны Rм.3.Внеклеточная среда и содержимое клетки, разделённые мембраной, являютсяконденсаторами См определенной ёмкости (0,1 – 3,0 мкФ/см2).Если в качестве модели живой ткани взять жидкую тканевую среду – кровь,содержащую только эритроциты, то при составлении эквивалентной схемы нужноучитывать пути электрического тока.Их два:1.В обход клетки, через внеклеточную среду.2.Через клетку.Путь в обход клетки представлен только сопротивлением средыRср.Путь через клетку сопротивлением содержимого клетки Rк, а такжесопротивлением и ёмкостью мембраны.Rм, См.  Если заменить электрические характеристики соответствующими обозначениями, тополучим эквивалентные схемы разной степени точности: Если заменить электрические характеристики соответствующими обозначениями, тополучим эквивалентные схемы разной степени точности: 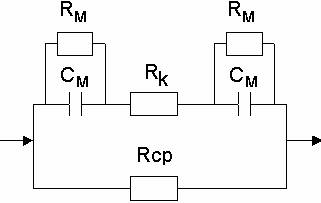  Схема Фрике (ионная проводимость неучитывается).Схема Швана (ионная проводимость учитывается в виде сопротивления мембраны) Обозначения на схеме: Rcp - активное сопротивление клеточной средыRk - Сопротивление клеточного содержимогоCm - ёмкость мембраныRm - сопротивление мембраны.Анализ схемы показывает, что при увеличении частоты тока проводимостьклеточных мембран увеличивается, а полное сопротивление тканевой средыуменьшается, что соответствует практически проведенным измерениям. 5. Живая ткань как проводник переменного электрического тока. Дисперсияэлектропроводности и её количественная оценка. Экспериментально установлены следующие особенности живой ткани как проводникапеременного ток:1. Сопротивление живой ткани переменном току меньше, чем постоянному.2. Электрические характеристики ткани зависят как от её вида, так и отчастоты тока.3. С увеличением частоты полное сопротивление живой ткани нелинейно уменьшаетсядо определенного значения, а затем остаётся практически постоянным (вбольшинстве на частотах свыше 106 Гц)4. На определенной частоте полное сопротивление зависит также отфизиологического состояния (кровенаполнения), что используется на практике.Исследование периферического кровообращения на основе измеренияэлектрического сопротивления называются реография (импедансплетизмография).5. При умирании живой ткани её сопротивление уменьшается и от частоты независит.6. При прохождении переменного тока через живые ткани наблюдается явление,которое называется дисперсией электропроводности. Схема Фрике (ионная проводимость неучитывается).Схема Швана (ионная проводимость учитывается в виде сопротивления мембраны) Обозначения на схеме: Rcp - активное сопротивление клеточной средыRk - Сопротивление клеточного содержимогоCm - ёмкость мембраныRm - сопротивление мембраны.Анализ схемы показывает, что при увеличении частоты тока проводимостьклеточных мембран увеличивается, а полное сопротивление тканевой средыуменьшается, что соответствует практически проведенным измерениям. 5. Живая ткань как проводник переменного электрического тока. Дисперсияэлектропроводности и её количественная оценка. Экспериментально установлены следующие особенности живой ткани как проводникапеременного ток:1. Сопротивление живой ткани переменном току меньше, чем постоянному.2. Электрические характеристики ткани зависят как от её вида, так и отчастоты тока.3. С увеличением частоты полное сопротивление живой ткани нелинейно уменьшаетсядо определенного значения, а затем остаётся практически постоянным (вбольшинстве на частотах свыше 106 Гц)4. На определенной частоте полное сопротивление зависит также отфизиологического состояния (кровенаполнения), что используется на практике.Исследование периферического кровообращения на основе измеренияэлектрического сопротивления называются реография (импедансплетизмография).5. При умирании живой ткани её сопротивление уменьшается и от частоты независит.6. При прохождении переменного тока через живые ткани наблюдается явление,которое называется дисперсией электропроводности.  Дисперсия электропроводности -это явление зависимости полного (удельного) сопротивления живой ткани отчастоты переменного тока.Графики такой зависимости называют дисперсионными кривыми. Дисперсионныекривые строят в прямоугольной системе координат, где по вертикали откладываютзначения полного (Z) или удельного сопротивления, а по горизонтали -частоту в логарифмическом масштабе (Lg n).Частотные зависимости по форме кривой для разных тканей сходный, ноотличается значением сопротивления.Имеется несколько диапазонов частот, на которых дисперсия особенно выражена.Один из них соответствует интервалу 102 -106 Гц Особенности дисперсии: 1. Присуща только живым тканям.2. Более выражена на частотах до 1 МГц.3. На практике используется для оценки физиологического состояния ижизнеспособности тканей.Количественно оценка дисперсии проводиться по коэффициенту дисперсии (К).Коэффициент дисперсии это безразмерная величина, равная отношениюнизкочастотного (102) полного (или удельного) сопротивления квысокочастотному (106 Гц). Дисперсия электропроводности -это явление зависимости полного (удельного) сопротивления живой ткани отчастоты переменного тока.Графики такой зависимости называют дисперсионными кривыми. Дисперсионныекривые строят в прямоугольной системе координат, где по вертикали откладываютзначения полного (Z) или удельного сопротивления, а по горизонтали -частоту в логарифмическом масштабе (Lg n).Частотные зависимости по форме кривой для разных тканей сходный, ноотличается значением сопротивления.Имеется несколько диапазонов частот, на которых дисперсия особенно выражена.Один из них соответствует интервалу 102 -106 Гц Особенности дисперсии: 1. Присуща только живым тканям.2. Более выражена на частотах до 1 МГц.3. На практике используется для оценки физиологического состояния ижизнеспособности тканей.Количественно оценка дисперсии проводиться по коэффициенту дисперсии (К).Коэффициент дисперсии это безразмерная величина, равная отношениюнизкочастотного (102) полного (или удельного) сопротивления квысокочастотному (106 Гц).  Z1 – полное сопротивление на частоте 102 ГцZ2 – полное сопротивление на частоте 106 Гцr1, r2 - удельное сопротивление на этих частотахЗначение коэффициента дисперсии зависит от вида ткани, её физиологическогосостояния, эволюционной стадии развития животного. Например, для печениживотного К = 9 -10 единиц, а для печени лягушки 2 -3 единицы. При умиранииткани коэффициент дисперсии стремиться к единице.Явление дисперсии связывают с наличием в живых тканях поляризации, которая сувеличением частоты меньше влияет на полное сопротивление. Поэтомукоэффициент дисперсии часто называют коэффициентом поляризации.Кроме частотных зависимостей в живых тканях отмечаются фазовые сдвиги междутоком и напряжением, которые тоже, но в меньшей степени, зависят от частоты.Фазовые сдвиги тоже уменьшаются при умирании тканей и, в перспективе, могутбыть использованы для практических целей. Z1 – полное сопротивление на частоте 102 ГцZ2 – полное сопротивление на частоте 106 Гцr1, r2 - удельное сопротивление на этих частотахЗначение коэффициента дисперсии зависит от вида ткани, её физиологическогосостояния, эволюционной стадии развития животного. Например, для печениживотного К = 9 -10 единиц, а для печени лягушки 2 -3 единицы. При умиранииткани коэффициент дисперсии стремиться к единице.Явление дисперсии связывают с наличием в живых тканях поляризации, которая сувеличением частоты меньше влияет на полное сопротивление. Поэтомукоэффициент дисперсии часто называют коэффициентом поляризации.Кроме частотных зависимостей в живых тканях отмечаются фазовые сдвиги междутоком и напряжением, которые тоже, но в меньшей степени, зависят от частоты.Фазовые сдвиги тоже уменьшаются при умирании тканей и, в перспективе, могутбыть использованы для практических целей.
35. Химия и физика мышцы (схема взаимодействия актина с миозином по Хаксли, кривая зависимости скорости изотонического сокращения от величины нагрузки по Хиллу). Сократительные белки актин и миозин образуют в миофибриллах тонкие и толстые миофиламенты. Они располагаются параллельно друг другу внутри мышечной клетки, как показано на рис. 4.1–схеме крошечного участка мышечного волокна человека. На ней изображены также одна из митохондрий (саркосом), лежащая между миофибриллами, и часть системы поперечных и продольных трубочек (их функции рассмотрены в разд. 4.2). Миофибриллы представляют собой сократимые пучки «нитей» (филаментов) диаметром около 1 мкм. Перегородки, называемые Z–пластинками, разделяют их на несколько компартментов–саркомеров длиной примерно по 2,5 мкм. Структура саркомеров схематически показана на рис. 4.1. С помощью светового микроскопа в них можно видеть регулярно чередующиеся поперечные светлые и темные полосы. Согласно теории Хаксли и Хансон [II], такая поперечная полосатость миофибрилл обусловлена особым взаиморасположением актиновых и миозиновых филаментов. Середину каждого саркомера занимают несколько тысяч «толстых» нитей миозина диаметром примерно по 10 нм. На обоих концах саркомера находятся около 2000 «тонких» (толщиной по 5 нм) нитей актина, прикрепленных к Z–пластинкам наподобие щетинок в щетке. Пучок лежащих в определенном по
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 880; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.57 (0.019 с.) |




 (IV.20)
(IV.20)
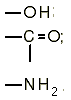


 F кДж/моль
F кДж/моль





 прямо пропорциональна градиенту концентрации
прямо пропорциональна градиенту концентрации 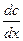 и площади S, через которую осуществляется диффузия:
и площади S, через которую осуществляется диффузия:




