
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ферменты,понятие. Сходства в действии ферментов и неорганических катализаторов. Общие свойства ферментов.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Ферменты,понятие. Сходства в действии ферментов и неорганических катализаторов. Общие свойства ферментов. Ферменты-это биологические катализаторы белковой природы,ускоряющие биохимические реакции в животных организмах. Сходства: 1) фермент и неорганический катализатор снижают энергию активации; 2)фермент и неорг. кат. ускоряют только энергетически возможные реакции; 3)фер. и неорг.кат. не изменяют направление реакции, не нарушают равновесия обратимой реакции,а только ускоряют наступление равновесия; 4)фер. и неорг.кат. не расходуются в процессе реакции и не входят в состав конечных продуктов реакции. Общие свойства: Общие свойства ферментов одновременно являются и отличием ферментов от неор.кат.: · Ферменты имеют белковую природу, поэтому обладают свойствами, характерными для белков; · Ферменты имеют сложное строение; · Ферменты обладают высокой специфичностью, как субстратной,так и специфичностью действия; · Ферменты имеют высокую биологическую активность, что обусловлено высоким сродством фермента к субстрату, и они гораздо сильнее снижают энергию активации. Ед.измерения активности фермента- катал; · Ферменты действуют в мягких условиях(при T-37-45,давлении 1 атм.); · Ферменты- это катализаторы с регулируемой активностью. Химическая природа ферментов По строению различают ферменты-протеины, однокомпонентные и ферменты- протеиды, двухкомпонентные. К группе ферментов-протеинов относят ферменты, построенные по типу простых белков, в отличие от которых фермент имеет активный центр. Наличие в их молекуле активного центра обеспечивает каталитическую активность фермента. К однокомпонентным ферментам относятся почти все ферменты желудочно-кишечного тракта. Ферменты- протеиды - двухкомпонентные(холоферменты)-сложные белки. Состоят из белковой части(апофермент) и вещества небелковой части(кофермент). У некоторых ферментов апофермент и кофермент соединены так прочно, что при разрыве это связи фермент разрушается. Но есть ферменты, у которых связь непрочная. Роль апофермента и кофермента различна. Белковая часть обуславливает субстратную специфичность фермента, а кофермент, входя в состав каталитического центра фермента, обеспечивает специфичность действия фермента, тип реакции, который ведет фермент. Роль коферментов выполняют производные различный витаминов, металлы(железо, медь). Строение активного центра фермента, его роль. Активный центр-это совокупность функциональных групп аминокислотных остатков, расположенных на поверхности ферментов и строго ориентированных в пространстве за счет третичной и иногда четвертичной структуры ферментов. Акт.центр имеет 2 участка: а) субстратный(контактный или якорная площадка), обуславливающий субстратную специфичность фермента и обеспечивающий его взаимодействие с субстратом; б) каталитический центр, ответственный за химические преобразования субстрата, который обуславливает специфичность действия фермента. Активный центр имеет форму узкого углубления или щели. В этом углублении присутствует несколько полярных аминокислотных остатков для связывания или катализа. Актив центры, занимают небольшую часть молекулы фермента. Остальная часть фермента сохраняет актив. Центр от разрушения. Первоначальная модель акт.центра, предложенная Э.Фишером, трактовала взаимодействие субстрата и фермента по аналогии с системой КЛЮЧ-ЗАМОК, те считалось, что между активным центром фермента и субстратом должно иметься полное соответствие. Эта модель, которую иногда называли модель ЖЕСТКОЙ МАТРИЦЫ. В настоящее время считают, что полного соответствия между субстратом и ферментом нет, оно возникает в процессе взаимодействия субстрата и фермента(теория Кошленда или теория индуцированного соответствия). Что такое аллостерический центр ферментов, его роль? У некоторых ферментов имеется так называемый аллостерический центр, участвующий в регуляции активности активного центра. Единого мнения о местонахождении этого центра нет. По некоторым данным аллост.центр располагается неподалеку от активного центра. При действии аллостерических эффекторов на этот центр происходят конформационные изменения молекулы фермента, в том числе изменяется и топография активного центра, в результате чего повышается или уменьшается структурное сродство фермента к субстрату. Аллост. центр характерен только для ферментов, имеющих несколько субъединиц. Механизм действия ферментов В механизме ферментативного катализа различают 3 стадии: 1.Образование фермент-субстратного комплекса. Субстрат присоединяется к участку молекулы фермента, который называется активным центром, в нем различают якорные участки. Соединение идет за счет связей, характер которых зависит от химической природы субстрата. Н-р, если в молекуле субстрата имеются заряженные группы, то образование комплекса возможно за счет электростатического взаимодействия. Место, куда прикрепляется субстрат находится на поверхности молекулы фермента. Таких участков может быть 2-3, они находятся на определенном расстоянии друг от друга. 2.Образование комплекса фермент - продукты реакции. Функционально активные группы активного центра фермента действуют на субстрат, дестабилизируя связи. При таком взаимодействии изменяется конфигурация субстрата, происходит его деформация, поляризация молекулы субстрата, растяжение связи между отдельными участками субстрата, перераспределение электронов, что приводит к изменению расположения электрического заряда, к снижению энергии активации, и субстрат распадается. 3.Распад комплекса фермент – продукты реакции с выделением свободного фермента. Третья стадия более медленная и от нее зависит скорость все реакции. Выявлено, что в механизме действия ферментов большое значение имеет изменение структуры субстрата, приводящее к снижению энергии активации. Величина энергии активации у различных субстратов разные. 6. Специфичность ферментов: а)субстратная, б) специфичность действия. Ферменты обладают специфичностью, т.е. избирательно действовать на определенный субстрат (субстратная специфичность) и ускорять определенную химическую реакцию (специфичность действия), т.е. специфичность действия – это способность ферментов производить с субстратом лишь одно из возможных химических превращений. Ферменты могут воздействовать на несколько субстратов, но при этом катализировать только одну определенную реакцию. Субстратная специфичность: если фермент катализирует превращение только одного субстрата, то специфичность абсолютная (аргиназа расщепляет аргинин). Если фермент катализирует превращение группы субстратов, объединенных одним типом связи, то такая специфичность называется относительной (пепсин расщепляет жиры и живот. и раст. происхождения). Стереохимическая специфичность обусловлена существованием оптических изомеров L- и D- форм или геометрических изомеров хим. веществ. Так фермент может действовать только на один из изомеров(фумараза катализирует превращение только фумаровой кислоты, но не действует на малеиновую кислоту) 7. Мощность действия ферментов. Большинство реакций, катализируемых ферментами, протекают в 10-100 раз быстрее, чем некатализируемые реакции. Для характеристики мощности действия ферментов введено понятие катал – число молекул субстрата, подвергающееся воздействию одной молекулы фермента в течение 1 минуты. Мощность большинства ферментов равна 1000 каталов, мощность действия каталазы – 1.000.000 каталов, амилазы – 240.000, а ацетилхолинэстеразы – более 1.000.000 каталов. Высокая мощность действия ферментов обуславливает высокую скорость химических процессов в организме. 8. Изоферменты, их диагностическое значение. Изоферменты – молекулярные формы ферментов, катализирующие одну и ту же реакцию с одним и тем же субстратом, но в различных условиях. Они различаются по строению апофермента, по физико-химическим свойствам, по сродству апофермента к субстрату. Коферменты изоферментов одинаковые, поэтому биологическое действие изоферментов одинаково. Клетки и органы различаются по содержанию тех или иных изоферментов, т.е. изоферменты обладают органотропностью. Это имеет большое диагностическое значение, так как при поражении того или иного органа в кровь выходят преимущественно определенные изоферменты, что позволяет провести органную диагностику. Н-р, лактатдегидрогиназа(ЛДГ), ускоряющая реакцию дегидрирования молочной кислоты, имеет 5 изоферментов с одинаковым коферментом – НАД. В состав апофермента ЛДГ входят 4 полипептидные цепи. Различают Н-цепи (сердце) и М-цепи(мышцы). ЛДГ1 – 4 цепи Н-типа, в сердце ЛДГ2 – 3 цепи Н-типа и 1 цепь М-типа, в сердце, почках ЛДГ3 – 2 цепи Н-типа и 2 цепи М-типа, в легких ЛДГ4 – 1 цепь Н-типа и 3 цепи М-типа, в печени ЛДГ5 – 4 цепи М-типа, в мышцах и печени.
Декарбоксилазы аминокислот По химической природе декарбоксилазы аминокислот – это сложные ферменты, коферментами которых могут являться фосфопиридоксаль(вит В6 связанный с фосф.к-той)
Подкласс-гидролиазы Представитель-карбангидраза- двухкомпонентный фермент, кофермент окончательно не изучен, но известно, что в его состав входит цинк. Фермент ускоряет обратимую реакцию синтеза и распада угольной кислоты Н2О + CO2 = H2CO3 Направление реакции зависит от концентрации СО2, поэтому фермент вызывает удаление избытка угольной кислоты и играет роль в регуляции дыхательного центра.
Декарбоксилазы аминокислот декарбоксилазы аминокислот- чаще всего бактериального происхождения, играют важную роль при бактериальных инфекциях и в процессе гниения. Набольшое кол-во встречается и в животных тканях, гфе они принимают участие в обмене некоторых аминокислот, способствую образования биогенных аминов(вещества, образующиеся в организме животных или растений из аминокислот при их декарбоксилировании ферментами декарбоксилазами и обладающие высокой биологической активностью.). По строению это двухкомп. Ферменты, коф-т – фосфопиридоксаль (витамин В6 с H3PO4).
Карбоангидраза. Карбоангидраза или угольная ангидраза - представитель подкласса гидро-лиазы. Двухкомп. фермент, сост из апофермента и кофермента, в состав кофермента входят ионы цинка. Катализирует р-ю распада и синтеза угольной к-ты. Сод-ся в эритроцитах и играет роль в процессах переноса СО2 от тканей к легким. Н2О + СО2 ↔ Н2СО3 Направление реакции зависит от конц-ии СО2. Имеет значение в удалении избытка угольной к-ты(СО2) и играет роль в регуляции дыхательного центра. 36 Оксирезуктазы. Классификация. Это большой класс ферментов, которые катализируют окислительно-восстановительные реакции (реакции отщепления или присоединения водорода или электронов). По химической природе двухкомпонентны, содержатся в клетках. Различают около 90 подклассов. Для удобства изложения и усвоения этого материала по способу окисления можно разделить на 4 группы: 1) дегидролазы (Представители: 1)пиридинферменты; 2) флавинферменты) Цитохромы, Каталаза и пероксидаза, Гидрооксилазы и оксигеназы Дегидрогеназы, предтавители К дегидрогеназам относятся ферменты, осуществляющие окисление веществ путем их дегидрирования (отнятия водорода), участвуя в БО и восстановлении, т.е. в реакциях, связанных с процессами тканевого дыхания, гликолиза, брожения. Известно свыше 150 ДГ-аз. Представители: 1)пиридинферменты; 2) флавинферменты Представители. 1. Реакции ЦТК Пункты сопряжения БО и ОФ БО имеет 3 пункта,в которых выделяется энергия,достаточная для образования АТФ. Эти пункты называются пунктами сопряжения БО и ОФ,это 2(когда НАДН2 окисляется ФФ),6(Цхв окисляется,ЦХс1 восстанавливается),9 и 10(в ЦХО,Цха окисляется,ЦХа3 восстанавливается) Разобщение БО и ОФ Главная суть в том, что они разрывают связь между БО и ОФ, то есть 3 и 4 стадией энерг. Обмена. А. 2.4 динитрофенол (принимался против ожирения) Б. Дикумарол – применяется как антикогулянт в клинич. Практике. В. Транспорт Са в митохондрии. Не происходит сохранение АТФ и АТФ тратится на захват кальция. Ферментные ансамбли. Мембранносвязанные ферменты, участвующие в БО в митохондриях, расположены не линейно, а обьеденены в комплекса: 1. Комплекс ФП(ФМН) 2. ФП(ФАД) 3. Цх b, c1 4. Цх а, а3
Оксидазное окисление. ПФ и ФП окисляют субстраты перенося водород, на убихиноне они распадаются на протоны и электроны. Далее электроны транспортируются различными цитохромами, передаваясь на кислород, ионизируя его. Ион кислорода, соедин. С протонами водорода, образует эндогенную воду. В процессе БО выделяется энергия, идущая на образование АТФ 40% и тепла 60% ½ О2 + 2Н+ = энергия + Н2О 61. Оксигеназное окисление, значение, ферменты, конечные продукты. Больше половины оставшегося кислорода используется на оксигеназный тип окисления, который идет по 2 путям – монооксигеназному и диоксигеназному. Монооксигеназный путь происходит в митохондриях и микросомах. В митохондриях происходит гидроксилирование (при участии НАДФН2, ЦхР450). При гидроксилировании образуется окисленный продукт, вода и НАДФ.
62. Пероксидазное окисление. Пероксидазное окисление - побочный путь окисления, обычно наблюдается при выходе из строя цитохромной системы или когда субстрат не окисляется другим путем, например, мочевая кислота. Протекает с участием ферментов оксидаз, наиболее активных в пероксисомах. Пероксисомы – микротельца, обнаруженные в гепотоцитах; окислительные органеллы. Эти микротельца содержат оксидазу мочевой кислоты, оксидазу Д-аминокислот, а также каталазу, которая расщепляет пероксид водорода. Например: Ксантин + Н2О2 + О2 = (фермент ксантиноксидаза) получается молочная кислота + Н2О2; 2 % кислорода в организме идет на окисление восстановленных ФП(ФАД) с образованием перекиси водорода ФПН2 + О2 = ФП + Н2О2(фермент Каталаза) Н2О2 = Н2О + О2 (фермент каталаза) 63. Пероксидное окисление. Образование АФК. Пероксидный тип окисления или перекисный, или свободно-радикальный — происходит при одноэлектронном восстановлении О2. Этому типу окисления подвергаются ПНЖК в составе ФЛ мембран. ПОЛ инициируется под действием АФК.АФК делятся на 2 группы: 1 группа – свободные радикалы: супероксиданион радикал, гидроксипероксирадикал (НОО•), гидроксильный радикал, радикал оксида азота, алкилоксирадикал (LO•), липопероксирадикал (LOO•) 2 группа – нерадикальные вещества: гипохлорит-анион, перекись водорода, синглетный кислород (1О2), озон (О3), железокислородный комплекс (Fe++—О2) и ГПЛ (LOOH). АФК в больших количествах опасны для клеток. Так, супероксиданион может вызвать деполимеризацию ГАГ, окисление адреналина и тиолов. Перекись водорода токсична, хотя механизм токсичности не ясен. Известно, что избыток перекиси водорода вызывает окисление тиогрупп белков, может приводить к образованию гидроксильного радикала. Главная опасность АФК – инициация ПОЛ. Свободно-радикальное окисление (СРО) носит цепной характер: ПНЖК - ДК - ГПЛ - МДА (малоновый диальдегид) диеновые конъюгаты гидропероксиды липидов ПОЛ – главный путь использования ПНЖК. Продукты ПОЛ необходимы при синтезе некоторых гормонов и белков (например, в синтезе тироидных гормонов), образования простагландинов (ПРГ), для функционирования фагоцитов, для регуляции проницаемости и состава липидов мембран, скорости пролиферации клеток и их секреторной функции. Однако следует учесть, что увеличение скорости ПОЛ и концентрации продуктов ПОЛ приводит к повреждению клетки и ее смерти, например, продукты ПОЛ, являясь высокотоксичными повреждают ДНК и РНК, вызывают мутации. Продукты ПОЛ вызывают денатурацию белков, разобщают БО и ОФ, нарушают структуру мембран. 64. Антиоксиданты ферментные и неферментные Скорость ПОЛ контролируется АОС. АОС подразделяется на ферментную и неферментную. К первой относятся: 1)СОД (Супероксиддисмутаза), которая переводит супероксидный радикал в менее токсичную перекись водорода2О2 + 2Н+ = Н2О2 +О2 2)Каталаза, которая разрушает пероксид водорода до воды и молеклярного кислорода; 3) Глутатионпероксидаза (ГПО)окисляет гидрокперекись липидов до легкоокисляемых ЖК 4) Глутатионредуктаза(ГР), восстанавливающая окисленный глутатион. К неферментной АОС относятся жирорастворимые витамины, каротиноиды, витамин С, витамин Р, витамин В2, карнозин (нейтрализует гидроксильный радикал), ферритин (связывает двухвалентное железо, которое является источником электронов для образования АФК), церулоплазмин (связывает двухвалентную медь, что уменьшает возможность ее окисления и образования супероксиданион-радикала, а также окисляет двухвалентное железо, выполняя роль феррооксидазы), металлотионеины (связывают медь и другие металлы, выполняя не только антиоксидантную функцию, но и антитоксическую), таурин (нейтрализует гипохлорит-анион). Пункты сопряжения БО и ОФ К ним относятся пункты под № 2,6,9,10
9-10) очень тесно объединены м.у собой, т.к происходят в мультиферментном комплексе - цитохромоксидазе. 2 ферро Цха(Fe2+)передают 2e 2ферриЦха3 (Fe3+). Цха(Fe2+)-окисляется, Цха3(Fe3+)- восстанавливается Разобщение БО и ОФ Некоторые липофильные вещества (2,4-динитрофенол, некоторые лекарства, жирные кислоты) могут переносить ионы водорода через внутреннюю мембрану митохондрий в матрикс, минуя канал АТФ-синтазы. В результате этого снижается протонный градиент и прекращается синтез АТФ. Это явление называется разобщением, а вещества - разобщителями дыхания и фосфорилирования. Прототипы разобщителей ОФ • 2,4 –динитрофенол – классический разобщитель ОФ. Токсичен, но одно время использовался как лекарство от ожирения. • Дикумарол – обладает аналогичным действие и используется как антикоагулянт • Транспорт Ca2+ в митохондрии также изменяет взаимоотношения между электронным транспортом и ОФ. Ферментные ансамбли Мембранносвязанные ферменты, участвующие в БО в митохондриях, расположены не линейно, а объединены в 4 комплекса: 1 комплекс ФП(ФМН), 2 комплекс ФП(ФАД), 3 комплекс Цхв и Цхс1, 4 – Цха и Цха3
Ферменты,понятие. Сходства в действии ферментов и неорганических катализаторов. Общие свойства ферментов. Ферменты-это биологические катализаторы белковой природы,ускоряющие биохимические реакции в животных организмах. Сходства: 1) фермент и неорганический катализатор снижают энергию активации; 2)фермент и неорг. кат. ускоряют только энергетически возможные реакции; 3)фер. и неорг.кат. не изменяют направление реакции, не нарушают равновесия обратимой реакции,а только ускоряют наступление равновесия; 4)фер. и неорг.кат. не расходуются в процессе реакции и не входят в состав конечных продуктов реакции. Общие свойства: Общие свойства ферментов одновременно являются и отличием ферментов от неор.кат.: · Ферменты имеют белковую природу, поэтому обладают свойствами, характерными для белков; · Ферменты имеют сложное строение; · Ферменты обладают высокой специфичностью, как субстратной,так и специфичностью действия; · Ферменты имеют высокую биологическую активность, что обусловлено высоким сродством фермента к субстрату, и они гораздо сильнее снижают энергию активации. Ед.измерения активности фермента- катал; · Ферменты действуют в мягких условиях(при T-37-45,давлении 1 атм.); · Ферменты- это катализаторы с регулируемой активностью.
|
||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 2560; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.219.186.229 (0.012 с.) |

 и пирролохинолинохинон (PQQ). ДК аминокислот являются ферментами бактерий, например, в толстом отделе кишечника у животных и человека. Эти ферменты в толстом кишечнике вызывают гниение белков, декарбоксилируя аминокислоты. В клетках человека и животных ДК аминокислот мало. Декарбоксилирование аминокислот также происходит при разложении трупа, когда под действием катепсинов белки тканей распадаются до аминокислот, а ДК аминокислот проводят дальнейшие изменения их
и пирролохинолинохинон (PQQ). ДК аминокислот являются ферментами бактерий, например, в толстом отделе кишечника у животных и человека. Эти ферменты в толстом кишечнике вызывают гниение белков, декарбоксилируя аминокислоты. В клетках человека и животных ДК аминокислот мало. Декарбоксилирование аминокислот также происходит при разложении трупа, когда под действием катепсинов белки тканей распадаются до аминокислот, а ДК аминокислот проводят дальнейшие изменения их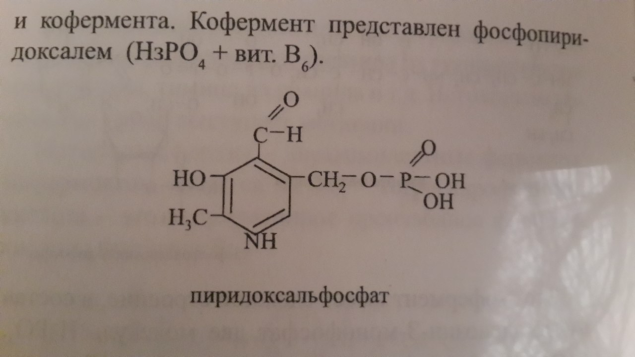
 При диоксигеназном пути оксигеназного типа под влиянием оксигеназ происходит включение обоих атомов кислорода в субстрат. Обычно это происходит с веществами, имеющими ненасыщенные связи по месту их разрыва, например, ненасыщенные ЖК.
При диоксигеназном пути оксигеназного типа под влиянием оксигеназ происходит включение обоих атомов кислорода в субстрат. Обычно это происходит с веществами, имеющими ненасыщенные связи по месту их разрыва, например, ненасыщенные ЖК.
 2) 2 пункт - НАДН2 окисляется ФП. Теряя водороды НАДН2 окисляется, а флавопротеиды, присоединяя водороды восстанавливается
2) 2 пункт - НАДН2 окисляется ФП. Теряя водороды НАДН2 окисляется, а флавопротеиды, присоединяя водороды восстанавливается 6) 6 пункт - Происходит ОВР между ферроЦхЬ(окисляется) и ферриЦхс1(восстанавливается).
6) 6 пункт - Происходит ОВР между ферроЦхЬ(окисляется) и ферриЦхс1(восстанавливается).


