
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Молекулярно - абсорбціоний аналіз.Содержание книги
Поиск на нашем сайте Цей вид аналіза оснований на поглинанні світла визначаємою речовиною якщо промениста енергія, тобто випромінювання, поглинається молекулами визначаємої речовини, то ці молекули переходять з одного стану з меншою енергією в інший стан з більшою енергією. Якщо при цьому в молекулі змінюється енергія руху електронів, то спостерігаємий спектр називається електронним. Він лежить у видимій та ультрофіолетовій областях спектра. До молекулярно - абсорбціоного анализу відносяться: колориметричний, фотоколориметричний та спектрофотометричний методи аналіза. Колориметричний метод аналізу основується на порівнянні інтенсивності забарвлення досліджуємого розчину з забарвленням стандартного розчину, концентрація якого точно відома. Інтенсивність поглинання світла залежить від присутності у розчині забарвлених молекул та іонів, які поглинають світло у значно більшій ступені, чим розчинник, т. ч. залежить від концентрації розчину. Фотоколориметричний метод аналізу основується на вимірюванні інтенсивності поглинання світла розчином і фактично представляє собою абсорбціометрію, т.ч. аналіз по світопоглинанню. Ступень поглинання світла, який використовує розчин вимірюють за допомогою фотоелементів, а використовуємі прибори називаються фотоелектроколориметрами (ФЭК). Спектрофотометричний метод аналізу також оснований на вимірюванні поглинання розчином випромінювання, но не поліхроматичного, а монохроматичного, як у видимій, так і в ультрофіолетовій та інфрчервоній областях спектра. Прибори, які використовують в спектрофотометрії, називають спектрофотометрами. Видиме випромінювання (або світло) - це випромінювання, яке визиває зорові відчуття. Випромінювання, яке не визиває зорового відчуття, називають невидимим випромінюванням. Головними оптичними характеристиками всіх забарвлених розчинів є: колір та інтенсивність його забарвлення. 1. Колір розчину. Всі забарвлені речовини характеризуються вибірковим поглинанням світла. Це значить, що забарвлення розчину зумовлене нерівномірним поглинанням окремих ділянок видимого випромінювання. Наприклад, розчин мідного купоросу синього кольору тому, що іони міді переважно (вибірково) поглинають жовту область спектру, а остальні області пропускають. Розчин, який поглинає синю область, буде здаватися жовтим, поглинаюча зелена ділянка спектра – пурпурний і т.п.. Таким чином, спостерігає мий колір розчину завжди є додатковим до кольору поглинаючого випромінювання. Речовина «білого» кольору тому, що вона видиме випромінювання не поглинає, а відбражає. Речовини «чорного» кольору тому, що рівномірно поглинає видимее випромінювання. Для повної характеристики розчинів забарвлених сполук використовують спектри (криві світопоглинання), які показують залежність значення оптичної густини від довжини хвилі випромінювання. Спектри поглинання будуєть у координатах: А – оптична густина (характеризує ступінь поглинання світла), l - довжина хвилі поглинаючого випромінювання (км). Довжина хвилі, яка відповідає максимуму світопоглинання (lmax), є важливою оптичною характеристикою речовини, а саме кольору розчину. Для збільшення чутливості та правильності фотометричних визначень слід використовувати при освітленні розчину не поліхроматичне випромінювання (білий світ), а деякою більш вузькою ділянкою спектра, яка найбільш сильно поглинає дану речовину. Для того, щоб виділити таку ділянку спектра, звичайно використовують світофільтри, а в особливих випадках - монохроматори, які виділяють монохроматичне випромінювання. 2. Інтенсивність забарвлення. Два розчини з однієї ж речовини, але з різними концентраціями однокового кольору, но відмінні по інтенсивності забарвлення. Кількість інтенсивності забарвлення розчину значенням оптичної густини. Під оптичною густиною розуміють величину поглинання світового потоку, який пройшов крізь розчин та позначається буквою ”A” (в підручниках, давнішого видання, позначається буквою “Д”). Основним законом світопоглинання є об’єднаний закон Бугера - Ламберта- Бера А = x×L×C(B), де А – оптична густина; С (В) – концентрація речовини, в моль/дм3; x - молярний коефіцієнт світопоглинання; L – товщина поглинаючого шару, см. Слід звернути увагу на то, що закон Бугера –Ламберта- Бера справедливий тільки для монохроматичного випромінювання при малих концентраціях аналізуємої речовини. Закон застосовується у тих вападках, коли частки, які поглинають світло, залишаються незмінними. Якщо характер часток буде змінюватись.
Завдання для виконання самостійної роботи Відповісти на запитання: 1. Класифікація оптичних методів аналіза. 2. У чому відмінність між колометричним та фотометричним методами аналіза? 3. Сутність спектрофотометричного метода аналіза? 4. Що називається емісіонним спектральним аналізом? 5. Сутність метода фотометрії полум’я? 6. Назвіть головні оптичні характеристики забарвлених розчинів. 7. Що називається спектром поглинання (кривою світопоглинання)? 8. Правило вибора світофільтрів. 9. Що називається оптичною густиною і світопропусканням (прозоростью). Яка існує взаємодія між цими величинами? 10. Рівняння основного закона світопоглинання (закона Бугера-Ламберта-Бера). САМОСТІЙНА РОБОТА № 9. Тема: Рефрактометричний метод аналізу.
Повинні знати: основи рефрактометричного методу аналізу, будову і принцип роботи рефрактометра. Повинні вміти: використовувати знання рефрактометричного аналізу на практиці. План: 1. Сутність рефрактометричного методу аналіза. 2. Показник преломлення. 3. Мольна та питома рефракція. 4. Будова і принцип роботи рефрактометра РПЛ-3. Стислі теоретичні відомості Сутність рефрактометричного методу аналізу. Метод оснований на вимірюванні показника приломлювання аналізуємої речовини. Показник приломлювання є одним із основних показників фізико-хімічних властивостей речовини, важливою характеристикою кожної індивідуальної речовини. Рефрактометричний метод визначення сухих речовин у розчинах знаходить широке використання у якісному та кількісному аналізі окремих речовин та їх суміші у хімічній, нафтоперероблювальній, фармацептичній, харчовій та ін. промисловості. У харчовій промисловості рефрактометром визначають: вміст сахарози у водному розчині; сухих речовин в патоці, сиропі, повидлі; вологість у згущеному молоці; екстрактивність солоду і т. п.. Показник преломлення. Показником преломлення (n) називають відношення синуса кута падаючого проміння
Показник преломлення залежить від природи речовини, від довжини хвилі падаючого світла (від джерела світла), від температури і від концентрації речовини. Кут падіння, при якому промінь проходить по поверхні розділа фаз (двух середовищ), називають кутом повного внутрішнього відображення. Якщо, знати кут повного внутрішнього відображення, можна визначити значення показника заломлення. Якщо промінь світла переходить із повітря в більш густе середовище, то кут падіння завжди більше кута переломлення. Якщо кут світла переходить з більш густого середовища в менш густе, то куи падіння завжди менше кута переломлення. При використанні монохроматичного світла та при постійній температурі показник преломлення залежить від хімічного складу речовини, його структури та концентрації. Рефрактометричні вимірювання надзвичай проводять у видимій частині спектру, визначаючи n по відношенню до повітря. Мольна та питома рефракція. Щоб вивчити залежність показника преломлення від складу речовини, необхідно використовувати величини, які залежать виключно від природи речовини. Такими величинами є питома (r) та молярна (R) рефракції, для визначення яких використовують формули Лорентц-Лоренца:
де r – питома рефракція, см3/г; R – молярна рефракція, г/моль; r - густина речовини, г/см3; n – показник переломлення; М – грам-молекулярна маса. Молярна рефракція не залежить від зовнішніх факторів (температури, тиску, агрегатного стану) і володіє властивостями аддитивності. Це значить, що молярна рефракція складної сполуки дорівнює сумі атомних рефракцій елементів, які входять в цю сполуку, і рефракції (інкрементів) кратних зв’язків і циклів.
|
||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 189; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.115 (0.007 с.) |

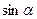 до синусу кута його преломлення
до синусу кута його преломлення  (по відношеню до повітря).
(по відношеню до повітря).
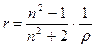 ;
; 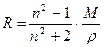 ,
,


