
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Соединения элементов семейства железа
Оксиды МеО – основные оксиды. Твердые кристаллические вещества, нерастворимые в воде: FeO (черный), CoO, NiO (зеленые). Оксиды МеО взаимодействуют с кислотами и некоторыми кислотными оксидами, FeO проявляет окислительно-восстановительную двойственность:
Получают МеО разложением гидроксидов или солей в инертной атмосфере: FeC2O4 Co(OH)2 Ме(ОН)2 – слабые, нерастворимые в воде гидроксиды, обладающие основными свойствами: Fe(OH)2 (белый), Co(OH)2 (розовый), Ni(OH)2 (зеленый). Ме(ОН)2 взаимодействуют с кислотами: Co(OH)2 + H2SO4 = CoSO4 + 2H2O. При переходе от железа к никелю устойчивость соединений в степени окисления +2 увеличивается: Fe(OH)2 → Co(OH)2 → Ni(OH)2
Fe(OH)2 легко окисляется кислородом воздуха: 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3, Е Co(OН)2 и Ni(OH)2 устойчивы на воздухе, окисляются только сильными окислителями. Получение Ме(ОН)2: реакция обмена из солей: NiSO4 + 2KOH ® Ni(OH)2↓ + K2SO4. Fe(OH)2 можно получить только при полном отсутствии в растворе кислорода. Оксиды Ме2 O 3 – амфотерные оксиды с преобладанием основных свойств: Fe2O3 (бурый), Co2O3 (неустойчивый), Ni2O3 (неустойчивый). Оксиды Co2O3, Ni2O3 разлагаются с выделением кислорода: 3Co2O3 = 2Co3O4 + 1/2O2; N2O3 = 2NiO + 1/2O2. Ме2О3 не взаимодействуют с водой, реагируют с кислотами и щелочами (при сплавлении): Fe2O3 + 6HCl = 2FeCl3 + 3H2O; Fe2O3 + 2NaOH Получение Fe2O3: 4Fe + 3O2 4FeS2 + 11O2 2Fe(OH)3 4Fe(NO3)3 Гидроксиды Ме(ОН)3. Для металлов семейства железа известны гидроксиды Ме(ОН)3: Fe(OH)3, Co(OH)3 (бурые), Ni(OH)3 (черный). Fe(ОН)3 – слабое, нерастворимое амфотерное основание с преобладанием основных свойств. Взаимодействует с кислотами и концентрированными растворами щелочей, со щелочами при сплавлении: 2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 + 6H2O; Fe(OH)3 + NaOH Fe(OH)3 + 3NaOH = Na3[Fe(OH)6]. Амфотерные свойства Со(ОН)3 и Ni(OH)3 выражены еще слабее. Так как степень окисления +3 для Со и Ni не характерна, Со(ОН)3 и Ni(OH)3 – сильные окислители, взаимодействуют с кислородсодержащими кислотами, окисляют соляную кислоту, воду до О2: 2Ni(OH)3 + 6HCl = 2NiCl2 + Cl2 + 6H2O; 4Co(OH)3 + 4H2SO4 = 4CoSO4 + O2 + 10H2O. Получают гидроксид железа (III) реакцией обмена из солей: FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl. Со(ОН)3 и Ni(OH)3 получают окислением Ме(OH)2 сильными окислителями:
2Ni(OH)2 + Br2 + 2NaOH ® 2Ni(OH)3↓ + 2NaBr Оксиды Ме 3 О 4 – смешанные оксиды MeO, Me2O3 или солеподобные соединения: Fe2+(Fe3+O2)2 феррит железа (II), Co 2+(Co3+O2)2 кобальтит кобальта (II), Ni3O4 не существует. Fe3O4 – основный оксид черного цвета, при нагревании в сильных кислотах растворяется с образованием солей железа (II) и железа (III): Fe3O4 + 4H2SO4 = FeSO4+Fe2(SO4)3 + 4H2O; Fe3O4 + 8HCl = 2FeCl3 + FeCl2 + 4H2O. Оксид Со3О4 (черного цвета) – сильный окислитель, в кислой среде окисляет воду до кислорода: 2Co3O4 + 6H2SO4 = 6CoSO4 + O2 + 6H2O; Со3О4 + 8Н+ + 2 е – = 3Со2+ + 4Н2О, Е Оксид FeO 3 – кислотный оксид и соответствующая ему железная кислота H 2 FeO 4 в свободном виде не получены. Соли этой кислоты, ферраты, получают в щелочной среде действием сильных окислителей на соединения железа в низких степенях окисления: Fe2O3 + 3KNO3 + 4KOH = 2K2FeO4 + 3KNO2 + 2H2O. феррат калия Ферраты – термически неустойчивые, красные кристаллические вещества, очень сильные окислители: 2K2FeO4 + 16HCl = 2FeCl3 + 3Cl2 + 4KCl + 8H2O; FeO Соли. Fe, Co, Ni образуют солипрактически со всеми кислотами. Соли железа 3+ с анионами, обладающими восстановительными свойствами (FeI3, Fe2S3, Fe(CN)3), не существуют. Соли железа 2+ и железа 3+ известны в равной мере. Для кобальта и никеля устойчивы соли В водных растворах соли Ме2+ гидролизуются: 2CoSO4 + 2H2O ⇄ (CoOH)2SO4 + H2SO4; Co+2 + H2O ⇄ CoOH+ + H+. Соли Ме3+ гигроскопичны, они гидролизуются сильнее, чем соли Ме2+, т. к. образованы более слабыми основаниями: FeCl3 + H2O ⇄ FeOHCl2 + HCl; Fe+3 + H2O ⇄ FeOH+2 + H+; NaFeO2 + 2H2O ⇄ Fe(OH)3 + NaOH. Водные растворы солей железа (II) применяют как восстановители: 10FeSO4 + 2 KMnO4 + 8H2SO4 = 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O. Соли железа (III) – довольно сильные окислители: 2FeCl3 + Cu = 2FeCl2 + CuCl2. Комплексные соединения. Элементы семейства железа образуют многочисленные комплексные соединения с координационным числом 6 и октаэдрическим расположением лигандов. Особенно характерны и устойчивы цианидные комплексы: K4[Fe(CN)6] – желтая кровяная соль, K3[Fe(CN)6] – красная кровяная соль, прочные низкоспиновые внутриорбитальные комплексы с d 2 sp 3-гибридизацией.
Способность цианидных комплексов давать окрашенные соединения используется в качественном анализе для определения ионов железа. Желтая кровяная соль используется для обнаружения Fe3+, красная кровяная соль – для обнаружения Fe2+: Fe3+Cl3 + K4[Fe2+(CN)6] = KFe3+[Fe2+(CN)6] + 3KCl; берлинская лазурь Fe2+Cl2 + K3[Fe3+(CN)6] = KFe2+[Fe3+(CN)6] + 2KCl. турнбуллева синь Берлинская лазурь и турнбуллева синь – идентичные осадки синего цвета. Качественной реакцией на ионы Fe3+ является комплексообразование с роданидом калия: Fe3+Cl3 + 3KCNS = Fe3+(CNS)3 + 3KCl. кроваво-красный раствор
Fe + 5CO Fe(CO)5;
Ni + 4CO Ni(CO)4. При нагревании все карбонилы разлагаются с выделением особо чистых металлов.
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 102; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.166.122 (0.011 с.) |
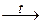 2Fe3O4;
2Fe3O4;

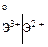 = +0,771 B.
= +0,771 B.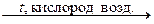 2Fe2O3;
2Fe2O3; = 1,746 В.
= 1,746 В.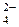 + 8H+ + 3 e – = Fe3+ + 4H2O; E
+ 8H+ + 3 e – = Fe3+ + 4H2O; E  Характерными комплексными соединениями Fe, Co, Ni являются карбонилы: Fe(CO)5, Co2(CO)8, Ni(CO)4. Их получают пропусканием CO над порошком металла при повышенном давлении и температуре. Fe(CO)5 и Ni(CO)4 – летучие жидкости, Co2(CO)8 – оранжевые кристаллы.
Характерными комплексными соединениями Fe, Co, Ni являются карбонилы: Fe(CO)5, Co2(CO)8, Ni(CO)4. Их получают пропусканием CO над порошком металла при повышенном давлении и температуре. Fe(CO)5 и Ni(CO)4 – летучие жидкости, Co2(CO)8 – оранжевые кристаллы.



