
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основные характеристики щелочных металлов
Как видно из представленных данных, в ряду Li – Cs наблюдается закономерное увеличение радиусов атомов. При переходе от лития к цезию металлические свойства и восстановительная способность элементов усиливаются. Для всех атомов щелочных металлов характерны наиболее низкие среди всех элементов значения относительных э лектроотрицательностей. Поэтому химическая связь в большинстве соединений Распространение в природе: Na – 2,5 масс. %, K – 2,5 масс. %. Остальные щелочные металлы встречаются в природе в виде примесей к солям Na и K. В свободном состоянии щелочные металлы не существуют. Важнейшие минералы, содержащие щелочные металлы:
Получение. Все щелочные металлы встречаются в природе исключительно в виде соединений, являются сильными восстановителями, и их получение требует высоких энергетических затрат. Литий получают электролизом расплава хлорида лития, который образуется при переработке сподумена. Переработка сподумена – процесс довольно сложный, сернокислотный метод включает стадии получения сульфата лития, карбоната лития и далее хлорида лития: Li2O × Al2O3 × 4SiO2 + H2SO4 Li2SO4 + Na2CO3 = Li2CO3↓ + Na2SO4; Li2CO3 + 2HCl = 2LiCl + CO2↑ + H2O. Сульфатный метод: Li2O × Al2O3 × 4SiO2 + K2SO4 Известковый способ включает стадии получения алюмината лития, гидроксида лития, хлорида лития: Li2O × Al2O3 × 4SiO2 + 4CaCO3
2LiAlO2 + Ca(OH)2 = 2LiOH + Ca(AlO2)2; LiOH + HCl = LiCl + H2O; 2LiCl Известен также способ получения лития из его оксида в вакууме: 2Li2O + Si Натрий получают электролизом расплава хлорида натрия с добавками хлорида кальция, понижающими температуру плавления: В электролизере происходят следующие электродные реакции: Катод ⊝: Na+ + e – = Na; Анод ⊕: 2Cl– – 2 e – = Cl2; 2NaCl Натрий можно получить, прокаливая соду с углем в закрытых тиглях, пары металла конденсируются на крышке тигля, выход реакции невысокий: Na2CO3 + 2C Калий, рубидий и цезий можно получить электролизом расплава их солей, однако на практике таким способом их не получают из-за высокой химической активности. Калий получают, пропуская пары натрия через расплав хлорида калия при 800°С, выделяющиеся пары калия конденсируют: KCl + Na или при взаимодействии между расплавленным гидроксидом калия и жидким натрием при 440°С: KOH + Na Рубидий и цезий получают восстановлением их хлоридов кальциием в вакууме при 700–800°С: 2RbCl + Ca В качестве восстановителя также используют магний, алюминий, кремний, цирконий. Физические свойства. Щелочные металлы – это серебристо-белые блестящие металлы, быстро тускнеющие на воздухе. Для них характерны низкие температуры плавления, малые значения плотностей, низкий потенциал ионизации, который уменьшается с увеличением атомного номера (табл. 8.1). Щелочные металлы мягкие, режутся ножом. Низкие значения температур кипения и плавления для щелочных металлов объясняются тем, что в их кристаллах металлическая связь непрочная (на один атом металла приходится только один свободный электрон). По мере роста радиуса атома прочность, связи в кристаллах щелочных металлов закономерно уменьшается. Следовательно, в ряду Li ‒ Cs понижаются температуры кипения и плавления. Щелочные металлы относятся к группе легких металлов (плотность меньше 5 г/см3), что объясняется строением их кристаллической решетки. Химические свойства. Типичные металлы, очень сильные восстановители. Восстановительная способность увеличивается с ростом атомной массы: Li – Na – K – Rb – Cs.
Реакции с простыми веществами: С кислородом. Продукты окисления щелочных металлов на воздухе имеют разный состав в зависимости от активности металла. Только литий окисляется на воздухе с образованием оксида: 4Li + O2 = 2Li2O–2 (оксид). При окислении натрия в основном образуется пероксид Na2O2 с небольшой примесью надпероксида NaO2: 2Na + O2 = Na2O В продуктах окисления калия, рубидия и цезия содержатся в основном надпероксиды: K + O2 = KO Элементы могут образовывать озониды по реакции с озоном: K + O3 = KO3; 4KOH + 4O3 = 4KO3 + O2 + 2H2O. Оксиды щелочных металлов Ме2О – кристаллические термически устойчивые вещества, при взаимодействии с водой образуют щелочи: Ме2О + Н2О = 2МеОH. Все пероксиды, надпероксиды, озониды – сильные окислители и разлагаются водой: K2O2 + 2H2O = 2KOH + H2O2; 2KO2 + 2H2O = 2KOH + O2 + H2O2; 4KО3 + 2H2O = 4KOH + 5O2. С водородом. При нагревании щелочные металлы соединяются с водородом с образованием гидридов: 2Na + H2 Гидриды металлов – сильные восстановители за счет водорода в степени окисления –1. Гидриды разлагаются водой и кислотами с выделением водорода: NaH + H2O = NaOH + H2; NaH + HCl = NaCl + H2. С галогенами щелочные металлы взаимодействуют с образованиием галогенидов: 2Na + Cl2 С серой щелочные металлы взаимодействуют с образованием сульфидов: 2Na + S С азотом, фосфором, углеродом и кремнием щелочные металлы взаимодействуют с образованием, соответственно, нитридов, фосфидов, карбидов и силицидов. Полученные соединения разлагаются водой и кислотами c образованием летучих водородных соединений:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 59; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.0.53 (0.012 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Уменьшение
Уменьшение , В
, В
 Li2SO4 + Al2O3 + 4SiO2 × H2O;
Li2SO4 + Al2O3 + 4SiO2 × H2O;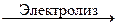 2Li + Cl2.
2Li + Cl2.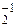 (пероксид).
(пероксид).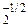 (надпероксид).
(надпероксид).


