Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кислородсодержащие соединения Mn , Tc , Re
Известны оксиды марганца в степенях окисления +2, +4, +7 и смешанные оксиды Mn3O4, Mn2O3. С ростом степени окисления основные свойства ослабевают, а кислотные свойства усиливаются, повышается окислительная активность. Низшие оксиды Tc и Re неустойчивы и малоизучены. Оксид марганца (II) Mn О – основный оксид. Это нерастворимое в воде кристаллическое вещество зеленого цвета. Взаимодействует с кислотами: MnO + H2SO4 = MnSO4 + H2O. MnO получают разложением солей: MnCO3 = MnO + CO2. MnO используют в лабораториях для удаления примесей кислорода из инертных газов: 2MnO + O2 = 2MnO2. Гидроксид марганца (II) Mn (OH)2 – слабое основание, немного растворимое в воде. Взаимодействует с кислотами: Mn(OH)2 + H2SO4 = MnSO4 + 2H2O. Гидроксид Mn(OH)2легко окисляется кислородом воздуха. MnO и Mn(OH)2 проявляют востановительные свойства: 4Mn(OH)2 + 2O2 + 4H2O = 4Mn(OH)4 или (MnO2 n H2O). белый коричневый Mn(OH)2 получают в виде белого осадка из солей реакцией обмена: MnSO4 + 2KOH = Mn(OH)2↓ + K2SO4. Оксиды Mn 2 O 3, Mn 3 O 4 можно рассматривать как соли метамарганцеватистой (Н2MnO3) и ортомарганцеватистой (H4MnO4) кислот. Оксиды содержат Mn в степенях окисления +2 и +4: Mn2O3 ® Mn+2Mn+4O3 – метаманганит марганца (П); Mn3O4 ® Mn Доказательством смешанного характера оксидов является взаимодействие с азотной кислотой: Mn2O3 + 2НNO3 = Mn+2(NO3)2 + Mn+4O2 + H2O. Mn2O3, Mn3O4 получают при нагревании MnO2: 4MnO2 Оксиды марганца, технеция, рения (IV) МеО2. известны для всех рассматриваемых металлов. MnO2, TcO2, ReO2 – не растворимые в воде твердые вещества черного цвета. МеО2 устойчивы, инертны по отношению к разбавленным растворам кислот и щелочей. TcO2 – самый устойчивый оксид технеция, ReO2 – менее устойчив, при нагревании диспропорционирует на Re2O7 и Re. Оксиды МеО2 – слабоамфотерны, с преобладанием кислотных свойств у MnO2. Взаимодействуют со щелочами в концентрированных растворах и расплавах: MnO2 + 2KOH = K2Mn+4O3 + H2O (манганит калия); ReO2 + 2NaOH = Na2Re+4O3 + H2O (ренит натрия). MnO2, как соединение в промежуточной степени окисления марганца, проявляет окислительно-восстановительную двойственность, однако окислительные свойства для него более характерны: MnO2 + 4H+ = Mn2+ + 2H2O; E Поэтому при взаимодействии с кислотами при нагревании MnO2 не образует катиона Mn+4, а проявляет окислительные свойства:
MnO2 + 4HCl(конц) = MnCl2 + Cl2 + 2H2O. Эта реакция используется для получения хлора в лаборатории. Диоксид марганца широко используют в качестве окислителя в химических источниках тока. В реакциях с более сильными окислителями MnO2 проявляет восстановительные свойства, переходит в соединение Mn (VI) или (VII): 3MnO2 + KClO3 + 6KOH = 3K2MnO4 + KCl + 3H2O. Для TcO2 и ReO2 окислительные свойства не характерны: ReO2 + 6HCl = H2[ReCl6] + 2H2O. Получают MnO2 разложением нитрата Mn (II):или Mn2O7: Mn(NO3)2 = MnO2 + 2NO2; 2Mn2O7 = 4MnO2 + 3O2. TcO2 и ReO2 получают разложением солей: 2NH4ReO4 = 2ReO2 + N2 + 4H2O. Гидроксиды Ме(ОН)4. Формула Ме(ОН)4 – условна, это соединения переменного состава, им соответствует формула МеО2 × n Н2О. Ме(ОН)4 – очень слабые, нерастворимые гидроксиды бурого цвета, обладающие амфотерными свойствами. Mn(OH)4 рассматривают чаще как марганцоватистую кислоту – H2MnO3. Mn(OH)4 со щелочами образует манганиты: Mn(OH)4 + 2KOH = K2 Mn+4O3 + 3H2O (метаманганит калия); Mn(OH)4 + 4KOH = K4Mn+4O4 + 4H2O (ортоманганит калия). C концентрированной серной кислотой Mn(OH)4 образует нестойкую соль: Mn(OH)4 + 2H2SO4 ® Mn(SO4)2 + 4H2O. Гидратированный оксид MnO2 × n H2O является еще более сильным окислителем, чем безводный MnO2. Получают Mn(OH)4 окислением соединений марганца (II): 4Mn(OH)2 + 2O2 + 4H2O ® 4Mn(OH)4 или (MnO2 × n H2O), восстановлением KMnO4 в нейтральной или слабощелочной среде: 2KMnO4 + 4H2O + 6KI ® 2MnO2 + 3I2 + 8KOH. Оксид марганца (VI) MnO 3 – кислотный оксид. MnO3 и соответствующая ему марганцовистая кислота H2MnO4, вследствие их нестойкости, не выделены. При получении они мгновенно разлагаются. Соли H 2 MnO 4 – манганаты, темно-зеленые кристаллы, получают сплавлением MnO2 со щелочами в присутствии окислителей: 2MnO2 + 4KOH + O2 Манганаты в водных растворах существуют только в сильнощелочной среде, в нейтральной и слабокислой среде диспропорционируют: 3K2Mn+6O4 + 2H2O = 2KMn+7O4 + Mn+4O2 + 4KOH. Соединения Mn+6 являются сильными окислителями и легко восстанавливаются до MnO2 (в щелочной среде) или солей Mn+2 (в кислой среде). Однако при действии более сильных окислителей они превращаются в перманганаты: 2K2MnO4 + Cl2 = 2KMnO4 + 2KCl; MnO Cl2 + 2 e – = 2Cl–, Е Оксиды марганца, технеция, рения (VII) M е 2 O 7 – кислотные оксиды, легко растворяются в воде с образованием марганцовой, технециевой, рениевой кислот:
Mn2O7 Tc2O7 R2O7 черно-зеленая желтый желтый маслянистая жидкость кристаллические вещества Mn2O7 – термически неустойчив, разлагается при ударе или нагревании: 2Mn2O7 ® 4MnO2 + 3O2 Гидроксиды HMeO 4 – сильные кислоты. В ряду HMnO4, HTcO4, HReO4 происходит усиление устойчивости и ослабление кислотных свойств: HMnO4 HTcO4 HReO4
HMnO4 наименее устойчива, в свободном виде не получена, существует только в растворах с массовой долей HMnO4 не более 20%. При большей концентрации HMnO4 разлагается: 4HMnO4 = 4MnO2 + 2H2O + 3O2. Кислотам HЭO4 соответствуют соли: перманганаты (фиолетовые), пертехнаты (красно-желтые), перренаты (бесцветные). Твердые перманганаты термически неустойчивы, разлагаются при нагревании: 2KMnO4 Эта реакция используется для получения О2 в лаборатории. Mn2O7, HMnO4 и перманганаты – сильные окислители. В зависимости от кислотности среды возможны следующие схемы восстановления ионов MnO41–: (pH < 7) MnO (наблюдается обесцвечивание раствора) (рН» 7) MnO (образуется бурый осадок) (рН >12,5) MnO (образуется зеленый раствор) Как видно из приведенных значений E Производные Тс (VII) и Re (VII) устойчивы при нагревании, являяются слабыми окислителями, т. к. находятся в характерной для них степени окисления. Получают Mn2O7 по реакции: 2KMnO4 + H2SO4(конц) = Mn2O7 + K2SO4 + H2O. Tc2O7, Re2O7 получают при окислении соответствующих элементов кислородом. Перманганаты в промышленности получают электрохимическим окислением манганатов: MnO В лаборатории их получают окислением солей марганца (II) сильными окислителями: 2MnSO4 + 5(NH4)2S2O8 + 8H2O = 2HMnO4 + 5(NH4)2SO4 + 7H2SO4. Mn образует соли со всеми известными кислотами. Ионы Mn2+ в растворе существуют в виде гидратных комплексов [Mn(H2O)6]2+, [Mn(H2O)4]2+. Из водных растворов они кристаллизуются в виде кристаллогидратов: Mn(NO3)2 × 6Н2О, Mn(ClO4)2 × 6H2O, MnSO4 × 7H2O. Растворимы все соли марганца, кроме MnCO3, MnS, Mn3(PO4)2. Растворимые соли марганца (II) подвергаются гидролизу: MnCl2 + H2O ⇄ MnOHCl + HCl; Mn2+ + H2O ⇄ MnOH+ + H+. Соли Mn2+ проявляют восстановительные свойства. В кислой среде окисление Mn2+ сопровождается образованием MnO2, под действием сильных окислителей образуются перманаганаты: 2Mn(NO3)2 + 5PbO2 + 6HNO3 = 2HMnO4 + 5Pb(NO3)2 +2H2O. В сильнощелочной среде образуются манганаты: 3MnSO4 + 2KClO3 + 12KOH = 3K2MnO4 + 2KCl + 3K2SO4 + 6H2O. Комплексные соединения. Для Mn2+ менее характерно комплексообразование, чем для других d- элементов. Это связано с электронной конфигурацией d 5 иона Mn2+. В высокоспиновом комплексе электроны заполняют по одному все d- орбитали:
В результате на орбиталях содержатся d- электроны как с высокой, так и с низкой энергией; суммарный выигрыш энергии, обусловленный действием поля лигандов, равен нулю. Координационное число марганца равно 6. В водных растворах ионы Mn2+ образуют октаэдрический аквакомплекс [Mn(H2О)6]2+. При действии избытка водного раствора аммиака на растворы солей Mn2+ oсаждается гидроксид Mn(ОН)2, амминокомплексы не образуются. При действии цианидов на соли Mn2+ образуются комплексы, содержащие ионы [Mn(СN)6]4–, которые легко окисляются на воздухе:
Mn(CN)2 + 4KCN = K4[Mn(CN)6]. Как обычно, комплексообразование стабилизирует неустойчивые в водном растворе состояния окисления. Так, могут быть получены в кристаллическом состоянии галогеноманганаты M2+[Mn+3F5], M2+[Mn+3Cl5], M2+[Mn+4F6], M2+[Mn+4Cl6]. Ионы [MnГ6]2– имеют октаэдрическое строение. Mn, Tc, Re образуют двухядерные карбонилы Ме2(СО)10 кластерного типа со связью металл-металл. Это летучие кристаллические вещества.
Биогенная роль марганца Из элементов VII Б группы только марганец является биогенным элементом и одним из десяти металлов жизни, необходимых для нормального протекания процессов в живых организмах. Установлено, что марганец участвует в основных нейрохимических процессах в центральной нервной системе, в образовании костной и соединительной тканей, регуляции жирового и углеводного обмена, обмене витаминов. Марганец оказывает влияние на процессы кроветворения и иммунную защиту организма. Укушенного каракуртом (ядовитым среднеазиатским пауком) человека можно спасти, если ввести ему внутривенно раствор сульфата марганца. В крови человека и большинства животных содержание марганца составляет около 0,02 мг/л. Суточная потребность взрослого организма составляет 3–5 мг Mn. Дефицит марганца – одно из распространенных отклонений в элементном обмене современного человека. Это связано со значительным снижением потребления богатых марганцем продуктов (грубая растительная пища, зелень), увеличением количества фосфатов в организме (лимонады, консервы и др.), ухудшением экологической ситуации в крупных городах и психо-эмоциональной перенапряженностью. Коррекция дефицита марганца оказывает положительное влияние на состояние здоровья человека. Избыточное накопление марганца в организме сказывается, в первую очередь, на функционировании центральной нервной системы. Это проявляется в утомляемости, сонливости, ухудшении функций памяти и наблюдается в основном у рабочих, связанных с производством марганца и его сплавов. О наличии технеция в живых организмах данных нет. Однако соединения технеция с бисфосфонатами используют для радиоизотопного метода диагностики. Метастабильный изотоп технеция 99Тс является излучителем лучей. После внутривенного введения препарата «Технефор», содержащего 99Тс, можно исследовать состояние мягких тканей, а через 2–3 ч после введения – костных. Таким образом, для решения медико-биологических задач используются не только соединения жизненно необходимого Мn, но и соединения искусственного элемента 99Тс.
|
||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 632; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.66.178 (0.05 с.) |
 Mn+4O4 – ортоманганит марганца (П).
Mn+4O4 – ортоманганит марганца (П).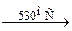 2Mn2O3 + O2; 6Mn2O3
2Mn2O3 + O2; 6Mn2O3  4Mn3O4 + O2..
4Mn3O4 + O2.. = +1,23 B.
= +1,23 B. 2K2MnO4 + 2H2O (манганат калия).
2K2MnO4 + 2H2O (манганат калия).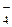 + e – = MnO
+ e – = MnO 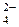 , E
, E 
 K2MnO4 + MnO2 + O2.
K2MnO4 + MnO2 + O2.