
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Правило фаз и правило отрезков.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Правило фаз Гиббса Закономерности существования устойчивых фаз в условиях равновесия определяются правилом фаз Гиббса. Правило фаз, устанавливая количественную зависимость между числом фаз Ф, количеством компонентов К и числом степеней свободы С, дает возможность предсказать процессы, проходящие в сплавах при нагреве и охлаждении, и определить число фаз в системе при данных условиях. Правило фаз выражается следующим уравнением: С = К + Р-Ф. Под числом степеней свободы, или вариантностью системы, понимают число внешних Р (температура, давление) и внутренних (концентрация) факторов, которые можно изменять без изменения числа фаз, находящихся в равновесии. Для металлических сплавов внешним фактором равновесия является только температура, так как при работе в атмосферных условиях давление практически постоянно. Поэтому для металлических сплавов правило фаз принимает следующий вид: С = К + 1 - Ф. Вариантность не может быть отрицательной. Поэтому для равновесия металлических сплавов необходимо, чтобы в их структуре число фаз не превышало число компонентов более, чем на 1. Из этого уравнения следует, что в случае кристаллизации чистого металла, когда имеются две фазы (жидкая и твердая), число степеней свободы равно нулю, так как С = К+1-Ф = 1 + 1-2 = 0. Такая система является инвариантной. Обе фазы находятся в равновесии при строго определенной температуре - температуре затвердевания. Температура может измениться только при исчезновении одной из фаз. Если чистый металл находится в жидком состоянии и присутствует только одна жидкая фаза, то число степеней свободы будет равно 1 (моновариантная система): C = к + 1 -Ф = 1 + 1 - 2 = 1. Наличие одной степени свободы показывает возможность изменять, например, в определенных пределах температуру без изменения числа фаз. Из правила фаз следует, что в двойных системах число одновременно существующих фаз не может быть более 3. При большем числе фаз сплав не будет находиться в равновесном состоянии. Правило фаз используется при построении диаграмм состояния сплавов. Правило отрезков. Посредством правила отрезков можно определить состав фаз в любой двухфазной области и количественное их соотношение. Правило отрезков состоит из двух частей. Первая часть: для того чтобы определить состав фаз через заданную точку в двухфазной области (точка соответствует конкретной температуре) проводят горизонтальную линию до пересечения с линиями, ограничивающими эту область. Проекция точек пересечения на ось концентрации даст нам состав фаз. Вторая часть: для того чтобы определить количество фаз через заданную точку проводят горизонтальную линию до пересечения с линией, ограничивающей эту область. Отрезки между заданной точкой и точками с соответствующим составом фаз обратно пропорциональны их количеству Тема №21 Понятие диаграммы состояния сплава. Диаграмма состояния представляет собой графическое изображение состояния сплава в зависимости от его температуры, давления и химического состава. Под состоянием понимается фазовый состав сплава, т.е. число и тип составляющих его фаз. Обычно давление считают постоянным, поэтому диаграмма принимает вид зависимости состояния сплава от температуры и концентрации компонентов. По оси Y откладывают температуру в °С, а по оси X концентрацию компонентов. Крайняя левая точка на этой оси соответствует чистому компоненту А, а крайняя правая - чистому компоненту В. Средняя точка соответствует сплаву с содержанием 50% А и 50% В и т.д. Как правило, на диаграмме указывают процентное содержание только одного из компонентов, обычно В. Концентрацию компонента А определяют по формуле: %А = 100% - %В. Каждая точка диаграммы состояния отражает фазовый состав сплава определенной концентрации, находящегося при определенной температуре. Так точка а отражает состояние сплава с концентрацией компонентов К1, находящегося при температуре Т1. Необходимо отметить, что все состояния сплава, отражаемые диаграммой, являются устойчивыми, равновесными, обладающими при данных условиях минимальной свободной энергией. По этой причине диаграммы состояния иногда называют равновесными диаграммами или диаграммами фазового равновесия. Если сплав двухкомпонентный, то его диаграмма состояния является плоской. Если сплав трёх- и более компонентный, его диаграмма имеет более сложный пространственный характер. В этом случае приводят ряд двухмерных срезов такой диаграммы. С помощью диаграмм состояния можно определять температуры плавления, кристаллизации и полиморфных превращений у различных сплавов, а так же тип, количество и химический состав фаз в конкретных сплавах при любой температуре. Диаграммы состояния обычно строят экспериментально, используя так называемый термический метод. В этом методе сплавы различных составов (чем больше, тем точнее) нагревают в печи до расплавленного состояния, а затем охлаждают на воздухе, измеряя через равные промежутки времени их температуру. Температуру сплавов обычно измеряют с помощью термопары. В результате получают так называемые кривые охлаждения, то есть графики зависимости температуры сплава от времени. По остановкам и перегибам на этих кривых, вызванных тепловыми эффектами превращений, определяют температуры фазовых превращений в сплавах. Параллельно методом рентгеноструктурного анализа и электронной микроскопии изучают микроструктуру сплавов в различных температурных интервалах. Полученные данные используют для построения диаграмм состояния. Тема №22 Диаграмма состояния. Диаграмма состояния представляет собой графическое изображение состояния любого сплава изучаемой системы в зависимости от концентрации и температуры (рис. 4.5). Рис. 4.5. Диаграмма состояния Диаграммы состояния показывают устойчивые состояния, т.е. состояния, которые при данных условиях обладают минимумом свободной энергии, и поэтому ее также называют диаграммой равновесия, так как она показывает, какие при данных условиях существуют равновесные фазы. Построение диаграмм состояния наиболее часто осуществляется при помощи термического анализа. В результате получают серию кривых охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба и температурные остановки. Температуры, соответствующие фазовым превращениям, называют критическими точками. Некоторые критические точки имеют названия, например, точки отвечающие началу кристаллизации называют точками ликвидус, а концу кристаллизации – точками солидус. По кривым охлаждения строят диаграмму состава в координатах: по оси абсцисс –концентрация компонентов, по оси ординат – температура. Шкала концентраций показывает содержание компонента В. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии соответствующие фазовым превращениям в твердом состоянии (3, 4). По диаграмме состояния можно определить температуры фазовых превращений, изменение фазового состава, приблизительно, свойства сплава, виды обработки, которые можно применять для сплава Тема №23 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (сплавы твердые растворы с неограниченной растворимостью) Диаграмма состояния и кривые охлаждения сплавов системы представлены на рис. 5.1.
Рис.5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (а); кривые охлаждения типичных сплавов (б)
Сначала получают термические кривые. Полученные точки переносят на диаграмму, соединив точки начала кристаллизации сплавов и точки конца кристаллизации, получают диаграмму состояния. Проведем анализ полученной диаграммы. 1. Количество компонентов: К = 2 (компоненты А и В). 2. Число фаз: f = 2 (жидкая фаза L, кристаллы твердого раствора 3. Основные линии диаграммы: · acb – линия ликвидус, выше этой линии сплавы находятся в жидком состоянии; · adb – линия солидус, ниже этой линии сплавы находятся в твердом состоянии. 4. Характерные сплавы системы: Чистые компоненты А и В кристаллизуются при постоянной температуре, кривая охлаждения компонента В представлена на рис. 5.1, б. Остальные сплавы кристаллизуются аналогично сплаву I, кривая охлаждения которого представлена на рис. 5.1, б. Процесс кристаллизации сплава I: до точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинают образовываться центры кристаллизации твердого раствора
Рис. 5.2. Схема микроструктуры сплава – однородного твердого раствора 5. Количественный структурно-фазовый анализ сплава. Пользуясь диаграммой состояния можно для любого сплава при любой температуре определить не только число фаз, но и их состав и количественное соотношение. Для этого используется правило отрезков. Для проведения количественного структурно-фазового анализа через заданную точку проводят горизонталь (коноду) до пересечения с ближайшими линиями диаграммы (ликвидус, солидус или оси компонентов). а) Определение состава фаз в точке m: Для его определения через точку m проводят горизонталь до пересечения с ближайшими линиями диаграммы: ликвидус и солидус. Состав жидкой фазы определяется проекцией точки пересечения горизонтали с линией ликвидус p на ось концентрации. Состав твердой фазы определяется проекцией точки пересечения горизонтали с линией солидус q (или осью компонента) на ось концентрации. Состав жидкой фазы изменяется по линии ликвидуса, а состав твердой фазы – по линии солидуса. С понижением температуры состав фаз изменяется в сторону уменьшения содержания компонента В. б) Определение количественного соотношения жидкой и твердой фазы при заданной температуре (в точке m): Количественная масса фаз обратно пропорциональна отрезкам проведенной коноды.Рассмотрим проведенную через точку m коноду и ее отрезки. Количество всего сплава (Qсп) определяется отрезком pq. О трезок, прилегающий к линии ликвидус pm, определяет количество твердой фазы.
Отрезок, прилегающий к линии солидус (или к оси компонента) mq, определяет количество жидкой фазы.
Тема №24 Диаграмма состояния сплавов с отсутствием растворимости компонентов в компонентов в твердом состоянии (механические смеси) Диаграмма состояния и кривые охлаждения типичных сплавов системы представлены на рис. 5.3.
Рис. 5.3. Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (а) и кривые охлаждения сплавов (б) Проведем анализ диаграммы состояния. 1. Количество компонентов: К = 2 (компоненты А и В); 2. Число фаз: f = 3 (кристаллы компонента А, кристаллы компонента В, жидкая фаза). 3. Основные линии диаграммы: линия ликвидус acb, состоит из двух ветвей, сходящихся в одной точке; линия солидус ecf, параллельна оси концентраций стремится к осям компонентов, но не достигает их; 4. Типовые сплавы системы. а) Чистые компоненты, кристаллизуются при постоянной температуре, на рис 5.3 б показана кривая охлаждения компонента А. б) Эвтектический сплав – сплав, соответствующий концентрации компонентов в точке с (сплав I). Кривая охлаждения этого сплава, аналогична кривым охлаждения чистых металлов (рис. 5.3 б) Эвтектик а – мелкодисперсная механическая смесь разнородных кристаллов, кристаллизующихся одновременно при постоянной, самой низкой для рассматриваемой системы, температуре. При образовании сплавов механических смесей эвтектика состоит из кристаллов компонентов А и В: Эвт. (кр. А + кр. В) Процесс кристаллизации эвтектического сплава: до точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинается одновременная кристаллизация двух разнородных компонентов. На кривой охлаждения отмечается температурная остановка, т.е. процесс идет при постоянной температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии трех фаз (жидкой и кристаллов компонентов А и В) число степеней свободы будет равно нулю в) Другие сплавы системы аналогичны сплаву II, кривую охлаждения сплава см на рис 5.3.б. Процесс кристаллизации сплава II: до точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинают образовываться центры кристаллизации избыточного компонента В. На кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации. На участке 1–2 идет процесс кристаллизации, протекающий при понижающейся температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии двух фаз (жидкой и кристаллов компонента В) число степеней свободы будет равно единице Схема микроструктуры сплава представлена на рис. 5.4. Рис. 5.4. Схема микроструктур сплавов: а – доэвтектического, б – эвтектического, в – заэвтектического 5. При проведении количественного структурно-фазового анализа, конода, проведенная через заданную точку, пересекает линию ликвидус и оси компонентов, поэтому состав твердой фазы или 100 % компонента А, или 100 % компонента В. Тема №25 Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии Диаграмма состояния и кривые охлаждения типичных сплавов системы представлены на рис.5.5. 1. Количество компонентов: К = 2 (компоненты А и В); 2. Число фаз: f = 3 (жидкая фаза и кристаллы твердых растворов 3. Основные линии диаграммы: линия ликвидус acb, состоит из двух ветвей, сходящихся в одной точке; линия солидус аdcfb, состоит из трех участков; dm – линия предельной концентрации компонента В в компоненте А; fn – линия предельной концентрации компонента А в компоненте В. 4. Типовые сплавы системы. При концентрации компонентов, не превышающей предельных значений (на участках Аm и nВ), сплавы кристаллизуются аналогично сплавам твердым растворам с неограниченной растворимостью, см кривую охлаждения сплава I на рис. 5.5 б. При концентрации компонентов, превышающей предельные значения (на участке dcf), сплавы кристаллизуются аналогично сплавам механическим смесям, см. кривую охлаждения сплава II на рис. 5.5 б.
Рис. 5.5 Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии (а) и кривые охлаждения типичных сплавов (б)
Сплав с концентрацией компонентов, соответствующей точке с, является эвтектическим сплавом. Сплав состоит из мелкодисперсных кристаллов твердых растворов Кристаллы компонентов в чистом виде ни в одном из сплавов не присутствуют. Тема №26 Диаграмма с перитектикой Другой тип нонвариантного превращения (трехфазного превращения) происходит, когда жидкая фаза взаимодействует с ранее выпавшими кристаллами (b - фазы) и они образуют новый вид кристаллов (a - фазы) (рис.6.9): Lc + bД t const® aР.
Рис. 6.9. Диаграмма состояния с перитектикой (а) и кривая охлаждения сплава I(б) Тема №27 Диаграмма состояния сплавов, компоненты которых образуют химические соединения.
Диаграмма состояния сплавов представлена на рис. 5.6. Рис. 5.6. Диаграмма состояния сплавов, компоненты которых образуют химические соединения Диаграмма состояния сложная, состоит из нескольких простых диаграмм. Число компонентов и количество диаграмм зависит от того, сколько химических соединений образуют основные компоненты системы. Число фаз и вид простых диаграмм определяются характером взаимодействия между компонентами. Эвт1 (кр. А + кр. AmBn); Эвт2 (кр. B + кр. AmBn). Тема №28
|
||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 3869; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.237.231 (0.01 с.) |



 )
)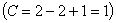 . При достижении температуры соответствующей точке 2, сплав затвердевает, при дальнейшем понижении температуры охлаждается сплав в твердом состоянии, состоящий из однородных кристаллов твердого раствора
. При достижении температуры соответствующей точке 2, сплав затвердевает, при дальнейшем понижении температуры охлаждается сплав в твердом состоянии, состоящий из однородных кристаллов твердого раствора 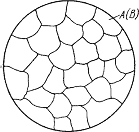 Схема микроструктуры сплава представлена на рис. 5.2.
Схема микроструктуры сплава представлена на рис. 5.2.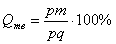


 . В точке 1/ процесс кристаллизации завершается. Ниже точки 1/ охлаждается сплав, состоящий из дисперсных разнородных кристаллов компонентов А и В.
. В точке 1/ процесс кристаллизации завершается. Ниже точки 1/ охлаждается сплав, состоящий из дисперсных разнородных кристаллов компонентов А и В.
 (раствор компонента А в компоненте В));
(раствор компонента А в компоненте В));





