
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Современные представления о структуре элементовСодержание книги
Поиск на нашем сайте
Дыхательной цепи
В переносе электронов от субстрата к молекулярному кислороду принимают участие: 1. Коферменты на основе витамина В5 (РР) - пиридинзависимые дегидрогеназы, для которых коферментами служат либо НАД, либо НАДФ; 2. Коферменты на основе витамина В2 - флавиновые дегидрогеназы (флавиновые ферменты), у которых роль простетической группы играют ФАД или ФМН; 3. Убихинон (коэнзим Q); 4. Цитохромы, содержащие в качестве простетической группы железопорфириновую кольцевую систему. Среди компонентов дыхательной цепи обнаружены также и железосерные белки (FeS), содержащие негеминовое железо. 5.2.1. Характеристика коферментов на основе витамина В5 (РР)
Витамин B5 является компонентом коферментов. Функции витамина в организме человека выполняют никотиновая кислота и ее амид. Ниацин в организме используется для образования никотинамидных коферментов. Их представителями являются никотинамид-аденин-динуклеотид (НАД+, NAD+) и никотинамид-аденин-динуклеотид-фосфат (НАДФ+, NADP+). Эти коферменты образуют специфические, каталитически активные комплексы с многочисленными (более 200) дегидрогеназами. Холоферменты участвуют в осуществлении окислительно-восстановительных реакций метаболизма. В частности, эти комплексы: 1. Облегчают реакции окисления одного субстрата за счет восстановления другого. Эти реакции особенно важны для осуществления окислительных процессов в отсутствии кислорода. Примером подобных реакций может служить обратимое окисление молочной кислоты до пировиноградной, которую катализирует фермент лактатдегидрогеназа (ЛДГ):
молочная к-та НАД+ НАДН∙Н+ ПВК
Схема 1. Участие кофермента НАД+ в обратимом окислении молочной кислоты в составе фермента лактатдегидрогеназы 2. Обеспечивают функцию компонентов дыхательной цепи, транспортируя электроны (водород) от субстрата на кислород.
Схема 2. Химическое строение никотинамида
Схема 3. Химическое строение никотиновой кислоты Помимо окислительно-восстановительных реакций, лежащих в основе энергетического обмена, ниацин участвует в ряде других, не окислительно-восстановительных реакций. В частности доказано, что эти реакции сопровождают передачу информации от клетки к клетке, транскрипцию ДНК, синтез хроматина, дифференциацию клеток и многие другие жизненные процессы. Поступает с пищей, синтезируется в организме из триптофана. Участвует в процессах тканевого дыхания, углеводном, белковом и липидном обмене, оказывает нормализующее влияние на уровень холестерина. Обладает выраженным свойством расширять периферические сосуды
Схема 4. Химическая структура кофермента НАД+ В рамке показана восстановленная форма активного центра кофермента (НАДН·Н+). Стрелкой показано расположение фосфатной группы в молекуле НАДФ. Суточная потребность в витамине В 5 (РР) – 15-25 мг. Повышается при физической нагрузке, лактации, низкой температуре, в высокогорье, а также при инфекционных заболеваниях, поражениях желудочно-кишечного тракта и нарушении всасывания. В организме возможен синтез никотиновой кислоты из аминокислоты триптофана. При этом из одной из 50 молекул триптофана образуется одна молекула никотиновой кислоты. Недостаток триптофана в пище резко усугубляет симптомы гиповитаминоза никотиновой кислоты при его наличии. Контрольные вопросы 1. В какие реакциях в организме принимает участие ниацин? 2. Сколько составляет суточная потребность в витамине В 5? 5.2.2. Характеристика коферментов на основе витамина В2 Относится к группе животных пигментов – флавонов. Рибофлавин хорошо растворим в воде, устойчив в кислых растворах, но легко разрушается в нейтральных и щелочных растворах. Весьма чувствителен к УФ-излучению и сравнительно легко подвергается обратимому восстановлению, присоединяя водород по месту двойных связей и превращается в бесцветную лейкоформу. Это свойство рибофлавина легко окисляться и восстанавливаться лежит в основе его биологического действия в клеточном метаболизме. Участвует в окислительно-восстановительных реакциях, влияя на обмен веществ всего организма. Витамин B2 интенсифицирует процессы обмена веществ в организме, участвуя в метаболизме белков, жиров и углеводов. Рибофлавин необходим для образования красных кровяных телец и антител, для дыхания клеток и роста. Он облегчает поглощение кислорода клетками кожи, ногтей и волос. Он улучшает состояние органа зрения, принимая, наряду с витамином A, участие в процессах темновой адаптации, снижает усталость глаз и играет большую роль в предотвращении катаракты. Витамин B2 оказывает положительное воздействие на слизистые оболочки пищеварительного тракта. Рибофлавин входит в состав флавиновых коферментов, в частности ФМН (флавиномононуклеотид) и ФАД (флавиноадениндинуклеотид).
6,7-Диметил-9-(D-1-рибитил)-изоаллоксазин Схема 5. Химическое строение рибофлавина
Различают 2 типа реакций с участием этих коферментов: 1. Фермент осуществляет прямое окисление с участием кислорода, т.е. дегидрирование (отщепление электронов и протонов) исходного субстрата или промежуточного метаболита. К ферментам этой группы относятся оксидазы L- и D-аминокислот, ацил-КоА-дегидрогеназа, глициноксидаза и др.
 
Схема 6. Химическое строение окисленной формы кофермента ФАД (ФМН). (цифрами 1 и 5 показаны места присоединения водорода в окислительно-восстановительных реакциях с образованием восстановленной формы кофермента ФАДН2)
В качестве примера можно привести следующую схему окисления с участием ФАД:
(суб. восс.ф.) (суб. окис.ф.)
ФАД ФАДН2 Схема 7. Участие кофермента ФАД в окислении карбоновых кислот 2. Характеризуется переносом электронов и протонов в системе биологического окисления. ФМН и ФАД прочно связываются с белковым компонентом молекулы фермента, иногда ковалентно, как в молекуле сукцинатдегидрогеназы. В составе дыхательной цепи ФМН в качестве кофермента входит в состав НАД·Н-дегидрогеназы, которая акцептирует водород, отщепляемый от НАДН·Н+. Молекулярная масса НАД·Н-дегидрогеназы около 106. Этот флавиновый фермент тесно связан с железосерным белком, участвующим передаче электронов на коэнзим Q. НАД·Н-дегидрогеназа пересекает поперек внутреннюю мембрану митохондрий, находясь в окружении липидов. Активный центр ее обращен к внутренней поверхности этой мембраны, т.е. к матриксу. Суточная потребность в витамине В2 – 2-3 мг. Возрастает при физической нагрузке, лактации, высокой калорийности пищи с большим содержанием белка, при употреблении больших количеств никотиновой кислоты. Контрольные вопросы 1. Какие функции в организме выполняет рибофлавин? 2. В состав каких коферментов входит рибофлавин? 3. Какие реакции в организме протекают с участием этих коферментов? 4. Сколько составляет суточная потребность в витамине В2?
|
||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 353; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.12.34.150 (0.01 с.) |


 НООC-CН(ОН)-CH3
НООC-CН(ОН)-CH3  НООC-C(О)-CH3
НООC-C(О)-CH3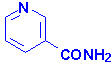




 R-CH2-CH2-COOH
R-CH2-CH2-COOH 


