
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Энергия активации. Уравнение Аррениуса.
Ур.Аррениуса устанавливает зависимость константы скорости хим.реакции от температуры. K=Ae-Ea/RT Энергия активации- минимальное кол-во энергии, необходимое сообщить системе, чтобы произошла реакция. Если известны K1 и K2 для температур T1 и T2, то энергия активации рассчитывается по формуле Аррениуса: lg Уравнение показывает, что зависимость lg (график) Чем меньше энергия активации, тем больше скорость реакции. Скорость энергии активации зависит от числа эффективных столкновений.
Катализ и катализаторы. Гомогенный, гетерогенный и микрогетерогенный катализ. Изменение скорости реакции при участии катализаторов заключается в снижении энергии активации протекающего процесса по сравнению с энергией активации соответствующей некатализируемой реакции. Катализаторы-вещества, изменяющие скорость реакции.\ Все каталитические реакции можно разделить на: Гомогенный катализ (в одной фазе). 2SO2+O2 SO2+NO2=SO3+NO NO+1/2O2=NO2 Гетерогенный катализ-протекает на поверхности раздела двух фаз (на поверхности катализатора). 2H2O Гетерогенные каталитические реакции протекают в несколько стадий: -приближение реагентов к поверхности катализатора -адсорбция и ориентация к поверхности катализатора -деформация связей в молекулах -химические превращения активных молекул -десорбция и удаление продуктов реакции с поверхности катализатора Микрогетерогенный катализ-связан с ферментативными процессами.
Ферменты как биологические катализаторы и их классификация. Ферменты представляют собой белки со строго специализированными функциями. В растворах, в которых существуют ферментативные процессы, нет типичной гетерогенности, т.к. нет четко выраженной поверхности раздела у фаз. Все ферменты классифицируются по характеру их действия, т.е. учитывается природа химических превращений, катализируемых данными ферментами. Согласно современной классификации все ферменты делятся на 6 больших групп: Оксидоредуктазы (окислительно-восстановительные действия) Трансферазы (каталитический перенос различных веществ) Гидролазы (катализирующие реакции гидролитического расщепления) Лиазы (катализируют присоединение групп к двойным связям или отрыв от этих групп)
Изомеразы (реакции изомеризации) Лигазы (особая группа ферментов, катализирующих соединения двух молекул, сопряженные с распадом связей АТФ)
Ферментативный катализ. Уравнение Михаэлиса-Ментен и его анализ. При изучении кинетики ферментативных реакций обычно изучают начальные скорости реакций. Зависимость скорости ферментативной реакции от концентрации субстрата: E+S V0= Ks-константа диссоциации фермент-субстрата комплекса, равная V0= Km-константа Михаэлиса. Km= Из уравнений видно, что они содержат одинаковую зависимость от концентрации субстрата, однако Ks Есть 2 предельных случая: При V0= При V0= Для большинства ферментативных реакций где участвует 1 субстрат Km=от 10-2 до 10-5 (моль/л)
Способы выражения концентрации растворов. Концентрация в объемном анализе может выражаться молярностью, нормальностью и титром раствора. Молярность показывает сколько молей вещества содержится в 1л. раствора. При одинаковой молярности разные объемы растворов содержат одинаковое число молей растворенного вещества. Нормальность показывает сколько эквивалентов растворенного вещества содержится в 1л. раствора. Растворы с одинаковой нормальностью реагируют между собой одинаковыми объемами. Растворы с различной нормальностью реагируют разными объемами. Это обратнопропорционально нормальностям. NAVA=NBVB или Титр - это количество грамм вещества, содержащееся в 1 мл. раствора. T= От нормальной концентрации к титру можно перейти по формуле: T=
|
|||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 940; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.144.32 (0.007 с.) |
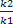 =
= 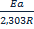 (
(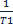 -
- 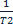 )
) дает прямую линию.
дает прямую линию.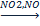 2SO3
2SO3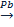 H2O+O2
H2O+O2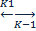 ES
ES 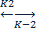 P+E
P+E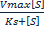
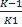
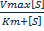
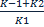
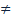 Km. Равенство может выполняться при K-1 намного больше чем K2.
Km. Равенство может выполняться при K-1 намного больше чем K2.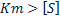
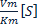 V0=Vm
V0=Vm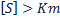
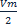
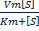 Km=
Km= 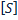
 =
= 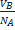
 (гр/мл.) где: m- навеска в граммах, V- объем раствора в мл., T- титр.
(гр/мл.) где: m- навеска в граммах, V- объем раствора в мл., T- титр. .
.


