
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Понятие об эквиваленте. Эквивалент сложных веществ. Изменение эквивалента веществ, при вступлении их в химические реакции. Закон эквивалентов.Стр 1 из 6Следующая ⇒
Понятие об эквиваленте. Эквивалент сложных веществ. Изменение эквивалента веществ, при вступлении их в химические реакции. Закон эквивалентов. Эквивалентом или эквивалентной массой элемента называется такая его масса, которая в данной химической реакции может замещать или присоединять 8г. O2 или 1,008г. H2. Теперь эквивалентом элемента называют такое его количество, которое взаимодействует с 1 молем атомов водорода. Например, в соединениях HCl, H2S, NH3, CH4 эквивалент хлора, серы, азота и углерода равен соответственно 1, 1/2, 1/3 и 1/4 моль. Масса 1 эквивалента элемента называется эквивалентной массой. В приведённых выше примерах эквивалентная масса хлора равна 35,5 г/моль, серы — 16 г/моль, азота — 4,67 г/моль, углерода — 3 г/моль. Эквивалент элемента можно определить соотношением: Э= Согласно закону эквивалентов, который был открыт в результате работ И. В. Рихтера, массы реагирующих веществ и m2 прямопропорциональны их эквивалентам э1 и э2: Например, в реакции NaOH+HCi=NaCl+H2O эквивалентом будет реальная частица — ион Na+, а в реакцииZn(OH)2+2HCl=ZnCl2+2H2O эквивалентом будет мнимая частица1/2Zn(OH)2.
Теоретические основы объемного анализа. Классификация методов объемного анализа по реакции, лежащей в их основе и по способу титрования. Расчеты, применяемые в объемном анализе. Концентрация в объемном анализе может выражаться молярностью, нормальностью и титром раствора. Молярность показывает сколько молей вещества содержится в 1л. раствора. При одинаковой молярности разные объемы растворов содержат одинаковое число молей растворенного вещества. Нормальность показывает сколько эквивалентов растворенного вещества содержится в 1л. раствора. Растворы с одинаковой нормальностью реагируют между собой одинаковыми объемами. Растворы с различной нормальностью реагируют разными объемами. Это обратнопропорционально нормальностям. NAVA=NBVB или Титр - это количество грамм вещества, содержащееся в 1 мл. раствора. T= От нормальной концентрации к титру можно перейти по формуле: T= Кислотно-основное титрование основано на применении реакций нейтрализации. Основным уравнением процесса нейтрализации в водных растворах является взаимодействие ионов гидроксония с ионами гидроксида, сопровождающееся образованием слабодиссоциированных молекул воды: Н3O+ + ОН- = 2Н2О.
Перманганатометрическое титрование основано на взаимодействии стандартного раствора перманганата калия с раствором восстановителя. В основе йодометрического метода титрования лежит реакция: I2+2е-=2I-
Йодометрия. Определение содержания чистой аскорбиновой кислоты в витамине C. В основе метода лежит реакция: I2+2е-=2I- В отличие от таких окислителей, как перманганат калия или дихромат калия, свободный йод является относительно слабым окислителем. Наоборот, йодиды, содержащие ионы I-, значительно более сильные восстановители, чем ионы Cr+3 и Mn+2. Это показывает, что существует ряд восстановителей, способных окисляться свободным йодом. Имеется также ряд окислителей, способных восстанавливаться йодом. Такие окислители по отношению к иону йода будут направлять реакцию в сторону выделения свободного йода: 2I--2е-=I2. Очень чувствительным индикатором в йодометрии является раствор крахмала, который дает с йодом непрочное соединение интенсивно синего цвета. Йодометрическое титрование нельзя проводить в щелочной среде, т.к. йод реагирует со щелочами: I2+2OH-=IO-+I-+H2O. Присутствие же гипойода IO- недопустимо, т.к. он является более сильным окислителем чем йод и окисляет тиосульфат частично до сульфата: S2O3-2+4IO-+2OH-=4I-+2SO4-2+H2O. Аскорбиновую кислоту можно определить с помощью титрования йодом его раствора с добавленным раствором крахмала, после чего вычисляется процентное соотношение в контрольном растворе, зная взятую навеску. Буферные системы крови. Буферные системы крови представлены буферными системами плазмы крови и буферными системами эритроцитов. Буферные системы плазмы – гидрокарбонатная, белковая и фосфатная, роль последней незначительна. На их долю приходится» 44% буферной емкости крови. Буферные системы эритроцитов – гемоглобиновая, гидрокарбонатная, система органических фосфатов (фосфатная). На их долю приходится»56% буферной емкости крови.
Так как в плазме крови основную роль в связывании ионов Н+ играет гидрокарбонат – анион, его концентрация в плазме обусловливает резервную щелочность крови. Гемоглобиновая буферная система находится только в эритроцитах. Механизм ее действия связан с присоединением и отдачей кислорода. В связи с этим гемоглобин (Нв) имеет окисленную ННвО2 и восстановленную ННв формы. Гемоглобиновая буферная система в организме эффективно функционирует только в сочетании с гидрокарбонатной системой.
Понятие об эквиваленте. Эквивалент сложных веществ. Изменение эквивалента веществ, при вступлении их в химические реакции. Закон эквивалентов. Эквивалентом или эквивалентной массой элемента называется такая его масса, которая в данной химической реакции может замещать или присоединять 8г. O2 или 1,008г. H2. Теперь эквивалентом элемента называют такое его количество, которое взаимодействует с 1 молем атомов водорода. Например, в соединениях HCl, H2S, NH3, CH4 эквивалент хлора, серы, азота и углерода равен соответственно 1, 1/2, 1/3 и 1/4 моль. Масса 1 эквивалента элемента называется эквивалентной массой. В приведённых выше примерах эквивалентная масса хлора равна 35,5 г/моль, серы — 16 г/моль, азота — 4,67 г/моль, углерода — 3 г/моль. Эквивалент элемента можно определить соотношением: Э= Согласно закону эквивалентов, который был открыт в результате работ И. В. Рихтера, массы реагирующих веществ и m2 прямопропорциональны их эквивалентам э1 и э2: Например, в реакции NaOH+HCi=NaCl+H2O эквивалентом будет реальная частица — ион Na+, а в реакцииZn(OH)2+2HCl=ZnCl2+2H2O эквивалентом будет мнимая частица1/2Zn(OH)2.
|
||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 454; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.86.138 (0.008 с.) |
 где: А-атомная масса, В-валентность элемента, Э-эквивалент элемента.
где: А-атомная масса, В-валентность элемента, Э-эквивалент элемента. =
=  .
. =
= 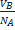
 (гр/мл.) где: m- навеска в граммах, V- объем раствора в мл., T- титр.
(гр/мл.) где: m- навеска в граммах, V- объем раствора в мл., T- титр. .
.


