Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
І. Мідь та сплави на її основіСодержание книги
Поиск на нашем сайте Мідь має червоно-рожевий колір. Кристалічна гратка – ГЦК. Поліморфні модифікації відсутні. Основні фізичні властивості міді наведені в табл.1.1. Таблиця 1.1 – Фізичні властивості міді [2]
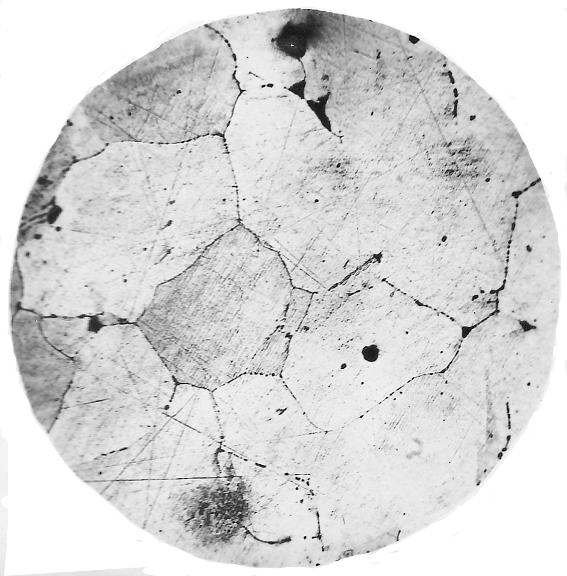
Мікроструктура міді наведена на рис.1.1. Технічно чисту мідь (ГОСТ 859-2001) маркують буквою «М» та цифрами, які вказують на ступінь чистоти міді (М00: Cu ³ 99,96 %; М0: Cu+Ag ³ 99,93 %; М1: Cu+Ag ³ 99,9 %; М3: Cu+Ag ³ 99,5 %). Букви наприкінці марки вказують на спосіб очищення від домішок або особливість використання: к – катодна, р – рафінована та розкислена, ф – розкислена фосфором, б – безкиснева мідь. Наприклад: М00к, М0б, М1р, М1ф. Хімічний склад технічно чистої міді наведено в додатку 1. Мідь діамагнітний метал. Має високу тепло- та електропровідність. За електропровідністю поступається тільки сріблу. Але завдяки широкому використанню міді її тепло- та електропровідність приймається за еталон (100 %) по відношенню до інших металів (табл. 1.2). Електропровідністьзалежить від чистоти міді (чим менше домішок, тим вище електропровідність та менше питомий електроопір). Суттєво знижують електропровідність такі домішки: P, As, Al, Fe, Sb, Sn. Найменший питомий електроопір має відпалена мідь (99,999 % Cu) очищена зонною плавкою з мінімальною концентрацією домішок – 0,0166 мкОм×м. Технічна мідь марки М00б (99,99 % Cu) характеризується максимальною електропровідністю [1].
а
б Рисунок 1.1 – Мікроструктура міді в литому стані (а), ´340 та після деформації і рекристалізаційного відпалу (б), ´300 [2] Таблиця 1.2 – Електро- та теплопровідність деяких металів по відношенню до міді [4]
Теплопровідність міді суттєво знижують домішки та легувальні елементи, а також температура (з підвищенням температури теплопровідність зменшується). Висока теплопровідність міді погіршує її зварюваність. Мідь має достатньо високу корозійну стійкість, особливо в прісній і морській воді. Проте сильно кородує в мінеральних кислотах (HNO3, HClO4 та інші), в кислих розчинах хромистих солей та під дією сірки та її сполук; також швидко руйнується в концентрованій сірчаній кислоті, особливо при нагріванні. Мідь погано опирається дії хлористого амонію, лужних ціаністих сполук. Мідь активно взаємодіє з розплавленим їдким натром при температурах ³ 350°С. Гідрооксид амонію та вологий аміак найбільш агресивні речовини для міді. При звичайній температурі сухе повітря та вода не діють на мідь і вона зберігає свій колір. При нагріванні на повітрі мідь активно взаємодіє з киснем і на її поверхні утворюються оксиди: до 100°С оксид CuO (чорного кольору), вище 600 °С оксид Cu2O (червоного кольору). На поверхні міді у вологому повітрі утворюється оксид Cu2O темно-червоного кольору. Суміш волого повітря та СО2 призводить до утвореня на поверхні міді нальоту зеленуватого кольору: карбонат CuCO3×Cu(OH)2. Мідь є катодом по відношенню до більшості металів та сплавів. В розчинах солей або кислот при контакті з міддю корозія цих металів та сплавів пришвидшується. Корозійностійкі сталі, деякі метали (Pt, Au, Pb, Sn) і їх сплави по відношенню до міді є катодами, при контакті з ними корозія міді значно посилюється. Чим більша різниця в електродних потенціалах, тим більше кородує мідь. Мідь добре оброблюється усіма способами обробки тиском. Сумарне обтиснення може становити 90%. При пластичній деформації ковзання відбувається по найбільш щільнопакованим площинам та напрямкам: {111} та <110>. Холодна пластична деформація міді підвищує її міцність, твердість, границю пружності але знижує характеристики пластичності та електропровідність. Особливість міді: в температурному інтервалі 300…600 °С в міді та її сплавах спостерігається різке зниження пластичності. Це можна пояснити блокуванням дислокацій домішками. Вище 600 °С дислокації відриваються від домішок. Температурний інтервал зниження пластичності зменшується з підвищенням чистоти міді (у безкисневої міді (99,99 % Cu) цей інтервал майже відсутній). Для усунення зниження пластичності в інтервалі 300…600°С мідь та її сплави розкислюють поверхнево активним елементом бором. Мідь погано оброблюється різанням. Для обробки різанням використовують інструмент виготовлений з швидкорізальних сталей із зниженим вмістом W або інструмент з твердих сплавів. Для покращення обробки різанням мідь легують телуром. Механічні властивості міді значною мірою залежать від її стану (табл.1.3). Таблиця 1.3 – Механічні властивості технічно чистої міді марки М1 [1]
У міді відсутній поріг холодноламкості. При температурах нижче 0°С мідь має більш високу міцність та пластичність ніж при кімнатних температурах (табл.1.4). Таблиця 1.4 – Механічні властивості технічно чистої міді М0б (дріт, відпалений стан) при різних температурах [1]
Кисневовмісна мідь схильна до водневої хвороби. При нагріванні міді до температур 850…900°С у відновній атмосфері (в середовищах в яких присутні Н2, СН4 та інші гази) утворюється атомарний Н, який має високу дифузійну рухомість в гратці міді. Водень взаємодіє з оксидом Cu2O. При цьому утворюються пари води, які не розчиняються в міді та утворюють мікрооб’єми з високим тиском. Це призводить до утворення несуцільностей, тріщин, зниження міцності та пластичності. Тому нагрівання міді до температур 850…900°С необхідно проводити в нейтральному або окисному середовищі. Недоліки міді: висока густина, погана обробка різанням та низька рідкотекучість. Термічна обробка міді: відпал для зняття напружень при 100…230°С та рекристалізаційний відпал при 500…700°С. Технічну мідь використовують для виготовлення мікронного дробу, провідників струму (обмотувальний дріт та кабельні вироби, підвісні струмонесучі та контактні дроти, колекторні пластини), нагрівачі, теплообмінники, холодильники, радіатори та для отримання сплавів на основі міді. За характером взаємодії з міддю домішки ділять на 3 групи: 1. Метали, які розчиняються в ГЦК гратці міді (Fe, Al, Ni, Zn, Si, Ag, Au, Pt, Cd, Mn, Sn, Sb). Ці елементи не мають суттєвого впливу на властивості міді, якщо їх вміст не перевищує кількості, що відповідає міді технічної чистоти (при більшому вмісті ці елементи є легувальними і значною мірою впливають на механічні властивості: до певних концентрацій підвищують міцність міді, не зменшуючи її пластичність, рис.1.2).
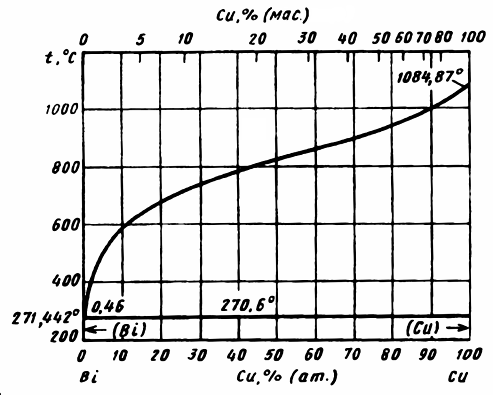
Рисунок 1.2 – Вплив елементів І групи на механічні властивості міді у відпаленому (1) та литому (2) стані [3] 2. Елементи, які майже не розчиняються в гратці міді та утворюють легкоплавкі евтектики (Bi, Pb). Розчинність Ві в міді дуже мала: не більше 0,001%, рис.1.3. В системі Cu-Bi утворюється легкоплавка евтектика (tпл = 270°С), яка складається з майже чистого Ві, рис.1.4. Присутність вісмуту окрихчує мідь: призводить до гаряче- та холодноламкості. Тому концентрацію вісмуту в міді обмежують до 0,003%. Для зв’язування Ві в тугоплавкі сполуки вводять Li, Ca, Ce, Zr, Mg.
Рисунок 1.3 – Діаграма стану Bi-Cu [16]
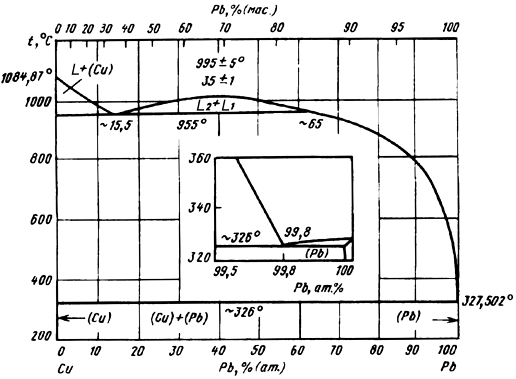
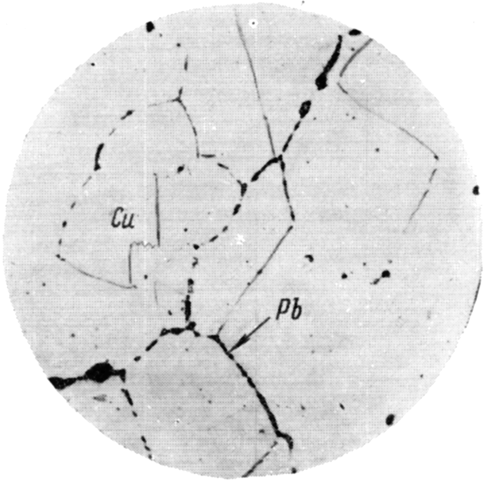
Рисунок 1.4 – Мікроструктура литої міді (0,2%Ві), ´200 [2] В системі Cu-Pb (рис.1.5) утворюється легкоплавка евтектика (tпл = 322°С), яка складається з майже чистого Pb, рис.1.6. Свинець призводить до гарячеламкості, але покращує обробку різанням. Для зв’язування Pb в тугоплавкі сполуки вводять Ca, Ce, Zr.
Рисунок 1.5 – Діаграма стану Cu-Pb [16]
Рисунок 1.6 – Мікроструктура литої міді (0,3%Pb), ´200 [2] 3. Елементи, які утворюють хімічні сполуки (P, Se, S, O, Te, As). Ці хімічні сполуки входять до складу евтектик та окрихчують сплави міді. Наявність миш’яку в міді нейтралізує поганий вплив вісмуту, сурми та кисню але знижує електро- та теплопровідність міді. Селен з міддю утворює сполуку Cu2Se. Розчинність Se в міді при 500°С становить 0,001%. Навіть при дуже малих добавках селену в системі Cu-Se утворюється крихка евтектика
Рисунок 1.7 – Мікроструктура литої міді з домішкою сірки, ´250 [2] Мідь з телуром утворює хімічну сполуку Cu2Te. Розчинність Те в міді дуже мала (0,0075% при 800°С та 0,0003% при 600°С). В системі Cu-Te при дуже малих концентраціях телуру утворюється крихка евтектика (Cu + Cu2Te). Телур знижує пластичність при холодній та гарячій обробці тиском але покращує обробку різанням. Фосфор – основний розкислювач. Підвищує рідкотекучість міді, покращує механічні властивості та зварюваність але знижує електро- та теплопровідність міді: вміст фосфору 0,013…0,05% знижує електропровідність на 20…30%. В присутності фосфору утворюється фосфідна евтектика (a + Cu3P), рис.1.8. Гранична розчинність кисню в міді 0,008% при 1066°С, яка із зниженням температури зменшується. В системі Cu-О утворюється крихка евтектика (Cu + Cu2O) з температурою плавлення 1066°С. Мікроструктура литої міді з киснем наведена на рис.1.9, 1.10. Крихка сполука Cu2O негативно впливає на пластичність, технологічність та корозійну стійкість міді. Наявність кисню в міді ускладнює лужіння, пайку та зварювання. Також може призводити до появи водневої хвороби.
Рисунок 1.8 – Мікроструктура литої міді (12,0 %Р), ´120 (при друкуванні зменшено в 1,5 рази) [2]
а – <0,05%О (´150); б – 0,15%О (´150); в – 0,39%О (´250); г – 0,5%О (´250) Рисунок 1.9 – Мікроструктура литої міді з киснем (при друкуванні зменшено в 1,5 рази) [2]
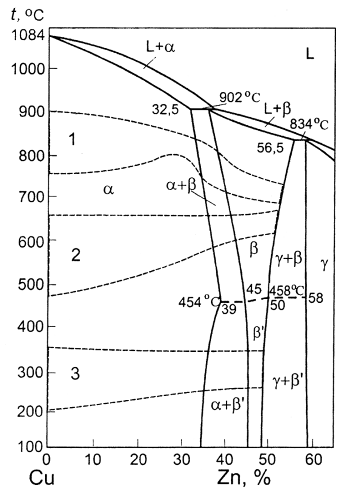
Рисунок 1.10 – Розподіл включень Cu2O після рекристалізації, ´250 [2] Класифікація сплавів на основі міді. За способом виробництва сплави міді поділяють на: деформівні та ливарні. За термічною обробкою, яка до них застосовується: на ті що зміцнюються і ті що не зміцнюються термічною обробкою. За хімічним складом: латуні, бронзи, мідно-нікелеві сплави. Сплави на основі міді мають високу тепло- та електропровідність, корозійну стійкість, добрі механічні, технологічні та антифрикційні властивості. Мідні сплави, в основному, легують елементами, які розчиняються в гратці міді: Zn, Sn, Al, Be, Si, Mn, Ni. Ці легувальні елементи підвищують міцність майже не знижуючи пластичність сплавів, а деякі елементи (Zn, Sn, Al) навіть її підвищують. ЛАТУНІ Латуні – це подвійні та багатокомпонентні сплави, в яких основний легувальний елемент – Zn (його вміст не перевищує 50% мас.). Мінімальний вміст Zn в латунях – 4% (мас.). Латуні мають добру корозійну стійкість в атмосфері та морському кліматі, в грунті. До харчових продуктів нейтральні. Латуні достатньо стійкі в розчинах луг (виключення – аміак) та в концентрованих розчинах нейтральних солей. Латуні із вмістом Zn до 15% за корозійною стійкістю близькі до міді промислової чистоти. Латуні схильні до знецинкування та сезонного розтріскування [1]. Знецинкування спостерігається при контакті латуні з електропровідним середовищем (кислі та лужні розчини). При знецинкуванні поверхня латуні розчиняється в реагенті і концентрація цинку в розчині порівняно з концентрацією в міді зростає. В результаті обмінних реакцій на катодних ділянках електрохімічно осаджується мідь у вигляді губчатої плівки. Латуні стають пористими, на поверхні утворюються плями червоного кольору, погіршуються механічні властивості. Чим більше цинку в латуні тим більша схильність до знецинкування. Для усунення схильності до знецинкування додають P, As та Sb в невеликих концентраціях. Сезонне або міжкристалітне розтріскування супроводжується появою міжкристалітної тріщини при одночасній дії розтягувальних напружень (залишкових та діючих) і специфічних хімічних реагентів (наприклад: розчини та пари аміаку, вологий сірчаний ангідрид, різні аміни, вологий діоксид вуглецю та інше). Латуні із вмістом Zn до 7% не чутливі до сезонного розтріскування. В латунях з 10…20% Zn сезонне розтріскування не спостерігається, якщо внутрішні залишкові напруження < 60 МПа. Найбільш чутливі до сезонного розтріскування латуні з концентрацією цинку наближеною до граничної розчинності в a-твердому розчині (39%) та двофазні a+b-латуні. Ці латуні стійкі до сезонного розтрікування, якщо розтягувальні напруження < 10 МПа [1]. Для визначення фазового складу подвійних латуней користуються діаграмою стану Cu-Zn (рис.1.11). При вмісті цинку до 39% латуні мають однофазну структуру a-фази. a-фаза – твердий розчин заміщення на основі міді, має ГЦК гратку. Розчинність Zn в a-фазі змінна, % (мас.): 32,5 (902°С), 39 (454°С), 34…35 (при кімнатній температурі). Рівноважна концентрація 34…35% Zn при промислових обробках не досягається, тому для оцінки фазового складу використовують максимальну розчинність 39%. b-фаза – твердий розчин на основі електронної сполуки CuZn з електронним співвідношенням 3/2, має гратку ОЦК. Утворюється за перитектичною реакцією при температурі 902°С. Високотемпературна b-фаза достатньо пластична. Тому для двофазних латуней використовують гарячу деформацію. При температурах нижче 454…468°С b-фаза переходить у впорядкований стан b®b¢ із формуванням більш твердої та крихкої b¢-фази. g-фаза – твердий розчин на основі електронної сполуки Cu5Zn8. Утворюється за перитектичною реакцією при температурі 834°С. g-фаза дуже тверда та крихка.
1 – нагрівання під обробку тиском; 2 – рекристалізаційне відпалення; 3 – відпал для зменшення залишкових напружень Рисунок 1.11 - Діаграма стану системи Cu-Zn та температурні інтервали термічної обробки [1] За структурою латуні ділять на: a-латуні, (a + b)-латуні та b-латуні, рис.1.12. З підвищенням концентрації цинку зменшується вартість латуні, покращується обробка різанням, здатність до припрацювання та зносостійкість але зменшується тепло- та електропровідність. Вплив цинку на механічні властивості латуні показано на рис.1.13. Зі збільшенням вмісту цинку міцність зростає та досягає максимуму в області (a + b)-латуні (45…47%Zn). При подальшому підвищенні вмісту Zn (однофазна область b¢-фази) міцність різко знижується. Максимальне значення відносне видовження досягає при 30…32%Zn, а потім різко знижується, коли в структурі присутня b¢-фаза. Сплави із структурою b¢-фази в холодному стані не деформуються. В промисловості переважно використовують a-латуні та (a + b)-латуні (до 45…47%Zn).
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 1206; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.011 с.) |