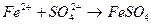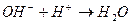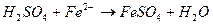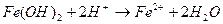Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Укажите номер правильного ответа:Содержание книги
Поиск на нашем сайте
11. Объём 0,10Н раствора азотной кислоты, необходимый для нейтрализации 20 мл 0,15Н раствора гидроксида натрия, равен ______________________ мл. 1) 30 2) 35 3) 40 4) 45
12. Осмотическое давление раствора, содержащего в 1 л раствора 3,75 г формалина при 0оС равно 283,6 кПа. Молярная масса формалина равна __________ 1) 30 2) 35 3) 40 4) 66 13. Диссоциация по двум ступеням возможна в растворе 1) угольной кислоты 3) карбоната калия 2) ортофосфата натрия 4) хлорида цинка
14. Наиболее слабым электролитом является 1) HCN 2) Al2(SO4)3 3) Ca(OH)2 4) HCl
15. Уравнение реакции практически осуществимой в водном растворе имеет вид: 1) MgSO4 + 2KOH → Mg(OH)2 + K2SO4 2) K2SO4 + Mg(NO3)2 → MgSO4 + 2KNO3 3) FeCl2 + H2SO4 → FeSO4 + 2HCl 4) BaCl2 + 2HNO3 → Ba(NO3)2 + 2HCl 16. Одним из продуктов гидролиза ортосиликата калия по второй ступени является 1) K2H2SiO4 3) KH3SiO4 2) K3HSiO4 4) H4SiO4
17. Кислая среда образуется при растворении в воде каждой из двух солей 1) Fe(NO3)3 и MnSO4 3) K2SO4 и Al2(SO4)3 2) K3PO4 и Na2S 4) BaCl2 и CuCl2
18. В уравнении для расчета константы гидролиза ацетата натрия не учитывается значение концентраций 1)
19. Только восстановительные свойства проявляют вещества 1) NH3 2) N2 3) NaNO3 4) NaNO2
20. Окислительно-восстановительную двойственность проявляют 1) K2CrO7 2) KCrO2 3) Cr 4) Cr2O3 ВАРИАНТ № 2 Часть А. Дайте полное решение заданий Укажите номер правильного ответа: 1. Массовая доля гидроксида калия в растворе, полученном при смешивании 200 г 30%-ного и 300 г 20%- ного раствора, равна ___________ г 1) 24 2) 12 3) 15 4) 18
2. При 20оС давление насыщенного пара воды равно 3,166 кПа. Давление насыщенного пара над раствором мочевины (Мr = 60) в 100 г которого содержится 5 г мочевины составляет ______________________ кПа 1) 3,117 2) 31,17 3) 93,50 4) 100
3. Уравнению реакции Fe (OH)2 + H 2 SO 4 → FeSO 4 + 2 H 2 O соответствует сокращенное ионное уравнение: 1) 2) 3) 4) 4. Кислая среда образуется при растворении в воде каждой из двух солей
1) Bi(NO3)3 и FeSO4 3) MgSO4 и K2SO4 2) Na2SiO3 и K2SiO3 4) MnCl2 и CaCl2
5. В уравнении реакции, схема которой H2S + K2Cr2O7 + Н2SO4 → S + Cr2(SO4)3 + K2SO4 + H2O, сумма коэффициентов 1) 20 2) 25 3) 30 4) 15 Дайте полное решение задания, используя ионно-электронный метод. Часть В. Выполните тестовые задания
Дополните: 1. Эквивалент основания рассчитывают по формуле Эосн – ия = _____, где ____ 2. Операция титрования – это _________________________________________ 3. Осмос – это ______________________________________________________ 4. Растворы неэлектролитов кипят при более высокой температуре по сравнению с чистыми растворителями, так, как ________________________ 5. Степень электролитической диссоциации – это ______________________ 6. С уменьшением концентрации слабого электролита, степень диссоциации его ______________, согласно закона _________________________________
7. Ионное произведение воды – это ___________________________________ 8. Раствор гидроксида калия имеет рН = 12. Концентрация основания при 100 % диссоциации равна _______________________ моль/л 9. Сложные вещества, содержащие элемент в высшей степени окисления играют роль ______________________________________________________
10. В нейтральной среде: а) избыток кислорода в частице связываем ______ с образованием _____________________________________________________ б) недостаток кислорода в частице берём из _________ с образованием __________________________________________
|
|||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 138; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.165.234 (0.006 с.) |

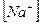 2)
2)  3)
3)  4)
4)