
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема 10. Окислительно-восстановительныеСодержание книги
Поиск на нашем сайте
РЕАКЦИИ Вариант № 1 Дополните: 1. Окислительно-восстановительные реакции – это ______________________ 2. Если алгебраическая величина степени окисления увеличивается, то протекает процесс _______, а с электронной точки зрения ________________
3. Окислитель в ходе реакции _______________, поэтому его алгебраическая величина степени окисления _________________________________________
4. Неметаллы (простые вещества) проявляют свойства _____, а с электронной точки зрения _______________________________________________________
5. Чем меньше алгебраическая величина стандартного окислительно-восстановительного потенциала (φоВ), тем сильнее выражены свойства _____
6. ЭДС = __, если ЭДС < 0, то окислительно-восстановительная реакция ____
7. В кислой среде: а) избыток кислорода в частице связываем ___________ с образованием _____________________________________________________ б) недостаток кислорода в частице берём из ________ с образованием _____________________________________________________
8. Для реакции K2Cr2O7 + KCl + H2SO4 → K2SO4 + Cr2(SO4)3 + Cl2 + H2O, если
коэффициент перед восстановителем __________________________________
9. Установите соответствие:
Выберите правильный вариант ответа:
10. Только восстановительные свойства проявляют вещества 1) KIO3 2) KIO2 3) KI 4) I2 11. Окислительно-восстановительную двойственность проявляют (два варианта ответа) ___________________________ 1) N2 2) NH3 3) NaNO2 4) NaNO3
12. В уравнении реакции Сu + HNO3 (разб.) → ______________ коэффициент перед окислителем _____________________________ 1) 8 2) 10 3) 6 4) 4 13. В уравнении реакции, схема которой Cu2S + HNO3 → Cu(NO3)2 + H2SO4 + NO + H2O, сумма коэффициентов 1) 45 2) 50 3) 60 4) 52 Дайте полное решение задания, используя ионно-электронный метод. Вариант № 2 Дополните: 1. Cтепень окисления – это ___________________________________________
2. Частица (атом, ион или молекула), отдающая электроны называется ______
3. Окислительно-восстановительные реакции называют сопряженными, так как __
4. Самые активные восстановители – это _______________________________
5. ЭДС рассчитывают по формуле _____________________________________
6. Сложные вещества, содержащие элемент в низкой степени окисления, играют роль _______________________________________________________
7. В щелочной среде: а) недостаток кислорода в частице берём из _____ с образованием _____________________________________________________ б) избыток кислорода в частице связываем _______ с образованием ______________________________________________________ 8. Для реакции K2Cr2O7 + KBr + H2SO4 → K2SO4 + Cr2(SO4)3 + Br2 + H2O, если
коэффициент перед восстановителем _________________________________ 9. Установите соответствие:
Выберите правильный вариант ответа: 10. Только окислительные свойства проявляет вещество 1) KClO4 2) KCl 3) KClO3 4) Cl2
11. Окислительно-восстановительную двойственность проявляют (два варианта ответа) 1) H2SO4 2) Na2SO3 3) H2S 4) S
12. В уравнении реакции Zn + HNO3 (сильно разб.) → _______ коэффициент перед окислителем ___________________ 1) 10 2) 8 3) 6 4) 4
13. В уравнении реакции, схема которой Fe(OH)3 +Br2 +KOH→ K2FeO4 +KBr +H2O сумма коэффициентов 1) 31 2) 40 3) 45 4) 47 Дайте полное решение задания, используя ионно-электронный метод
Вариант № 3 Дополните:
1. Cущностью окислительно-восстановительных реакций является _________
2. Если алгебраическая величина степени окисления уменьшается, то протекает процесс ______________, а с электронной точки зрения _________
3. Металлы (простые вещества) проявляют только свойства __________, а с электронной точки зрения __________________________________________
4. Сложные вещества, содержащие элемент в высшей степени окисления играют роль _______________________________________________________
5. Количественной характеристикой окислительно-восстановительной способности веществ является величина, называемая _______, обозначается буквой __ 6. Если ЭДС > 0, то окислительно-восстановительная реакция _____________
7. В нейтральной среде а) избыток кислорода в частице связываем ______ с образованием _____________________________________________________ б) недостаток кислорода в частице берём из _________ с образованием _________________________________
8. Для реакции K2Cr2O7 + KI + H2SO4 → K2SO4 + Cr2(SO4)3 + I2 + H2O, если
коэффициент перед восстановителем __________________________________
9. Установите соответствие:
Выберите правильный вариант ответа:
10. Только восстановительные свойства проявляют вещества 1) KMnO4 2) MnO2 3) Mn 4) K2MnO4
11. Окислительно-восстановительную двойственность проявляют 1) KClO4 2) KCl 3) KClO2 4) Cl2
12. В уравнении реакции Mg + H2SO4 (конц.) → ____________ коэффициент перед окислителем ____________________ 1) 5 2) 4 3) 8 4) 4
13. В уравнении реакции, схема которой H2S + K2Cr2O7 + Н2SO4 → S + Cr2(SO4)3 + K2SO4 + H2O сумма коэффициентов 1) 20 2) 25 3) 30 4) 15 Дайте полное решение задания, используя ионно-электронный метод. Вариант № 4 Дополните:
1. Окисление – это процесс __________________________________________ 2. Частица (атом, ион или молекула), принимающая электроны называется __ 3. Восстановитель в ходе окислительно-восстановительной реакции _______, поэтому его алгебраическая величина степени окисления _________________
4. Самые активные окислители – это __________________________________
5. Чем больше величина стандартного окислительно-восстановительного потенциала (φоВ), тем сильнее выражены свойства ______________________
6. Если ЭДС = 0, то окислительно-восстановительная реакция _____________
7. В кислой среде а) недостаток кислорода в частице берём из _________ с образованием ______________________________________________________ б) избыток кислорода в частице связываем _________ с образованием ______________________________________________________
8. Для реакции K2Cr2O7 + KF + H2SO4 → F2 + K2SO4 + Cr2(SO4)3 + H2O, если
коэффициент перед восстановителем __________________________________
9. Установите соответствие:
Выберите правильный вариант ответа:
10. Только восстановительные свойства проявляют вещества 1) NH3 2) N2 3) NaNO3 4) NaNO2
11. Окислительно-восстановительную двойственность проявляют 1) K2CrO7 2) KCrO2 3) Cr 4) Cr2O3 12. В уравнении реакции Ag + HNO3 (разб.) → _____________ коэффициент перед окислителем _________________________________ 1) 4 2) 5 3) 8 4) 6
13. В уравнении реакции, схема которой Na2S + KMnO4 + H2SO4 → Na2SO4 + MnSO4+ K2SO4 + H2O сумма коэффициентов перед формулами исходных веществ 1) 25 2) 29 3) 15 4) 16 Дайте полное решение задания, используя ионно-электронный метод.
|
||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 286; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.3 (0.009 с.) |


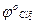 /
/ 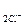 = + 1,36В,
= + 1,36В, 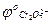 /
/ 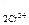 = 1,33В; ЭДС = ____, следовательно ____
= 1,33В; ЭДС = ____, следовательно ____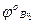 /
/ 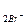 = + 1,06В,
= + 1,06В,  O2 + 4NO2 + 2CuO
O2 + 4NO2 + 2CuO
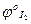 /
/  = 0,54В,
= 0,54В, 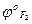 /
/ 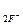 = 2,85В,
= 2,85В, 


