
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Чем глюкоза по хим свойствам отличается от сахарозы. Что такое крахмал и целлюлоза, чем они отличаются.
Сахароза образована из остатков глюкозы и имеет циклическую форму
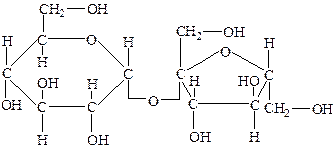
И сахароза поэтому может проявлять только свойства многоатомных спиртов, реагировать с натрием, с Cu(OH)2, азотной кислотой, а глюкоза имеет как линейную, так и циклическую форму, в линейной форме глюкоза имеет альдегидную группу, поэтому в отличие от сахарозы может реагировать еще с водородом и вступать в реакцию серебряного зеркала. Также сахароза может подвергаться гидролизу с распадом до глюкозы. Глюкоза является моносахаридом – простейшим сахаром, сахароза – дисахаридом – так как состоит из 2-х остатков глюкозы. Крахмал и целлюлоза являются полисахаридами и полимерами, так как состоят из огромного числа остатков глюкозы. Крахмал образуется из α – глюкозы, имеет сетчатую разветвленную структуру, поэтому хорошо набухает в воде, из него варят клей, так как в горячей воде образует клейкое вещество. Крахмал имеет непрочную хрупкую структуру, легко перемалывается, входит в состав клубней картофеля и других злаковых растений и плодов. При добавлении йода крахмал синеет – качественная реакция на крахмал. Крахмал способен подвергаться гидролизу до декстринов, амилопектина, и потом до глюкозы Целлюлоза образуется из β – глюкозы, имеет линейную прочную структуру, образует клетчатку, кору, древесину, не подвергается гидролизу, в в воде набухает но очень ограниченно и долго, не растворяется в воде в отличие от крахмала, может реагировать только с азотной кислотой в жестких условиях, горит при сжигании. Написать формулы гомологических рядов алканов, алкенов, алкинов, диенов, аренов, одноатомных и многоатомных спиртов, альдегидов, карбоновых кислот, аминов, сложных и простых эфиров, углеводов. Кто из них является изомерами. CnH2n+2 – алканы CnH2n – алкены и циклоалканы CnH2n-2 – алкины и диены CnH2n-6 – арены CnH2n+2О – одноатомные предельные спирты и простые эфиры CnH2nО – альдегиды и кетоны CnH2nО2 – карбоновые кислоты и сложные эфиры Cn (H2О) n – углеводы CnH2n+1NH2 – амины Аминокислоты изомерны нитро алканам
Кто такие гомологи. Гомологи – это вещества, относящиеся к одному классу, отличающиеся на одну или несколько –СН2 – групп. Гомологи входят в один класс соединений
Что такое карбонильная, карбоксильная, амино, нитро, сульфо, гидроксильная, альдегидная группы, у кого они есть. NO2 – нитро SO3H – сульфо NH2 – амино (амины и аминокислоты) -C=O – альдегиды и кетоны Н-С=О – альдегидная (альдегиды) -COOH – карбоксильная (карбоновые кислоты и аминокислоты) -OH – гидроксильная (спирты, углеводы)
Какие ионы могут одновременно существовать в растворе? Что это значит?
Одновременно могут существовать в растворе только те ионы, которые при соединении друг с другом не будут давать газ осадок воду или другое малодиссоциируещее вещество. Например, Na+ и Cl- в растворе при соединении образуют соль NaCl, которая хорошо растворима, не является газом, поэтому эти ионы могут существовать отдельно в растворе, а например ионы H+ и СО32- при соединении образут Н2О и СО2, воду и газ, поэтому данные ионы не могут существовать вместе в растворе, так как сразу переходят в вещества, которые уже не распадаются обратно на эти ионы, то есть вода и угдекислый газ
Знать основные степени окисления, которые проявляют элементы с 1 по 8 группу.
Щелочные металлы +1 Щелочноземельные металлы +2 Cu +1, +2 Hg +1,+2 C -4, +2, +4 Si -4,+4 P -3,+1, +3, +5 N -3,-2,-1,+1,+2,+3,+4,+5 S -2,+2, +4, +6 Cl -1,+1,+2,+3,+4,+5,+6,+7 F -1 Fe +2,+3 Pb +2,+4 Mn +2,+3,+4,+5,+6,+7 Cr +2,+3,+6 O -1,-2 71. Основные сильные окислители и восстановители в неорганической химии Сильные восстановители – NH3, H2S, K2S, K2SO3, KI, HI, СО, все металлы Сильные окислители – KMnO4, K2Cr2O7, K2CrO4, H2SO4 (к), HNO3, KClO4, О2, О3, все галогены Окраски индикаторов в разных средах Среда |
Индикатор | ||||||||
| лакмус | фенолфталеин | метилоранж | ||||||||
| нейтральная | фиолетовый | бесцветный | оранжевый | |||||||
| кислая | красный | бесцветный | красный | |||||||
| щелочная | синий | малиновый | желтый | |||||||



