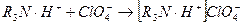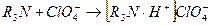Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Занятие № 7. Методы количественного анализа.
Методы титрования. Метод нейтрализации. а) алкалиметрия б) ацидиметрия в) нейтрализация в неводной среде. Нейтрализация в водной и неводной среде – наиболее широко применяемый в фармацевтическом анализе метод. Его используют для определения более 40% фармакопейных лекарственных веществ. В основе метода лежит реакция нейтрализации. Титрование в водной среде заключается в том, что растворимые в воде вещества, обладающие кислыми свойствами, титруют растворами гидроксида натрия (алкалиметрия), а вещества основного характера титрованными растворами хлористоводородной или серной кислот (ацидиметрия). Точка эквивалентности при титровании в водной среде может находиться в кислой или щелочной областях значений рН. Это зависит от природы определяемого вещества и условий титрования. Наиболее часто используемые в фармакопейном анализе индикаторы при титровании водных растворов кислот и оснований: метиловый оранжевый (3,1 – 4,4); метиловый красный (4,8 – 6,0); бромтимоловый синий (6,0 – 7,6); феноловый красный (6,4 – 8,0); фенолфталеин (8,2 – 10,0); тимолфталеин (9,4 – 10,6). Ацидиметрию применяют для определения натриевых солей неорганических и органических кислот (натрия гидрокарбонат, натрия тетраборат, калия ацетат, натрия бензоат, натрия салицилат, натрия n-аминосалицилат, кофеина-бензоат натрия и др.). Используя в качестве титранта хлористоводородную кислоту, определяют натриевые соли барбитуратов. Основные свойства в водных или спиртовых растворах проявляют ряд органических оснований (гексаметилентетрамин, амидопирин) и алкалоидов (кодеин, цитизин). Их также титруют кислотами:
Алкалиметрию используют для количественного определения лекарственных веществ, представляющих собой неорганические (хлористоводородная, борная) и органические (уксусная, лимонная, глутаминовая, аскорбиновая, никотиновая) кислоты, а также вещества сложной гетероциклической структуры, содержащие в молекуле карбоксильную группу (салюзид):
Соли органических оснований (в том числе алкалоидов, витаминов) определяют по связанной (НА) хлористоводородной, азотной или фосфорной кислоте (хинозол, секуринина нитрат, пиридоксина гидрохлорид и др.). Титруют щелочью также лактаты, гидротартраты органических оснований:
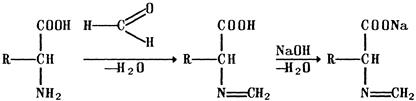
Формольное титрование (метод Сёренсена). Первичные алифатические и ароматические аминокислоты и их соли (калия и магния аспарагинат, кислота глутаминовая), взаимодействуя с раствором формальдегида, образуют азометины. При этом происходит усиление кислотных свойств аминокислоты и ее титруют раствором гидроксида натрия с индикатором фенолфталеином:
Натриевые соли титруют методом формольного титрования в среде смешанных растворителей (смесь метанола и ацетона) с использованием в качестве индикатора тимолового синего. Оксимный метод основан на нейтрализации эквивалентного количества хлористоводородной кислоты, выделившейся в результате взаимодействия гидроксиламина гидрохлорида с кетопроизводными:
Оксимный метод применяют для определения бициклических терпенов (камфора) и стероидных соединений, содержащих в молекуле кетогруппу. Один из используемых в фармацевтическом анализе вариантов кислотно-основного титрования состоит в сочетании реакции нейтрализации с предварительной этерификацией или гидролизом. Титрование в смешанных растворителях, состоящих из воды и органических растворителей, применяют тогда, когда препарат плохо растворим в воде или водные растворы имеют слабо выраженные кислотные (щелочные) свойства. Титрование в среде неводных растворителей (неводное титрование) позволяет количественно определять органические вещества, обладающие кислотными и основными свойствами, но трудно растворимые в воде. Можно осуществлять выбор органического растворителя, который способен изменять силу кислотных или основных свойств анализируемого вещества. В качестве титрантов используют растворы сильных кислот или сильных оснований. Недостатком неводного титрования является необходимость иметь герметизированную титровальную установку. Работа ведется с весьма токсичными летучими растворителями. Метод неводного титрования широко используется в фармацевтическом анализе, поскольку многие синтетические и природные органические лекарственные вещества проявляют слабые основные или слабые кислые свойства.
Неводное титрование органических оснований (и их солей) выполняют, используя в качестве растворителя безводную уксусную кислоту или уксусный ангидрид. Сочетают также уксусную кислоту с уксусным ангидридом, который улучшает условия титрования. Титрантом служит раствор хлорной кислоты, а индикатором – раствор кристаллического фиолетового, тропеолина 00 или метилового оранжевого. Растворы титранта и индикатора готовят в ледяной уксусной кислоте. Слабое органическое основание (
При растворении хлорной кислоты в уксусной последняя проявляет свойства сильного сопряженного основания, образуя перхлорат- и ацетоний-ион:
Последний нейтрализует ацетат-ионы:
а перхлорат-ион взаимодействует с катионом основания:
Суммарно процесс нейтрализации слабого органического основания хлорной кислотой выглядит следующим образом:
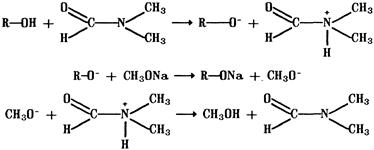
Данный процесс происходит при титровании лекарственных веществ основного характера, относящихся к числу производных пиразолона (амидопирин), пиридина (никотинамид, фтивазид); алкалоидов, представляющих собой слабые основания (резерпин, кофеин). Неводное титрование органических веществ, проявляющих кислые свойства, выполняют обычно, используя в качестве растворителя диметилформамид или его смесь с бензолом, а также этилендиамин, бутиламин, пиридин. Титрантом служит раствор гидроксида натрия в смеси метилового спирта и бензола или раствор метилата натрия (метилата лития). В качестве индикатора применяют тимоловый синий. Фенолы (R–ОH), растворенные в диметилформамиде, количественно взаимодействуют с метилатом натрия:
В таких условиях можно количественно определять не только фенолы, но и карбоновые кислоты, аминокислоты, сульфаниламидные препараты, барбитураты, производные тиоурацила, 4-оксикумарина и др. Выбор растворителя и титранта зависит от степени ионизации титруемого объекта. Более сильные кислоты (барбитал, фенобарбитал, фталазол) по ГФ титруют в среде диметилформамида раствором гидроксида натрия, а вещества со слабо выраженными кислотными свойствами (фенолы) – раствором метилата натрия.
|
||||||
|
Последнее изменение этой страницы: 2021-04-20; просмотров: 268; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.28.197 (0.008 с.) |
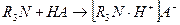
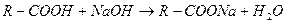
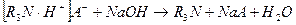

 ) при растворении в безводной уксусной кислоте становится сильной сопряженной кислотой:
) при растворении в безводной уксусной кислоте становится сильной сопряженной кислотой: .
. .
.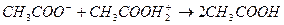 ,
,