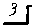Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Деление людей и животных разных видов на симпатикотоников и парасим- патикотоников также необоснованно.
Тонус симпатического нерва у различных видов животных для сердца не выражен — блокада симпатических нервов не изменяет ЧСС, в том числе и у так называемых симпатотоников (кролика, морской свинки). Не выражен у этих животных и тонус блуждающего нерва. Тонус симпатических нервов, иннервирующих сосуды, выражен не для всех органов. Расширение сосудов кожи и ЖКТ после их денервации выражено хорошо. Симпатическая денервация сосудов почки не сопровождается их расширением, у сосудов мышц вазодилататорный эффект нестойкий, а вазодилатация сосудов мозга и сердца выражена слабо. Тонус блуждающего нерва для сердца хорошо выражен только у тех животных, которые ведут активный образ жизни (много бегают), например у собаки. Хорошо выражен тонус блуждающих нервов у человека, поэтому введение в организм с лечебной целью атропина, блокирующего М-холинорецепторы, сопровождается тахикардией. Чем больше двигательная активность человека, тем выше тонус блуждающих нервов. Особенно высок он у спортсменов (бегунов) — уменьшение тонуса блуждающих нервов обеспечивает весьма быстрое учащение сердцебиений при беге, что является важным приспособительным фактором. Полагают, что наиболее характерными признаками симпатикотонии у человека являются учащенный пульс и отсутствие потливости. Однако учащение сердцебиений может быть следствием сниженного тонуса блуждающего нерва либо повышенной функции щитовидной железы. Согласно этому мнению, у ваготоников, напротив, наблюдается замедление пульса (брадикардия), повышенная потливость, склонность к покраснению кожи, желудочным расстройствам. Из всех перечисленных симптомов, с нашей точки зрения, только брадикардия может свидетельствовать о ваготонин. Брадикардия также может быть следствием и сниженного обмена веществ. Известно, что у мелких животных, например мышей, вследствие высокого обмена веществ ЧСС достигает 600 уд./мин (у собаки — 90, у человека — 60-80). Что касается желудочных расстройств, то они могут быть результатом каких-то заболеваний. Потовые железы вообще не имеют парасимпатической иннервации, поэтому потливость не может служить критерием ваготонин. Покраснение кожи также не связано с парасимпатической нервной системой, так как кожные сосуды, как и большинство других сосудов организма, не имеют парасимпатической иннервации — покраснение кожи является следствием снижения тонуса симпатических сосудосуживающих нервов или выброса катехоламинов в кровь, которые в физиологических дозах возбужда
Таким образом, большинство перечисленных признаков не может служить критерием деления людей на симпати- котоников и парасимпатикотоников. 7.10. Трофическое действие нервной системы Трофическое действие эфферентных волокон. В экспериментах на собаках И.П. Павлов обнаружил веточку симпатического нерва, идущую к сердцу, раздражение которой вызывает усиление сердечных сокращений без изменения их частоты (усиливающий нерв Павлова). Впоследствии было показано, что раздражение симпатического нерва, действительно, усиливает в сердце обменные процессы. Развивая идею И. П. Павлова, Л. А. Орбели и А. Г. Ги- нецинский в 20-х гг. XX в. обнаружили усиление сокращений утомленной скелетной мышцы при раздражении идущего к ней симпатического нерва {феномен Орбели—Гинецинского, рис. 7.7). Усиление сокращений утомленной мышцы в опыте Орбели—Гинецинского связано с активацией в ней обменных (трофических) процессов под влиянием норадреналина. Раздражение симпатических нервов не только улучшает функциональные характеристики скелетных мышц, но повышает возбудимость периферических рецепторов и структур ЦНС. Такое действие симпатической нервной системы Л.А.Орбели назвал «адаптационно-трофическим». Трофическое действие на ткань присуще всем нервам, но наиболее ярко оно выражено у симпатической нервной системы. Предполагается наличие трофогенов в нервных окончаниях. К трофогенам относят нуклеотиды, серотонин, катехоламины, ацетилхолин и др. (см. п. 7.10). Афферентные нервные волокна, так же оказывают трофическое действие на иннервируемые ткани. Так, стимуляция электрическим током задних корешков спинного мозга ведет к высвобождению терминалями афферентных волокон химических веществ, оказывающих специфическое действие на окружающую ткань. Такими веществами являются преимущественно нейропептиды. Наиболее часто при этом выявляются субстанции Р и пептид, генетически родственный кальцитонину.
БАВ, вырабатываемые разными клетками организма, оказывают тро- IIIM
Рис. 7.7. Повышение работоспособности утомленной изолированной икроножной мышцы фическое действие на саму нервную систему. Об этом свидетельствует явление угнетения активности ферментов, ответственных за синтез ацетилхолина в преганглионарных симпатических нейронах (они находятся в боковых рогах спинного мозга), после разрушения ганглионарного симпатического нейрона. По-видимому, имеется несколько нейрональных факторов, регулирующих рост, развитие нервных клеток и функционирование зрелых нервных клеток. Одним из таких веществ является фактор роста нервов (ФРН), выделенный из слюнных желез; продуцируется ФРН также гладкомышечными волокнами стенок внутренних органов и тканями других органов-мишеней. Обнаружено также вещество, регулирующее рост и развитие мотонейронов спинного мозга. ФРН в наибольшей степени стимулирует рост симпатических и спинномозговых ганглиев на ранних стадиях развития нервной системы. На более поздних стадиях развития и у взрослых ФРН необходим для поддержания нормальной структуры и функции симпатических нейронов. Если в организм новорожденных животных ввести антитела к ФРН, то в симпатической нервной системе развиваются дегенеративные изменения. Адаптационно-трофическое действие на ткани оказывают многие Б АВ: сложные липиды, ганглиозиды, некоторые аминокислоты, простагландины, либерины, соматостатин, энкефалины, эндорфины, брадикинин, нейротензин, ХЦК, фрагменты АКТГ, окситоцин. Понятие «трофоген», по-видимому, является собирательным.
8.1. Характеристика гормональной регуляции Общие положения. Гормоны участвуют в регуляции всех функций развивающегося и зрелого организма, и особо важную роль они играют в регуляции обменных процессов (поддерживают гомеостазис организма в целом), определяют рост и развитие детей и подростков. Гормоны (греч. hormao — приводить в движение, возбуждать) — БАВ, вырабатываемые эндокринными железами либо отдельными клетками или группами клеток (например, в поджелудочной железе, ЖКТ). Эндокринными называют железы, которые не имеют выводных протоков и выделяют свой секрет (инкрет, гормон) путем экзоцитоза непосредственно в межклеточное пространство, откуда он попадает в кровь. Гормоны вырабатываются также нервными клетками (нейрокриния) — это нейрогормоны, например гормоны гипоталамуса (либерины и статины), регулирующие функцию гипофиза (рис. 8.1). БАВ вырабатываются также неспециализированными клетками — это тканевые гормоны (гормоны местного действия, паракринные факторы, парагормоны — см. ниже). Действие БАВ непосредственно на соседние клетки, минуя кровь, называют паракринным, а действие таких веществ преимущественно на рецепторы выделившей их клетки — аутокринным (например, действие выделенного из нервного окончания медиатора на само окончание).
Действие гормонов специфично, они не могут быть заменены другими БАВ. Например, недостаток йодированных гормонов щитовидной железы сопровождается недоразвитием ЦНС, и никакое другое БАВ не может заменить гормоны щитовидной железы. Гормоны обладают чрезвычайно большой биологической активностью — их концентрация в крови измеряется пикограммами и микромолями. Классификация гормонов По месту действия гормоны делят на две группы: 1) эффекторные гормоны, действующие на клетки-эффекторы (например, инсулин, регулирующий обмен веществ в организме, увеличивает синтез гликогена в клетках печени, увеличивает транспорт глюкозы и других веществ через клеточную мембрану, повышает интенсивность синтеза белка); 2) тропные гормоны (тропины), действующие на другие эндокринные железы и регулирующие их функции: например,
По химической природе гормоны делят на три группы: 1) белки и полипептиды (гормоны гипоталамуса, гипофиза, поджелудочной железы); 2) производные аминокислот (гормоны щитовидной железы, эпифиза, катехоламины); 3) стероиды (кортикоиды, половые гормоны). По эффекту различают стимулирующие и тормозящие гормоны. По механизму действия на к л е т к и-ми ш е н и гормоны подразделяют на: действующие посредством мембранных рецепторов (липофобные гормоны) и действующие с помощью внутриклеточных рецепторов (липофильные гормоны). Липофильные гормоны — растворимые в жирах, но нерастворимые в воде (стероидные гормоны — кортикоиды и половые, а также гормоны щитовидной железы) — все эти гормоны проникают через клеточные мембраны; липофобные гормоны — нерастворимые в жирах, но растворимые в воде (гормоны гипоталамуса, гипофиза, поджелудочной железы, катехоламины) — эти гормоны не проникают через клеточные мембраны. Виды влияний гормонов. Гормоны ока- зывают два вида влияний на органы, ткани и системы организма: функциональное (играют весьма важную роль в регуляции функций организма) и морфогенетическое — обеспечивают морфогенез (рост, физическое и половое развитие, созревание структур ЦНС).
Функциональное влияние гормонов: пусковое, модулирующее и пермиссивное. Пусковое влияние — это способность гормона запускать деятельность эффектора (например, только в присутствии АДГ стенки дистального сегмента нефрона проницаемы для воды). Модулирующее влияние — изменение интенсивности деятельности органа. Например, стимуляция адреналином деятельности сердца, которая осуществляется и без адреналина. Модулирующее влияние реализуется за счет изменения интенсивности протекания биохимических процессов в органах и тканях (например, угнетение секреции желудочных желез под действием соматостатина). Модулирующим влиянием гормонов является также изменение чувствительности ткани к действию других гормонов. Например, фолликулин усиливает действие прогестерона на слизистую оболочку матки, тиреоидные гормоны усиливают эффекты катехоламинов. Пермиссивное влияние — способность одного гормона обеспечивать реализацию эффекта другого гормона. Например, инсулин необходим для проявления действия соматотропного гормона (СТГ), пролактин свое действие на молочную железу оказывает после предварительного влияния эстрогенов и прогестерона. Морфогенетическое влияние гормонов (нарост,физическое и половое развитие) подробно изучается другими дисциплинами (гистология, биохимия) и лишь частично — в курсе физиологии (см. п. 8.2-8.7). Оба вида влияний гормонов (морфогенетическое и функциональное) реализуются с помощью метаболических процессов, запускаемых посредством клеточных ферментных систем, иногда — с помощью электрофизических (например, ускорение сердцебиений при действии адреналина). Механизм действия различных гормонов. Известны положения П. Эрлиха (1911, 1913): «Вещества не действуют, не будучи связанными» как «замок» и «ключ»; «роль замка выполняют клеточные рецепторы, роль ключа — лиганд (гормон, медиатор, фармакологический препарат)». Для каждого гормона в клетках-мишенях имеется рецептор. Влияние любого гормона на клетку-мишень начинается с его взаимодействия с рецептором (рис. 8.2). Существует два основных варианта действия гормона на клетку. 1. Если клеточная мембрана непроницаема для г о р м о н а, то рецепторы расположены в самой мембране (для белково-полипептидных гормонов гипоталамуса, гипофиза, поджелудочной железы, а также катехоламинов мозгового слоя надпочечников, которые растворимы в воде, но нерастворимы в липидах). Гормонрецепторный комплекс этих гормонов активирует внутриклеточные процессы, ведущие к образованию вторых посредников, реализующих свое действие в основном через ядерный аппарат клетки. Основными из них яв-
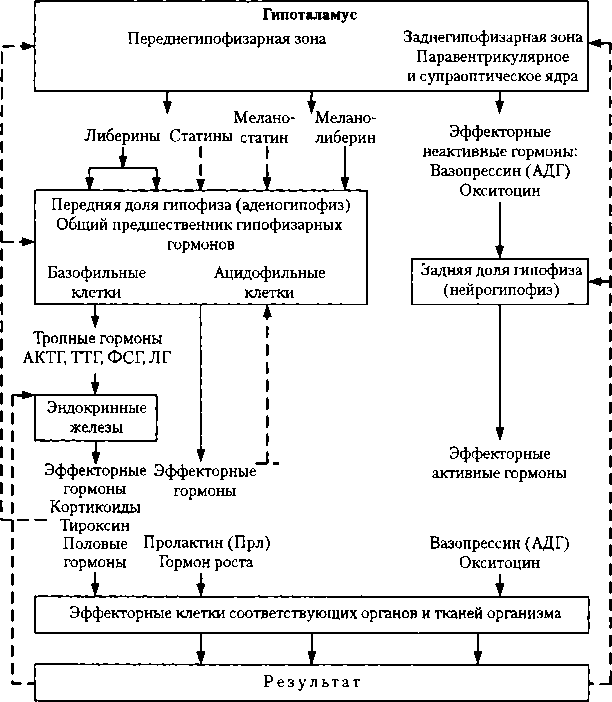
Гр Г2, Г3 — гормоны; Рр Р2, Р3 — рецепторы, избирательно связывающие гормоны ляются: 1) аденилилциклаза — цАМФ; 2) гуанилилциклаза — цГМФ; 3) фосфолипаза С — ИФ3 и ДАТ; 4) ионизированный кальций — кальмодулин (белок немышечных клеток и миоцитов гладких мышц) или тропонин С (в поперечнополосатых мышечных клетках). 2. Если клеточная мембрана проницаема для гормона (стероидные гормоны — кортикоиды и половые гормоны, а также гормоны щитовидной железы, растворимые в липидах), то он взаимодействует с внутриклеточными рецепторами. Активированные рецепторы связываются внутри клетки с последовательностями ДНК — в основном в ядре, а также в цитозоле. Рецепторы для стероидных гормонов локализуются в ядре и цитоплазме, для тиреоидных гормонов — в ядре. Рецепторы представляют собой белки, способные взаимодействовать с определенным гормоном. При взаимодействии гормона с рецептором происходит конформация G-белка, что запускает метаболические процессы. В крови гормоны находятся в двух формах: свободной — готовой к действию (активная форма) и связанной с белками (неактивная форма) — это своеобразное депо гормонов. Период полураспада гормонов обычно составляет около часа. Действие их прекращается с помощью тканевых ферментов и ферментов самих эндокринных желез, печени, почек. Многие продукты расщепления гормонов тоже активны и иногда вызывают сходные эффекты. Продукты распада гормонов выводятся главным образом почками, а также железами — слюнными, ЖКТ, потовыми и с желчью. Несколько процентов гормонов выводится из организма почкой в неизмененном виде. Регуляция выработки гормонов осуществляется согласно общим принципам, ведущим из которых является принцип обратной отрицательной связи, причем на четырех уровнях: 1) ЦНС — эндокринные железы; 2) гипофиз — эндокринные железы; 3) эндокринные железы — параметры регулируемого показателя; 4) внутриклеточная саморегуляция. 1. Регуляция на уровне ЦНС представлена на общей схеме регуляции выработки гормонов (см. рис. 8.1 и 8.3). Наивысшим уровнем регуляции выработки гормонов является лимбическая система и новая кора, при этом особо важную роль играет гипоталамус, как одна из структур лимбической системы, что осуществляется с помощью специальных гормонов: SRIF — соматостатин; GHRH — рилизинг-гормон для гормона роста гипофиза; CRH — кортикотропин-рилизинг гормон;
Рис. 8.3. Гипоталамо-гипофизарная система:
<—> — двусторонние связи в ЦНС (по К. Voigt, PIF — пролактинингибирующий фактор; GnRH — гонадотропин-рилизинг гормон; TRH — тиреотропин-рилизинг гормон. В период развития организма и в зрелом возрасте в случае относительно благоприятного средового окружения и психоэмоционального состояния, при отсутствии внешних и внутренних стрессорных воздействий центральные механизмы регуляции устанавливаются на «трофотропную» активность — на анаболизм, интенсивный рост и тканевую дифференцировку, на активацию памяти и механизмов обучаемости, на любознательность и исследовательское поведение. Этот комплекс запускается через включение нейроэндокринных цепей, ассоциированных с гормоном роста, окситоцином, ростовым пептидом, гастрином, ХЦК. Это и есть доминирующая совокупность свойств нормальной жизни и нормального развития ребенка любого возраста при ведущей роли парасимпатической активации. При возникновении стрессоров, острого дискомфорта или восприятия угрозы, эмоционального и физического напряжения включается комплекс аварийных систем выживания с доминированием компонентов ортотропной» системы с ведущим участием симпатической активации, АКТГ, катехоламинов и кортикостероидов. В растущем организме задачи развития отступают на задний план или вообще снимаются, катаболизм доминирует над анаболическими процессами. Гормональное звено в случае рефлекторной регуляции функций организма включается с помощью ВНС (это характерно для выработки адреналина мозговым слоем надпочечников; выработка тропных гормонов регулируется ЦНС с помощью нейрогормонов гипоталамуса — либерины-стимуляторы, статины-ингибиторы выработки гормонов. Симпатические нервные волокна, идущие от верхнего шейного ганглия, усиливают выработку тропных гормонов гипофизом, а парасимпатические нервные волокна, идущие от языкоглоточного нерва, напротив, угнетают их синтез. 2. Регуляция с помощью гипофиза осуществляется посредством тропных гормонов (ТТГ, АКТГ, фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов). 3. Регуляция на эффекторном уровне (эндокринные железы — параметры регулируемого показателя). Так, секреция инсулина и глюка- гона клетками островков Лангерганса регулируется уровнем глюкозы в крови. В случае снижения концентрации глюкозы в крови выработка инсулина уменьшается, выработка глюкагона клетками панкреатических островков возрастает (глюкагон увеличивает преобразование гликогена печени в глюкозу и выход ее в кровь). Если же концентрация глюкозы в крови высока, то по принципу отрицательной обратной связи стимулируется выработка инсулина, который снижает концентрацию глюкозы в крови с помощью увеличения утилизации ее клетками организма и увеличения отложения в виде гликогена в клетках печени, в результате чего снижается (нормализуется) концентрация глюкозы в крови (см. рис. 8.1). 4. В н у тр и к л е т о ч н ая саморегуляция деятельности клеток эндокринных желез по выработке гормонов генетически запрограммирована. При этом цепь реакций по выработке секрета может стимулироваться или тормозиться по принципу обратной отрицательной связи продуктами последующих реакций: недостаток синтезируемых элементов стимулирует их образование, избыток — угнетает. Роль витаминов в выработке гормонов существенна. Так, витамин А тормозит секреторную функцию щитовидной железы, витамин В усиливает активность эозинофильных клеток передней доли гипофиза и одновременно тормозит функцию базофильных клеток (см. рис. 8.1). Витамин С необходим для образования кортикостероидов, витамин £ способствует продукции половых гормонов, витамин D тормозит образование гормонов паращитовидными железами. Роль тканевых гормонов, представляющих собой биогенные амины (гистамин, серотонин), простагландины, кинины (калликреин, брадикинин) и др. Они занимают промежуточное положение между гормонами и метаболитами как гуморальные факторы регуляции. Паракринные вещества оказывают свое регулирующее влияние на клетки тканей посредством изменения их биофизических свойств (проницаемости мембран, их возбудимости), изменения интенсивности обменных процессов, чувствительности клеточных рецепторов, образования вторых посредников. В результате этого изменяется чувствительность клеток к нервным и гуморальным влияниям. Поэтому тканевые гормоны называют модуляторами регуляторных сигналов: они оказывают модулирующее влияние. Тканевые гормоны образуются неспециализированными клетками, но действуют они посредством специализированных клеточных рецепторов. 8.2. Гормоны гипофиза, эпифиза и тимуса Гипофиз состоит из передней доли (аденогипофиза) и задней доли (нейрогипофиза). В передней доле гипофиза вырабатываются тропные гормоны (ТТГ — тиреотропин, АКТГ — кортикотропин и гонадотропные гормоны — гонадотропины) и эффекторные гормоны: гормон роста (СТГ) и пролактин. Функции эффекторных гормонов аденогипофиза Гормон роста (соматотропин, СТГ) назван так потому, что он стимулирует рост организма. В пренатальном периоде и до 2 лет постнатального онтогенеза этот гормон малоэффективен. Далее СТГ стимулирует рост организма до полового созревания, после чего его влияние тормозится. Действие СТГ реализуется посредством влияния на обмен веществ, стимуляции роста эпифизарных хрящей и осуществляется при нормальном содержании гормонов щитовидной, поджелудочной и половых желез. СТГ оказывает влияние на рост через инсулиноподобные факторы роста посредством активации метаболизма. Он повышает синтез белка и снижает распад аминокислот, что сказывается на увеличении запасов белка и величине ретенции азота. СТГ угнетает окисление углеводов в тканях. Это действие в значительной мере опосредовано и через поджелудочную железу. СТГ вызывает задержку в организме фосфора, натрия, калия, кальция. Одновременно увеличивается распад жира, о чем свидетельствует нарастание в крови свободных жирных кислот. Все это приводит к ускорению роста организма. Гормон роста увеличивает выработку лимфоцитов. Влияние недостаточного питания на скорость роста детей осуществляется через систему инсулиноподобных факторов. Сами факторы и связывающие их транспортные белки и рецепторы имеют свои возрастные закономерности по интенсивности синтеза, циркуляции в крови и участию в ростовых процессах. При диагностическом исследовании гормона роста определяют его базальный уровень (около 10 нг в 1 мл) и уровень во время сна, когда происходит естественное повышение выделения данного гормона. Кроме того, используют провокацию выделения гормона, создавая умеренную гипогликемию введением инсулина или других стимуляторов. Во сне и при стимуляции уровень гормона роста возрастает в 2—5 раз. При гиперфункции гипофиза в раннем онтогенезе развивается гигантизм (у взрослого человека — акромегалия), при гипофункции — болезнь Симмондса (нанизм, карликовость). Отклонения в росте и в развитии детей являются следствием нарушения функции также других эндокринных желез, которая регулируется посредством тропных гормонов гипофиза. При врожденных формах карликовости и инфантилизма дети рождаются нормального роста и массы тела. Рост этих детей обычно продолжается в течение еще некоторого времени после рождения. Однако, как правило, с 2-4 лет начинает отмечаться отставание в росте. Тело имеет обычные пропорции и симметрию. Характерен противоречащий возрасту старческий вид — прогерия. Кожа морщинистая, образует складки. Распределение жира нарушено. Развитие костей и зубов, закрытие эпифизарных хрящей и половое созревание заторможены. Пролактин стимулирует образование и выделение молока (лактация) у матери, чему способствуют эстрогены и прогестерон (эстрогены вызывают рост протоков молочной железы, прогестерон — развитие ее альвеол). Пролактин обладает также лютеотропным действием, т.е. способствует продолжительному функционированию желтого тела и образованию им гормона прогестерона. Секреция пролактина увеличивается во время акта сосания (рефлекторный механизм). В организме подростков пролактин, действуя совместно с лютропи- ном и тестостероном, стимулирует рост предстательной железы и семенных пузырьков. Высокая концентрация пролактина, вероятно, способствует также преходящему увеличению грудных желез у мальчиков (пубертатная гинекомастия). 0-э ндорфин — опиод, участвующий в обезболивающих реакциях организма. Функция тропных гормонов аденогипофиза заключается в регуляции выработки эффекторных гормонов эндокринными железами (см. рис. 8.1 и 8.3). Адренокортикотропный гормон (АКТГ, кортикотропин) образуется в проопиомеланокортинсин- тезирующих клетках аденогипофиза (ПОМК-клетки). В этих же клетках образуется Р -эндорфин. АКТГ является физиологическим стимулятором пучковой зоны коры надпочечников, в которой образуются глюкокортикоиды. В меньшей степени выражено влияние гормона на клубочковую и сетчатую зоны. Кортикотропин, стимулируя образование глюкокортикоидов, приводит к тем же эффектам, что и глюкокортикоиды. При избытке АКТГразвивается болезнь Иценко—Кушинга ("вследствие чрезмерной стимуляции функции надпочечников). Ее характерными признаками являются ожирение, полнокровие, акроцианоз, тенденция к появлению пурпуры, багровые полосы на животе, гирсутизм, дистрофия половой системы, гипертония, остеопороз, тенденция к гипергликемии. При болезни Иценко—Кушинга типично чрезмерное отложение жира на лице (лунообразное лицо), туловище, шее; ноги остаются худыми. При недостаточности гипофиза развивается гипопитуитаризм. Вследствие понижения выработки одного или нескольких гормонов гипофиза ребенок отстает в росте с последующим проявлением карликовости. Одновременно поражаются и другие эндокринные железы. Надпочечниковая недостаточность при гипопитуитаризме проявляется слабостью, неспособностью адаптироваться к стрессорным воздействиям и пониженной сопротивляемостью к инфекциям, нередко усилением проявлений аллергической сенсибилизации. Тиреотропный гормон (ТТГ, тиреотропин) стимулирует функцию щитовидной железы, действие ТТГ на белковый, жировой, углеводный, минеральный и водный обмен осуществляется через гормоны щитовидной железы. Если удалить или разрушить гипофиз у животных, наступает атрофия щитовидной железы, а введение тиреотропина восстанавливает ее функцию. Гонадотропные гормоны (гонадотропины) — фолликулостимулирующий (ФСГ, фоллитропин) и лютеинизирующий (ЛГ, лютропин) — имеются у мужчин и у женщин. Фоллитропин у женщин стимулирует рост везикулярного фолликула в яичнике, оказывает слабое влияние на образование женских половых гормонов (эстрогенов). У мужчин фоллитропин стимулирует образование мужских половых клеток — сперматозоидов. Лютропин у женщин необходим для роста везикулярного фолликула яичника на стадиях, предшествующих овуляции, и для самой овуляции, т.е. для разрыва оболочки созревшего фолликула и выхода из него яйцеклетки, и также для образования желтого тела на месте лопнувшего фолликула; также он стимулирует образование эстрогенов. Свое действие лютропин реализует на фоне предварительного длительного воздействия фоллитропина. Лютропин стимулирует также выработку прогестерона, образование желтого тела. У мужчин лютропин способствует образованию мужских половых гормонов — андрогенов. Функция задней доли гипофиза (нейрогипофиза). В нейрогипофизе гормоны не вырабатываются. Они образуются в неактивном состоянии нейронами супраоптического и паравентрикуляр- ного ядер (рис. 8.4), и накапливаются в клетках задней доли гипофиза — пи-
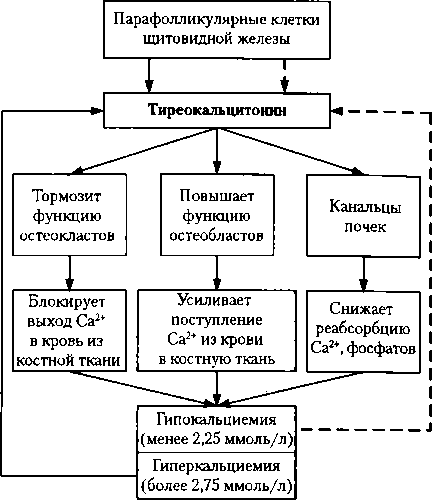
Рис. 8.4. Физиологическая роль, регуляция секреции тиреокальцитонина и содержание Са2+ в крови (по В. Ф. Киричуку, 2001, с изменениями)
туицитах, где прогормоны превращаются в активную форму. Нейросекреты транспортируются по аксонам нейронов этих ядер (по так называемому гипота- ламо-гипофизарному тракту). В пара- вентрикулярном ядре образуется преимущественно окситоцин, в супраоптическом — вазопрессин (АДГ). Вазопрессин (антидиуретиче- ский гормон, АДГ) выполняет в организме две функции. Главная из них связана со способностью вазопрессина усиливать реабсорбцию воды в собирательных трубках почек — это антидиуретическое Действие гормона. Другая функция вазопрессина связана с его влиянием на гладкую мускулатуру артериол. Однако второе название АДГ — вазопрессин — не полностью соответствует свойству этого гормона суживать сосуды. Дело в том, что в нормальных физиологических концентрациях он сосудосуживающим действием не обладает. Сужение сосудов под влиянием АДГ может наблюдаться при экзогенном введении или большом выбросе его гипофизом при значительной кровопотере. При недостаточности нейрогипофиза развивается синдром несахарного диабета, при котором с мочой теряется огромное количество воды (до 15 л/сут), так как снижается реабсорбция ее в собирательных трубках. Вследствие невыносимой жажды больные постоянно пьют воду. Окситоцин во время беременности не действует на матку, так как под влиянием гормона желтого тела прогестерона она становится нечувствительной к окситоцину. Если механически раздражать шейку матки, происходит рефлекторное выделение окситоцина, чему способствует также акт сосания. Окситоцин стимулирует сокращение миоэпителиальных клеток, способствующих выделению молока из молочных желез (секреция регулируется пролактином). Гормон эпифиза — мелатонин, представляющий собой производное аминокислоты триптофан; промежуточным продуктом синтеза мелатонина является серотонин. Мелатонин участвует в регуляции пигментного обмена за счет обесцвечивания меланофоров кожи, однако основной его эффект — торможение секреции гонадотропинов, что сдерживает половое созревание. Поэтому при гипофункции эпифиза наступает раннее половое созревание, а при гиперфункции возникают явления гипогенитализма и ожирения. Мелатонин снижает также продукцию и других гормонов: тиреоидных, надпочечниковых; выделяет вещества, тормозящие выработку гормона роста. У мальчиков к началу полового созревания происходит резкое падение уровня мелатонина в сыворотке крови. У женщин наибольший уровень мелатонина наблюдается в период менструаций, наименьший — в период овуляции. Это сопровождается соответствующими изменениями секреции эстрогенов. Непосредственным стимулом для выделения мелатонина является норадреналин, который действует через мембранные а- и 0-адренорецепторы секреторных клеток эпифиза. Норадреналин (через цАМФ и другие вторые посредники) стимулирует синтез мелатонина. Действие света тормозит синтез мелатонина, что связано с угнетением выделения норадреналина постганглионарными симпатическими волокнами, иннервирующими эпифиз. Функции вилочковой железы (тимус) Тимус на 12-й неделе пренатального развития напоминает зрелый орган, в дальнейшем продолжает расти в преи постнатальном периодах до полового созревания; его активность в этот период стимулируется тироксином и СТГ. Тимус вырабатывает несколько гормонов: тимозин, тимусовый гуморальный фактор, тимопоэтин I, тимопоэтин II, гомеостатический тимусовый гормон — это полипептиды, стимулирующие образование антител и, по-видимому, рост развивающегося организма. При увеличении тимуса развивается статус тимиколимфатикус, при этом разрастается также лимфатическая ткань, наблюдается одутловатое пастозное лицо, тучность, тонкая кожа, беспричинная рвота, изменение дыхания, иногда сердечно-сосудистый коллапс. После полового созревания происходит быстрая атрофия тимуса под влиянием главным образом эстрогенов и, в меньшей степени, андрогенов. В тимусе происходит дифференцировка лимфоидных стволовых клеток в Т-лимфоциты. В случае недоразвития тимуса у детей нарушаются клеточные иммунные реакции, в результате чего возникают гнойные инфекции. 8.3. Функции гормонов щитовидной железы Щитовидная железа вырабатывает йодированные гормоны тироксин (Т4) и трийодтиронин (Т3) и нейодированный гормон тиреокальцитонин. Тироксин и трийодтиронин оказывают очень сильное влияние на рост и развитие детского организма. Их действие определяет нормальный рост, нормальное созревание скелета (костный возраст), нормальную дифференцировку клеток головного мозга и интеллектуальное развитие, нормальное развитие структур кожи и ее придатков, увеличение потребления кислорода тканями, ускорение использования углеводов и аминокислот в тканях. Содержание тироксина в крови больше, чем трийодтиронина. Однако в тканях большинство молекул Т4 преобразуются в Т3 путем дейодирования. Активность Т3 в 4—10 раз больше, чем Т4, так как последний прочнее связан с белками плазмы крови, в основном с глобулинами, которые транспортируют эти гормоны. В клетках всех тканей организма под влиянием тиреоидных гормонов синтезируется большое количество ферментов, структурных и транспортных белков, что стимулирует обмен белков, жиров и углеводов, рост и развитие организма, созревание ЦНС. При гипофункции щитовидной железы во внутриутробном и раннем постнатальном периодах наблюдается кретинизм, основными проявлениями которого являются задержка роста и умственная отсталость. При гиперфункции щитовидной железы ускоряется рост, отчего дети в раннем возрасте значительно выше своих сверстников. Однако, в связи с ускорением закрытия эпифизарных хрящей, длительность процесса роста укорачивается, и окончательный рост взрослых может быть даже меньше нормы. При гиперфункции щитовидной железы возникает нервозность, тревожность, раздражительность. Отмечается высокая утомляемость, мышечный тремор и Другие симптомы, свидетельствующие о нарушении функции ЦНС; отмечаются нарушения сна, памяти, эмоциональная неустойчивость и другие патологические изменения высшей нервной деятельности. Тиреоидные гормоны увеличивают метаболическую активность всех тканей организма. При гиперфункции щитовидной железы у человека основной обмен может возрастать на 60-100 %. Под влиянием гормонов щитовидной железы в организме заметно уменьшаются запасы жира и гликогена в печени, при этом наблюдается исхудание. Гормоны щитовидной железы увеличивают ЧСС, дыхательных движений, повышают потоотделение, фибринолитическую активность крови. Тиреоидные гормоны уменьшают образование в печени, почках, легких и сердце факторов, участвующих в процессе свертывания крови, и увеличивают синтез антикоагулянтов, а также веществ, стимулирующих фибринолитические свойства крови. Посредством простагландинов и циклических нуклеотидов тиреоидные гормоны угнетают адгезивную и агрегационную способность — все это ухудшает гемостаз при повреждении сосудов.
|
||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-12; просмотров: 121; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.55.14 (0.08 с.) |