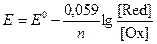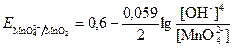Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Окислительно-восстановительные реакции
6.1. Основные определения Окислительно-восстановительные реакции – реакции, протекающие с изменением степени окисления атомов, входящих в состав взаимодействующих соединений. В ОВР всегда присутствует и окислитель, и восстановитель. По сути ОВР – это процесс переноса электронов от восстановителя к окислителю, т.е. электрон-донорно-акцепторные реакции Окислитель (Ox) – вещество (молекула, атом, ион), принимающее электроны, т.е. восстанавливающееся в результате реакции. Процесс принятия электронов окислителем называется восстановлением. Восстановитель (Red) – вещество (молекула, атом, ион), отдающее электроны, т.е. окисляющееся в результате реакции. Процесс отдачи электронов восстановителем называется окислением. Типы окислительно-восстановительных реакций Межмолекулярные ОВР – окислитель и восстановитель входят в состав разных молекул: С0 + О20 = С+4О2–2 Ox Red Внутримолекулярные ОВР – окислитель и восстановитель входят в состав одного вещества: KN+5O3–2 = KN+3O2 + O20 Ox и Red ОВР диспропорционирования – атомы одного и того же элемента, находящиеся в одной степени окисления, в ходе окислительно-восстановительной реакции одновременно выступют в качестве окислителя и восстановителя, при этом из одной промежуточной степени окисления получаются две, большая и меньшая: Cl20 + 2NaOH = NaCl–1 + NaOCl+1 + H2O Ox и Red ОВР конпропорционирования – атомы одного и того же элемента, находящиеся в разных степенях окисления, одновременно играют роль окислителя (если находятся в большей степени окисления) и восстановителя (если находятся в меньшей степени окисления), при этом из двух разных степеней окисления этого элемента образуется одна промежуточная: 2H2S–2 + S+4O2 = 3S0 + 2H2O Red Ox Метод полуреакций Метод полуреакций используют для нахождения коэффициентов в ОВР, протекающих в водном растворе. В этом методе учитывается количество электронов, участвующих в процессах окисления-восстановления между реально существующими частицами в растворе (молекулами и ионами) или, другими словами, учитывая процессы электролитической диссоциации. Уравнивание ОВР методом полуреаций можно описать следующей последовательностью.
1. Определить потенциальный окислитель и восстановитель. 2. Определить продукты реакции, т.е. то, во что переходят окислитель и восстановитель. 3. Исходя из этого, написать полуреакции, соответствующие окислению восстановителя и восстановлению окислителя, учитывая при этом среду, в которой протекает реакция. 4. Свести материальный баланс полуреакций, а затем и электронный баланс, подсчитав заряды в обеих частях уравнений. 5. Все дальнейшие действия с полуреакциями осуществлять, представляя их алгебраическими уравнениями. Количество электронов, ушедших от восстановителя при его окислении, должно быть равно количеству электронов, принятому окислителем в процессе восстановления. Поэтому домножая эти уравнения (полуреакции) на количество электронов и складывая их, получаем реакцию в ион-молекулярном виде. После приведения подобных членов и введения ионов в левую и правую части, получаем ОВР. Пример 1, кислый раствор. KMnO4 + NaNO2 + H2SO4 → MnSO4 + NaNO3 + K2SO4 + H2O В данной реакции, проходящей в кислом растворе (в левой части уравнения присутствует серная кислота), окислителем является перманганат калия, KMnO4, а восстановителем – нитрит натрия, NaNO2. Т.к. оба этих соединения являются сильными электролитами, то в водном растворе реальным окислителем будет перманганатный ион MnO4─, который в результате реакции превращается в сульфат марганца MnSO4, или, на самом деле, в Mn2+: MnO4─ → Mn2+ (полуреакция восстановления) Аналогично, в случае нитрита натрия: NO2─ → NO3─ (полуреакция окисления) При использовании метода полуреакций сначала необходимо уравнять количество элементов в обеих частях реакции. В кислом растворе для уравнивания кислорода и водорода можно пользоваться молекулами воды и протонами: MnO4─ + 8H+ → Mn2+ + 4H2O NO2─ + H2O → NO3─ + 2H+ Затем необходимо уравнять заряды в левой и в правой части обеих полуреакций, исходя из того, что окислитель принимает электроны, а восстановитель отдает, уравнять полуреакции между собой по электронам и сложить с учетом произведенного домножения левые части полуреакций с левыми, а правые части – с правыми. Сокращая одинаковые частицы в левой и в правой частях полуреакции, получается окислительно-восстановительная реакция в ином виде:
5 [NO2─ + H2O] ─1 – 2ē → [NO3─ + 2H+]+1 (суммарный заряд повышается на 2 единицы, следовательно, система частиц отдает 2 электрона) 2MnO4─ + 16 H+ + 5NO2─ + 5 H2 O → 2Mn2+ + 8 H2 O + 5NO3─ + 10 H+ (подчеркнутые частицы можно сократить): 2MnO4─ + 6H+ + 5NO2─ → 2Mn2+ + 3H2O + 5NO3─ Остается перенести коэффициенты из ионного уравнения в молекулярное, учитывая индексы ионов в молекулах (коэффициент перед серной кислотой равен трем, т.к. в ее состав входит два протона): 2KMnO4 + 5NaNO2 + 3H2SO4 → 3MnSO4 + 5NaNO3 + K2SO4 + 3H2O Пример 2, щелочной раствор. KMnO4 + NaNO2 + КОН → K2MnO4 + NaNO3 + H2O Метод уравнивания аналогичен случаю в кислом растворе. В случае щелочного раствора для уравнивания кислорода и водорода используются молекулы воды и гидроксидные анионы:
1 [NO2─ + 2OH─] ─3 – 2ē → [NO3─ + H2O] ─1 2MnO4─ + NO2─ + 2OH─ → 2MnO42─ + NO3─ + H2O; или в молекулярном виде: 2KMnO4 + NaNO2 + 2КОН → 2K2MnO4 + NaNO3 + H2O Пример 3, нейтральный раствор. KMnO4 + NaNO2 + H2O → MnO2 + NaNO3 + КОН В нейтральном растворе при уравнивании полуреакций по элементам в левой части записывается только вода, а в правой части либо протоны, либо гидроксидные ионы:
3 [NO2─ + H2O] ─1 – 2ē → [NO3─ + 2H+] +1 2MnO4─ + 4H2O + 3NO2─ + 3H2O → 2MnO2 + 8OH─ + 3NO3─ + 6H+ В нейтральном растворе, как правило, в правой части полученного ионного уравнения присутствуют одновременно протоны и гироксидные ионы, которые обязательно взаимодействуют между собой: H+ + OH─ = H2O. В рассмотренном примере вместо 8OH─ + 6H+ в правой части будет 6H2O + 2OH─. В результате сокращения воды получается следующая реакция: 2MnO4─ + 3NO2─ + H2O → 2MnO2 + 3NO3─ + 2OH─ 2KMnO4 + 3NaNO2 + H2O → 2MnO2 + 3NaNO3 + 2КОН Приведенная ниже таблица позволяет понять, какие частицы следует добавлять в полуреакциях для уравнивания кислорода и водорода:
В нейтральном растворе в левой части присутствует только вода. Восстановительный потенциал Для количественной характеристики окислительно-восстановительных реакций используются восстановительные потенциалы. Стандартный восстановительный потенциал Е0 – это стандартная свободная энергия полуреакции, отнесенная к одному заряду электрона в полуреакции: Ox + nē = Red где n – число электронов, участвующих в полуреакции, а F – постоянная Фарадея, равная заряду одного моля электронов, F ≈ 96500 Кл/моль. В качестве точки отсчета принят потенциал стандартного водородного электрода (р = 1 атм, 2н H2SO4 ([H+] = 1 M), Pt): H+ + ē = ½H2 E0 = 0 В В приложении в таблице № 5 приведены величины остальных потенциалов для стандартного кислого ([H+] = 1 М, pH = 0) и для стандартного щелочного ([OH─] = 1 М, pH = 14) растворов. В случае окислительно-восстановительной реакции критерием ее протекания является разница в стандартных восстановительных потенциалах окислителя и восстановителя. ∆E0 > 0 – реакция термодинамически возможна (∆G0 < 0):
Чем больше значение E0, тем выше окислительная способность окисленной формы (находящейся в левой части полуреакции) и меньше восстановительная способность восстановленной формы (находящейся в правой части полуреакции), и наоборот. Таким образом, наиболее сильные окислители имеют высокое значение Е0, а наиболее сильные восстановители – низкое значение Е0. Для определения направления протекания окислительно-восстановительной реакции так же удобно пользоваться правилом «Z». Для этого необходимо записать две стандартные полуреакции одну под другой, причем верхняя должна иметь меньшее значение E0. В этом случае восстановитель верхней полуреакции будет взаимодействовать с окислителем нижней, приводя к соответствующим продуктам ОВР: Mn2+ + 2ē = Mn E0 = –1,18 В (Mn – восстановитель)
2H+ + 2ē = H2 E0 = 0 В (H+ – окислитель) Mn + 2H+ = H2 + Mn2+ ∆E0 = 0 – (–1,18) = 1,18 В >0 Разница стандартных восстановительных потенциалов окислителя и восстановителя связаны с константой равновесия реакции:
 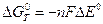
Стандартный восстановительный потенциал и потенциал при нестандартных условиях связаны между собой уравнением Нерста:
где Е0 – стандартный восстановительный потенциал (В), R – универсальная газовая постоянная (8,31 Дж/моль∙К), T – температура (К), n – число электронов, участвующих в полуреакции, F – постоянная Фарадея, [Ox] и [Red] – молярные концентрации окисленной и восстановленной форм соответственно. При T = 298 К уравнение Нерста принимает вид:
Например, для полуреакции MnO42─ + 2H2O + 2ē → MnO2 + 4OH─
Этот потенциал зависит от рН раствора. Есть потенциалы, которые не зависят от рН раствора (в полуреакцию не входит вода, окислитель и восстановитель не менят формы существования в зависимости от среды), например Na+ + ē à Na.
|
|||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 70; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.14.164 (0.035 с.) |
 2 [MnO4─ + 8H+]+7 + 5ē → [Mn2+ + 4H2O]+2 (суммарный заряд понижается на 5 единиц, следовательно, система частиц принимает 5 электронов)
2 [MnO4─ + 8H+]+7 + 5ē → [Mn2+ + 4H2O]+2 (суммарный заряд понижается на 5 единиц, следовательно, система частиц принимает 5 электронов) 2 [MnO4─]─1 + 1ē → [MnO42─]─2
2 [MnO4─]─1 + 1ē → [MnO42─]─2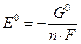
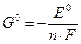 ,
,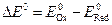
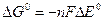

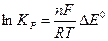
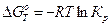
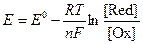 ,
,