Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Глава 1. Роль отечественных учёных в развитииСодержание книги
Поиск на нашем сайте ОСНОВЫ ХРОМАТОГРАФИИ Часть 1. Газо-жидкостная хроматография и высокоэффективная жидкостная хроматография
Методическое пособие для студентов 4 курса очного отделения фармацевтического факультета
КАЗАНЬ - 2013
ББК 24.4 УДК 543.544+615.07 Печатается по решению Центрального координационно-методического совета Казанского государственного медицинского университета
Составители: доцент, к.ф.н. Сидуллина С.А.
Рецензенты: доцент каф. фармакологии фармацевтического факультета с курсами фармакогнозии и ботаники, к.б.н. Хазиев Р.Ш., профессор КНИТУ, д.х.н. Гармонов С.Ю.
Основы хроматографии. Часть 1. Газо-жидкостная хроматография и высокоэффективная жидкостная хроматография / С.А. Сидуллина - Казань КГМУ, 2013.- 75 с. Методическое пособие предназначено для студентов 4 курса очного отделения фармацевтического факультета. Включает изложение роли отечественных учёных в развитии хроматографических методов анализа, теоретических основ хроматографии, характеристику адсорбентов, требования к подвижным фазам, аппаратуре, использование газо-жидкостной и высокоэффективной жидкостной хроматографии в качественном и количественном анализе лекарств.
©Казанский государственный медицинский университет, 2013
Содержание
4 ВВЕДЕНИЕ Хроматография (от греч. chroma, chromatos - цвет, краска), физико-химический метод разделения и анализа смесей, основанный на распределении их компонентов между двумя фазами – неподвижной (НЖФ) и подвижной (ПЖФ), протекающей через неподвижную. Хроматографический анализ является критерием однородности вещества: если каким-либо хроматографическим способом анализируемое вещество не разделилось, то его считают однородным (без примесей). В настоящее время хроматография - обширная область науки, охватывающая разнообразные хроматографические методы. Именно, хроматография изучает движение зоны вещества или группы веществ в потоке одной (или нескольких) фазы, движущейся относительно другой фазы или нескольких фаз. Только владея навыками хроматографического метода анализа можно изучать вопросы разделения близких по свойствам веществ. И только после разделения компонентов анализируемой смеси можно идентифицировать (установить природу) и количественно определять (массу, концентрацию) любыми химическими, физическими и физико-химическими методами. Существенным фактором эффективности проведения подобных хроматографических исследований является уровень профессиональной подготовки специалистов. Цель методического пособия - помочь студентам при освоении ПК-4 (способность и готовность к анализу лекарственных средств с использованием хроматографии в условиях фармацевтических предприятий и организаций, включая выбор условий хроматографирования и необходимого оборудования, с соблюдением требований международных стандартов; ПК-28 (способность и готовность к разработке, испытанию и анализу, регистрации лекарственных средств, оптимизации существующих лекарственных препаратов на основе современных технологий и методов контроля в соответствии с международной системой требований и стандартов); ПК-35 (способность и готовность проводить анализ лекарственных средств с помощью химических, биологических, хроматографических и физико-химических методов в соответствии с требованиями ГФ); ПК-36 (способность и готовность интерпретировать и оценивать результаты анализа лекарственных средств); ПК-37 (способность и готовность проводить определение физико-химических характеристик отдельных лекарственных форм, в том числе таблеток, мазей, растворов для инъекций); ПК-49 (способность и готовность к участию в постановке научных задач и их экспериментальной реализации). Задача обучающихся студентов фармацевтического факультета 3-5 курсов по вышеуказанной теме - овладеть профессиональными умениями и навыками выбора структуры исследований при создании новых перспективных лекарственных препаратов и навыками хроматографического анализа. Виды хроматографии
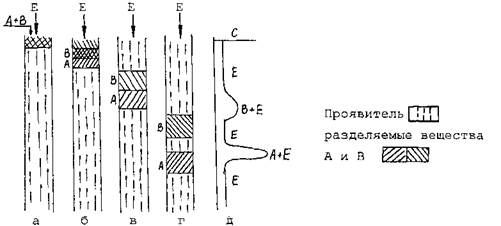
Тем самым, многообразие видоизменений и вариантов хроматографического метода требует систематизации или классификации их. В основу классификации можно положить различные признаки, а именно: агрегатное состояние фаз; природу элементарного акта; способ относительного перемещения фаз; аппаратурное оформление процесса; цель процесса. Классификация по способу Проявительная хроматография Заполненную сорбентом колонку промывают чистой жидкой или газообразной неподвижной фазой Е (рис. 2).
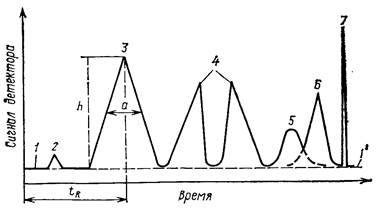
Рис. 2. Схема образования зон и распределения концентрации в зонах в проявительном методе Не прекращая потока подвижной фазы, в верхнюю часть колонки вводят порцию жидкой или газообразной анализируемой смеси, состоящей, например, из веществ А или В. Попав на слой сорбента, эти вещества сорбируются и начинают перемещаться вдоль слоя сорбента в направлении движения потока подвижной фазы (рис. 2 а) Если введенные в колонку вещества обладают различным сродством к выбранному сорбенту, то скорость перемещения каждого компонента вдоль слоя сорбента окажется различной. Вследствие этого, та зона, занятая на сорбенте слабее сорбирующимся веществом, например, веществом А, передвигается вдоль слоя сорбента быстрее зоны вещества В и постепенно уходит вперед (рис. 2 б,в). Если длина колонки достаточна, то зона вещества А оторвется от зоны вещества В и будет вымыта из колонки первой (рис. 2 г). Порядок изменения состава смеси на выходе из колонки примерно следующий (рис. 2 д). Сначала из колонки выходит подвижная фаза Е в чистом виде. Затем в потоке подвижной фазы появляется вещество А, концентрация которого возрастает, достигает максимума, а затем падает до нуля. Далее из колонки снова вымывается чистый растворитель и, наконец, появляется вещество В. Если каким-то образом зафиксировать ход изменения концентрации вымываемых из колонки веществ, получится кривая, аналогичная кривой (рис. 2 д). Такую кривую принято называть хроматограммой, а каждую часть кривой, относящуюся к изменению концентрации данного вещества – хроматографическим пиком. Очевидно, что если разделение смеси достигнуто, то число хроматографических пиков на хроматограмме должно соответствовать числу компонентов анализируемой смеси. Проявительный метод - один из наиболее распространенных из всех вариантов хроматографии. Существенным его достоинством является возможность практически полного разделения смеси на компоненты. Недостаток же состоит в значительном разбавлении компонентов смеси веществом подвижной фазы, что существенно снижает исходную концентрацию веществ на выходе из колонки. Фронтальная хроматография Заполненную сорбентом колонку промывают тем растворителем (жидкостью или газом), в котором растворены анализируемые вещества А и В, причем вещество А имеет более слабое сродство к выбранному сорбенту, чем В. Анализируемую смесь непрерывно пропускают через слой сорбента. Поступающие в верхний слой сорбента вещества А и В постепенно вытесняют находившийся в колонке растворитель, причем фронт движущейся смеси состоит из менее сорбирующегося вещества А, а затем движется исходная смесь. Таким образом, сначала вся масса сорбента насыщается менее сорбирующимся веществом А, а затем и веществом В. Хроматограмма в этом случае имеет ступенчатый характер. Вначале на выходе из колонки фиксируется чистый растворитель, затем концентрация вещества А в растворителе резко возрастает, достигает предельной величины и остается без изменений до появления вещества В. После этого состав раствора на выходе из колонки соответствует составу исходной смеси. В случае более сложной смеси её исходная концентрация достигается после насыщения сорбента всеми компонентами. Таким образом, число ступеней на хроматограмме фронтального анализа должно соответствовать числу компонентов анализируемой смеси. В отличие от проявительного метода фронтальный метод позволяет выделить из смеси в чистом виде лишь одно, наиболее слабо сорбирующееся вещество. Поэтому для аналитического разделения смеси веществ он не применяется. Однако в ряде специальных случаев, например, при необходимости выделения одного компонента в чистом виде, концентрирования примесей, а также для определения некоторых физико-химических характеристик одного компонента фронтальный метод может применяться. Элюционные характеристики (хроматографические параметры) Хроматограф (прибор для проведения хроматографии) имеет детектор — устройство для регистрации концентрации компонентов смеси на выходе из колонки. А хроматограмма — это результат регистрирования зависимости концентрации компонентов на выходе из колонки от времени. Хроматографический пик - участок хроматотраммы, соответствующий площади ограниченной функцией хроматограммы в момент выхода определяемого вещества из колонки и базовой линией. Основание пика - продолжение нулевой линии, соединяющее начало и конец хроматографического пика. На рис. 6 изображена типичная дифференциальная хроматограмма.
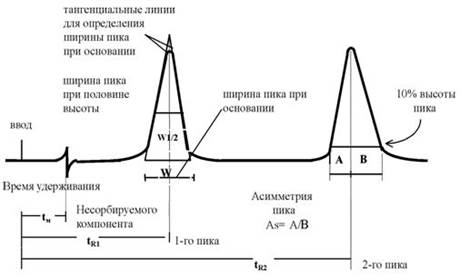
Рис. 6. Типичная дифференциальная хроматограмма: 1-1' - нулевая (базовая линия); 2-7 – пики; а и h – ширина и высота пика соответственно; tR – время удерживания. Нулевая (базовая) линия хроматограммы - линия, соответствующая нулевой концентрации анализируемых веществ в элюате. Шум - помехи, статистические флуктуации нулевой линии хроматограммы. Уровень шума складывается из статистических флуктуации всех параметров, принимающих участие в образовании сигнала детектора. Дрейф нулевой линии - постепенное смещение регистрируемое на хроматограмме. Ширина пика у основания (Wb) - отрезок основания пика, отсекаемый двумя касательными, проведенными в точках перегибов восходящей и нисходящей ветвей хроматографического пика. Ширина пика на полувысоте (Wh) - отсекаемый пиком отрезок линии, проведенной параллельно основанию пика на середине его высоты. Высота пика (h)- расстояние от максимума пика до его основания, измеренное вдоль оси отклика детектора. Площадь пика (S) - площадь хроматограммы, заключённая между пиком и его основанием. В первом приближении S = h . Wh. Мёртвое время (tM) - время пребывания несорбируемого вещества в хроматографе. На практике мёртвое время определяют от момента ввода пробы несорбируемого вещества в хроматограф до момента регистрации максимума сигнала детектора. Абсолютное время удерживания (tR) – это время пребывания исследуемого вещества в хроматографе, то есть время прошедшее от момента ввода пробы до выхода максимума концентрации определяемого компонента (соответствующего хроматографического пика). Время удерживания экспериментально определяется по секундомеру либо с помощью интегратора или системы автоматизации анализа (САА) и измеряется в минутах и секундах (n'n''). Расстояние удерживания (l R) – это расстояние на хроматограмме от момента ввода пробы до выхода пика определяемого компонента. Измеряется на хроматограмме с помощью линейки от линии старта до вершины пика (в мм). Расстояние удерживания непредставительная величина, так как она зависит от скорости перемещения диаграммной ленты и от других факторов. На рис. 7 приведена хроматограмма с указанием основных хроматографических параметров.
Рис. 7. Хроматографические параметры. tM - время удерживания несорбируемого соединения; tR1 и tR2 - абсолютные времена удерживания компонентов 1 и 2. Коэффициент асимметрии (АS) - отношение двух отрезков, образуемых на горизонтальной линии, проведённой на высоте 10% от основания пика, при её пересечении с вертикалью, опущенной из вершины пика. При этом берется отношение "тыльного" отрезка к "фронтальному": АS = А/В. Разрешение пиков (RS) - расстояние между максимумами выбранных соседних пиков, делённое на полусумму их ширин у основания (выраженных в одних и тех же единицах измерения): RS = 2 (tR2 - tR1) / (Wb1+Wb2). Разрешение как параметр, характеризующий разделение пиков, увеличивается по мере возрастания селективности, отражаемой ростом числителя, и роста эффективности, отражаемой снижением значения знаменателя из-за уменьшения ширины пиков. Экстраколоночное расширение пика (ЭКР) - размывание хроматографической зоны, происходящее в инжекторе, соединительных капиллярах, в ячейке детектора. Геометрический объём колонки (Vc) - внутреннее пространство пустой колонки. Свободный объём (Vo) - часть объёма колонки, не занятая сорбентом. Мертвый объём, (VM) – объём подвижной фазы между точкой ввода пробы и точкой её обнаружения (кюветой детектора). Мертвый объём включает в себя свободный объём колонки, объёмы устройства ввода пробы (дозатора), детектора, а также объёмы коммуникаций между ними. Удерживаемый объём (VR) – это объём газа-носителя (в см3), прошедший через хроматографическую колонку от момента ввода пробы до момента выхода максимальной концентрации определяемого вещества. То есть, объём удерживания определяют между точкой ввода пробы и точкой, при которой регистрируется максимум сигнала детектора. Объём удерживания находят по уравнению: VR = tR . Fоб., (1), где Fоб. – объёмная скорость газа-носителя, см3/мин - объём газа-носителя, протекающего за единицу времени через пенный расходомер, т.е. на выходе из колонки и при температуре колонки. При наличии специальных блоков точного задания и измерения расхода газа-носителя, с табло этих приборов снимаются показания скорости газа-носителя. Если их нет - расход замеряется с помощью мыльно-плёночного измерителя. Поэтому при вычислении удерживаемых объёмов следует использовать значение объёмной скорости, учитывающей температуру колонки и давление водяного пара при температуре измерения:
Fоб. = Fизм. . —— . 1 - —— (2), Тср. Рв где Fизм. – измеренная объёмная скорость, см3/мин; Тк – температура колонки, К; Тср. – температура окружающей среды, К; Pн2о – давление насыщенных паров воды при температуре измерения, Па; Рв – атмосферное (барометрическое) давление, Па. Перечисленные параметры, при условии использования одной и той же температуры опыта и скорости газа-носителя, являются качественной характеристикой анализируемых веществ в данных условиях на одном и том же приборе. Поэтому ими можно пользоваться для выполнения качественного анализа, только используя один и тот же прибор, строго соблюдая неизменность режима его работы. Для сопоставления получаемых значений первичных параметров удерживания с литературными данными или полученными на другом приборе или в иных условиях (для той же неподвижной фазы и температуры колонки) необходимо помнить, что на них влияют следующие факторы: а) свойства и количества HЖФ (адсорбента в газоадсорбционной хроматографии и сорбента в ГЖХ), причем в газожидкостной хроматографии влияет отдельно и HЖФ, и твердый носитель; б) температура колонки и скорость газа-носителя; в) конструктивные особенности применяемой аппаратуры; г) перепад давления газа-носителя на входе и выходе колонки. Чтобы исключить влияние некоторых факторов на первичные параметры удерживания, используют следующую группу параметров.
Детектирование Распределение концентрации на выходе из хроматографической колонки необходимо зафиксировать. Для этой цели в газовой хроматографии служат специальные устройства, называемые детекторами. Детектор помещается на пути потока газа непосредственно по выходе из колонки. Результаты записи, а следовательно, и результаты всего опыта в значительной степени зависят от правильного выбора типа детектора, его конструкции. Принятая классификация детекторов позволяет правильно установить возможности и назначение каждого из них. Применяют детекторы двух типов: дифференциальные и интегральные. В соответствии с природой детектора и механизмом возникновения сигнала различают химические, физические, физико-химические, биологические и т.д. детекторы (табл. 3.). Качественный анализ Функция колонки в газовой хроматографии сводится лишь к разделению смеси на индивидуальные компоненты. Определение их качественного состава может быть выполнено за пределами колонки. Существует два способа качественного анализа разделённой в хроматографической колонке смеси: по характеристикам удерживания и с использованием других аналитических приемов.
Таблица 3 Качественный анализ Качественные определения проводят по величинам удерживания, а количественные - по высотам или площадям пиков на хроматограммах. Характерным для жидкостной хроматографии является анализ вытекающего из колонки раствора химическими, физико-химическими или физическими методами. При этом вытекающий из колонки раствор собирают в виде отдельных фракций. Обычно для сбора фракций применяют специальные коллекторы, работающие автоматически. Собранные в коллекторные пробирки фракции подвергаются анализу. Анализируют или непосредственно собранные растворы, или же растворитель предварительно удаляют нагреванием раствора на водяной бане. Качественная идентификация компонентов анализируемой смеси производится одним из следующих методов: химическим микроанализом по характерным окраскам, появляющимся в результате взаимодействия анализируемого вещества с добавляемым реагентом, по спектрам поглощения в ультрафиолетовой или инфракрасной областях; по спектрам флуоресценции; по масс-спектрам или же по спектрам ядерного магнитного резонанса. Важнейшие характеристики хроматограммы - время удерживания и связанный с ней удерживаемый объём - отражают природу веществ, их способность к сорбции на материале неподвижной фазы и, следовательно, при постоянстве условий хроматографирования являются средством идентификации вещества. Для идентификации вещества по хроматограмме обычно используют стандартные образцы или чистые вещества. Сравнивают время удерживания неизвестного компонента tRx с временем удерживания t RCT известных веществ. Но более надежна идентификация по измерению относительного времени удерживания. При этом в колонку сначала вводят известное вещество (внутренний стандарт) и измеряют время его удерживания tR (BC), затем хроматографически разделяют (хроматографируют) исследуемую смесь, в которую предварительно добавляют внутренний стандарт. Относительное время удерживания определяют по формуле. Количественный анализ Количественные измерения проводят, определяя концентрации вещества в каждой пробирке и суммируя полученные данные для всего объёма вытекающего из колонки раствора, содержащего определяемое вещество. Если известны начало и конец выхода раствора, содержащего определяемое вещество, то весь этот раствор сливают вместе и в нём определяют концентрацию анализируемого вещества. Таким образом, погрешность количественных измерений определяется погрешностями аналитического метода и измерения объёмов собранных порций раствора. В этом случае точность количественных определений по хроматограммам может оказаться выше точности непосредственного анализа хроматографических фракций. Электрическими или электронными интеграторами снабжены современные хроматографы. Для определения содержания веществ в пробе используют в основном три метода: метод абсолютной градуировки, метод внутренней нормализации и метод внутреннего стандарта. Метод абсолютной градуировки основан на предварительном определении зависимости между количеством введённого вещества и площадью или высотой пика на хроматограмме. В хроматограмму вводят известное количество градуировочной смеси и определяют площади или высота полученных пиков. Строят график зависимости площади или высоты пика от количества введённого вещества. Анализируют исследуемый образец, измеряют площадь или высоту пика определяемого компонента и на основании градуировочного графика рассчитывают его количество. Метод внутренней нормализации основан на приведении к 100% суммы площадей всех пиков на хроматограмме. Расчёт массовой доли в % одного компонента проводят по формуле: KASA w(a)% = ________________ (16), KASa+KbSb+...K2Si где К - поправочные коэффициенты; Sa, Sb, Si - площади пиков компонентов смеси. Этот метод даёт информацию только об относительном содержании компонента в смеси, но не позволяет определить его абсолютную величину. Метод внутреннего стандарта основан на сравнении выбранного параметра пика анализируемого вещества с тем же параметром стандартного вещества, введенного в пробу в известном количестве. В исследуемую пробу вводят известное количество такого стандартного вещества, пик которого достаточно хорошо отделяется от пиков компонентов исследуемой смеси. Проводят анализ пробы с внутренним стандартом и рассчитывают количество определяемого вещества по формуле: k(a) h(a) g(а) = ___________ g(BC) (17), K(BC) h(BC) где g(A) - количество определяемого компонента А; h(A) - высота пика компонента A; g(BC) - количество внутреннего стандарта; h(BC) - высота пика внутреннего стандарта; к(A) и k(BC) - поправочные коэффициенты. В последних двух методах требуется введение поправочных коэффициентов, характеризующих чувствительность используемых детекторов к анализируемым веществам. Для разных типов детекторов и разных веществ коэффициент чувствительности определяется экспериментально. В жидкостной адсорбционной хроматографии используется также анализ фракций растворов, собранных в момент выхода вещества из колонки. Анализ может быть проведён различными физико-химическими методами. С помощью ВЭЖХ можно определять красители, органические кислоты, аминокислоты, сахара, примеси в лекарственных веществах. Мелоксикама и консервантов
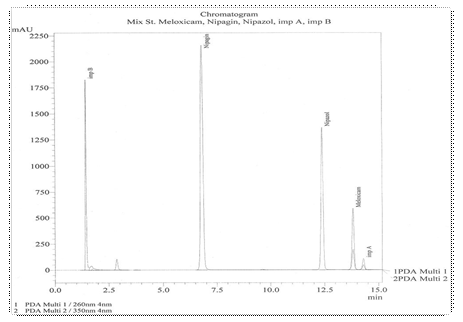
Как видно из хроматограммы (рис.11) и таблицы 5 время удерживания мелоксикама - 13 мин., для метилпарабена - 6 мин., а для пропилпарабена - 12 мин., что по значению приближается ко времени удерживания мелоксикама. Идентификация мелоксикама в геле основана на том, что при определённых условиях постоянного хроматографирования - время удерживания мелоксикама в стандартном растворе не изменяется и соответствует времени удерживания лекарственного вещества - мелоксикама в испытуемом растворе геля мелоксикама, что наглядно можно увидеть на хроматограмме, представленной на рис. 12 и 13.
Рис. 12. Хроматограмма 1% геля с мелоксикамом.
Рис. 13. Хроматограмма раствора стандартов мелоксикама, метилпарабена, пропилпарабена, примеси А и примеси Б.
Анализируя данные хроматограммы геля с мелоксикамом оценивали время удерживания и площадь пика мелоксикама, метилпарабена, пропилпарабена и других примесей, значения которых приведены в таблице 6. Таблица 6 ЛИТЕРАТУРА Обязательная 1. Беликов В. Г. Фармацевтическая химия. М., 2007. - 354 с. 2. Руководство к лабораторным занятиям по фармацевтической химии: учеб. пособие /Э.Н. Аксенова и др.; под ред. А.П. Арзамасцева.-3-е изд., перераб. - М: Медицина, 2001. - 384 с. Дополнительная 1. Березкин, В.Г., Лапин А.Б., Газовая хроматография на капиллярных колонках со сверхтолстыми пленками неподвижнойжидкой фазы: неравновесная газовая хроматография. // Доклады Академии Наук, 2002. - Т. 382. №1. - С.78-81. 2. Васянина С.А. Идентификация кислородсодержащих компонентов методом ГЖХ в напитках // Тезисы докладов I Всероссийской конференции студентов и аспирантов: Пищевые продукты и здоровье человека. В 2-х частях. - Кемерово, 2008. -Ч. 2. - С. 192-194. 3. Васянина С.А., Мирошников A.M. Разделение кислород-содержащих продуктов брожения методом ГЖХ на модифицированных полиэтилендиолах // Сб. материалов V всероссийской научн.-практ. конференции: Инновационные технологии обеспечения безопасности питания и окружающей среды. - Оренбург, 2007 - С. 67-69. 4. Винарский, B.A. Хроматография. Газовая хроматография / В.А. Винарский // Минск: Издательский центр БГУ, 2003. - 170 с. 5. Жерносек А.К., Талуть И.Е. Аналитическая химия для будущих провизоров. Часть 1. Учебное пособие / А.К. Жерносек, И.Е. Талуть; Под ред. А.И. Жебентяева. – Витебск, ВГМУ, 2003. – 362 с. 6. Лапин, А.Б., Березкин, В.Г., Некоторые закономерности изменения селективности разделения в газо-жидкостной хроматографии с программированием температуры. // Заводская лаборатория, 2003. - №4, 69. – С. 7-12. 7. Новые направления в газохроматографическом анализе фармацевтических препаратов / Рос.хим. ж. - Ж. Рос. хим. об-ва им. Д.И. Менделеева, 2003. т. XLVII. №1. С. 18-32. 8. Царев, Н.И. Практическая газовая хроматография: Учебно-методическое пособие для студентов химического факультета по спецкурсу «Газохроматографические методы анализа» / Н.И. Царев, В.И. Царев, И.Б. Катраков. — Барнаул: Изд-во Алт. ун-та, 2000. - 156 с. 9. Barry, E.F., Columns: packed and capillary; columns selection in gas chromatography, In: Grob, R.L., Barry, E.F. (Eds), Modern Practice of Gas Chromatography, N.Y.: Willey, 2004, 65-191. 10. Barry, E.F., Grob, R.L., Columns for gas chromatography, performance and selection. Wiley-Interscience, New Jersey, 2007, 298 p. 11. Barry, E.F., Grob, R.L., Columns for Gas Chromatography, Performance and Selection, John Wiley & Sons, Hoboken, New Jersey, 2007, 298p. 12. Berezkin V.G., Lapin, А.В., Lipsky, J.B., Investigation of a new field in gas chromatography: Capillary columns with a super-thick layer of stationary liquid phase II J. Chromatogr., 2005, 1084, 18-23. 13. Berezkin, V.G., Viktorova, E.N., Changes in the basic experimental parameters of capillary gas chromatography in the 20th century. // J. Chromatogr. A., 2003, 985, 3-10. 14. Igor G. Zenkevich Hydroxy Compounds: Derivatization for GC Analysis // Encyclopedia of Chromatography. June, 2005. - P. 35. ОСНОВЫ ХРОМАТОГРАФИИ Часть 1. Газо-жидкостная хроматография и высокоэффективная жидкостная хроматография
Методическое пособие для студентов 4 курса очного отделения фармацевтического факультета
КАЗАНЬ - 2013
ББК 24.4 УДК 543.544+615.07 Печатается по решению Центрального координационно-методического совета Казанского государственного медицинского университета
Составители: доцент, к.ф.н. Сидуллина С.А.
Рецензенты: доцент каф. фармакологии фармацевтического факультета с курсами фармакогнозии и ботаники, к.б.н. Хазиев Р.Ш., профессор КНИТУ, д.х.н. Гармонов С.Ю.
Основы хроматографии. Часть 1. Газо-жидкостная хроматография и высокоэффективная жидкостная хроматография / С.А. Сидуллина - Казань КГМУ, 2013.- 75 с. Методическое пособие предназначено для студентов 4 курса очного отделения фармацевтического факультета. Включает изложение роли отечественных учёных в развитии хроматографических методов анализа, теоретических основ хроматографии, характеристику адсорбентов, требования к подвижным фазам, аппаратуре, использование газо-жидкостной и высокоэффективной жидкостной хроматографии в качественном и количественном анализе лекарств.
©Казанский государственный медицинский университет, 2013
Содержание
4 ВВЕДЕНИЕ Хроматография (от греч. chroma, chromatos - цвет, краска), физико-химический метод разделения и анализа смесей, основанный на распределении их компонентов между двумя фазами – неподвижной (НЖФ) и подвижной (ПЖФ), протекающей через неподвижную. Хроматографический анализ является критерием однородности вещества: если каким-либо хроматографическим способом анализируемое вещество не разделилось, то его считают однородным (без примесей). В настоящее время хроматография - обширная область науки, охватывающая разнообразные хроматографические методы. Именно, хроматография изучает движение зоны вещества или группы веществ в потоке одной (или нескольких) фазы, движущейся относительно другой фазы или нескольких фаз. Только владея навыками хроматографического метода анализа можно изучать вопросы разделения близких по свойствам веществ. И только после разделения компонентов анализируемой смеси можно идентифицировать (установить природу) и количественно определять (массу, концентрацию) любыми химическими, физическими и физико-химическими методами. Существенным фактором эффективности проведения подобных хроматографических исследований является уровень профессиональной подготовки специалистов. Цель методического пособия - помочь студентам при освоении ПК-4 (способность и готовность к анализу лекарственных средств с использованием хроматографии в условиях фармацевтических предприятий и организаций, включая выбор условий хроматографирования и необходимого оборудования, с соблюдением требований международных стандартов; ПК-28 (способность и готовность к разработке, испытанию и анализу, регистрации лекарственных средств, оптимизации существующих лекарственных препаратов на основе современных технологий и методов контроля в соответствии с международной системой требований и стандартов); ПК-35 (способность и готовность проводить анализ лекарственных средств с помощью химических, биологических, хроматографических и физико-химических методов в соответствии с требованиями ГФ); ПК-36 (способность и готовность интерпретировать и оценивать результаты анализа лекарственных средств); ПК-37 (способность и готовность проводить определение физико-химических характеристик отдельных лекарственных форм, в том числе таблеток, мазей, растворов для инъекций); ПК-49 (способность и готовность к участию в постановке научных задач и их экспериментальной реализации). Задача обучающихся студентов фармацевтического факультета 3-5 курсов по вышеуказанной теме - овладеть профессиональными умениями и навыками выбора структуры исследований при создании новых перспективных лекарственных препаратов и навыками хроматографического анализа. Глава 1. Роль отечественных учёных в развитии
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 192; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.115 (0.017 с.) |

 Тк Рн2о
Тк Рн2о