
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
I . Приготовление питательных смесей.
1. Приготовить стоковых (концентрированные) растворы по Хогланду – Арнону из расчета, что в 10 мл концентрированного раствора каждой соли макроэлементов содержится такое её количество, какое должно содержаться их количеству в 1 литре 1 н. смеси Хогланда - Арнона. Микроэлементы вносить по 1 мл на 1 л питательной смеси (Табл. 11 и 12). 2. Составить рабочую таблицу, в которой указать необходимое количество солей на выбранный объем раствора 3.Приготовить смесь без азота. Заменить Са(NО3)2 и KNO3 на CaSO4 × 2H2O и KCl, соответственно. 4. Выполнить расчет количества KCl и CaSO4 × 2H2O. а). Определить количество калия, связанного с анионом NO3-, в соли КNO3. Грамм-молекула КNO3 (101,11 г) содержит 39,10 г калия, а в 0,50555 г КNO3 его находится х г:
101,11 г ¾ 39,1 г 0,50555 г ¾ x г отсюда x = 39,1 ´ 0,50555 / 101,11 = 0,1955 г
б). Определить количество КСl, которое необходимо внести в питательную смесь, чтобы сохранить количество калия, эквивалентное его содержанию в 0.50555 г КNO3. Грамм-молекула КСl (74,6 г) содержит 39,10 г калия, а 0,1955 г калия находится в х г КС1:
74,6 г ¾ 39,1 г x г ¾ 0,1955 г отсюда
x = 74,6 ´ 0,1955 / 39,1 = 0,373 г Итак, вместо 0,51 г KNO3, исключенного из питательной смеси, в раствор нужно внести 0,38 г КС l.
в). Определить количество кальция, связанного в соли Са(NО3)2. Грамм-молекула Са(NО3)2 (164,1 г) содержит 40,08 г кальция, а в 0,82045 г Ca(NО3)2 его находится х г:
164,1 г ¾ 40,08 г 1,18065 г ¾ x г
отсюда x = 1,18065 ´ 40,08 / 164,1 = 0,2884 г г). Определить количество CaSO4 × 2H2О, которое необходимо внести в питательную смесь, чтобы сохранить количество кальция, эквивалентное его содержанию в 0,82045 г Ca(NО3)2. Грамм-молекула CaSO4 × 2H2О (172,16 г) содержит 40,08 г кальция, а 0,2884 г находится в х г CaSO4 × 2H2О:
172,16 г ¾ 40,08 г x г ¾ 0,2884 г отсюда
x = 172,16 ´ 0,2884 / 40,08 = 1,2388 г Итак, вместо 1,18065 г Ca (N О3)2 нужно внести 1,2388 г CaSO4 × 2H2О. 5. Приготовить смесь без фосфора. Заменить соль KH2PO4 на КСl. Выполнить расчеты по приведенному выше образцу. Вместо 0,13609 г KH 2 PO 4, исключенного из питательной смеси, в раствор нужно внести 0,07 г КС l.
6. Приготовить смесь без калия. Заменить соль KH2PO4 на NaH2PO4, КNО3 на NaNО3. Выполнить расчеты по приведенному выше образцу.
Соли NaH 2 PO 4 нужно внести 0,138 г, Na NО3 – 0,42 г.
7. Приготовить стоковые (концентрированные) растворы солей из расчета, что в 10 мл стокового раствора будет содержаться количество соли необходимое для приготовления 1 - нормального раствора Хогланда – Арнона (Табл. 11). Приготовленные растворы хранить в бутылях из темного стекла.
Внимание! Стоковые растворы макросолей следует растворять и хранить в отдельных ёмкостях
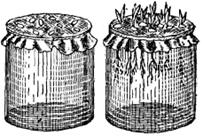
II. Закладка опыта и учет результатов. 1. Банку объемом 1 литр закрыть по всей высоте бумажным чехлом (черным внутри и белым снаружи). 2. В банку налить около 700 мл водопроводной воды. 3. Поочередно внести в банку с водой растворы солей в той повторности, в какой они указаны в прописи (Табл. 11) (CaSO4 × 2H2O внести в порошке). После прибавления очередного раствора содержимое сосуда перемешивать стеклянной палочкой. 4. Приготовить следующие растворы: а). Полная питательная смесь (Контроль); б). С исключением азота; в). С исключением фосфора; г). С исключением калия.
9. После застывания парафина, острым скальпелем проделать 4 небольшие отверстия в закрывающей банку марле. 10. Высадить в отверстия 3 выровненных проростков. При необходимости закрепить проростки негигроскопичной ватой. 11. Наклеить этикетку, на которой обозначить фамилию номер группы, вариант опыта, дату начала опыта. 12. Через четвертое отверстие в крышке долить в банку воды так, чтобы её уровень доходил до самого верха. 13. В течение месяца питательные растворы ежедневно продувать воздухом с помощью компрессора и стеклянной трубки в течение 15 - 20 мин. По мере убыли питательного раствора за счет транспирации доливать в сосуды воду до исходного уровня.
Таблица 13. Развитие растений в зависимости от
Состава питательной смеси
14. По истечении месяца провести определение необходимых параметров растений. Результаты опыта записать по форме (табл. 13). 15. Сделать выводы по результатам опыта.
Работа 20 Определение изменения pH раствора в результате поглощения ионов Корни растений способны активно смещать реакцию среды небуферных растворов, обеспечивая поддержание оптимального для роста корней pH среды (внешний pH-стат). Это является следствием постоянно осуществляемого растением катионо-анионного обмена между клетками корня и средой корнеобитания. Регулирование pH среды достигается в основном за счет передвижения в системе корень→среда и среда→корень ионов Н+, ОН- и HCOJ. Соль (NH4)2SО4 — физиологически кислая, а соль NaNО3 — физиологически щелочная. Это значит, что после пребывания растения на растворе (NH4)2SО4 реакция его смещается в кислую сторону вследствие большого поглощения иона После пребывания растения на растворе соли NaNО3 реакция смещается в щелочную сторону, так как анион Иногда сдвига реакции в щелочную сторону на растворе соли NaNO3 не наблюдается. Это может произойти вследствие выделения слабых органических кислот корневой системой. Чтобы узнать насколько подкисляется раствор за счет этих выделений, помещают третью группу растений пшеницы на дистиллированную воду, pH которой также предварительно измеряют. После пребывания растений на воде pH ее снова измеряют и производят поправку к опыту на соли NaNО3
Цель работы. Изучение изменения растениями уровня pH корнеобитаемой среды при использовании аммонийных и нитратных солей. Объекты исследования: Семидневные проростки пшеницы, выращенные на водопроводной воде Материалы и оборудование. Пипетка; стаканчики на 50 мл; магнитная мешалка; рН-метр.
Порядок работы: 1. Заранее вырастить 7-дневные проростки пшеницы на водопроводной воде, чтобы ко времени опыта у них развилась значительная корневая система. 2. Одну группу из 10 - 15 растений поместить на раствор (NH4)2SО4, содержащий 0,01 мг 3. Для определения изменения реакции раствора нужно определить исходную величину pH данного растению раствора и ту величину pH, которая устанавливается в растворе после пребывания на нем растения в течение 2 - 3 час. 4. Результаты опыта представить в виде таблицы (составить самостоятельно). 5. Сделать выводы.
Работа 21
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-11-23; просмотров: 309; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.1.158 (0.02 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
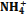 и
и 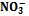 из питательного раствора
из питательного раствора поглощается растением в большей степени, нежели катион Na+.
поглощается растением в большей степени, нежели катион Na+.


