
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химическая классификация природных водСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Большинство гидрохимических классификаций природных вод.построено на чисто химическом принципе. В основу их берутся: общая минерализация лли сухой остаток, содержание главных компонентов химического состава, 44 выраженное в миллиграмм-эквивалентной или процент-эквивалентной форме, газы и микрокомпоненты, абсолютное преобладание одного или нескольких главных компонентов, или их соотношение (коэффициенты). Существуют общие и специальные схемы классификаций; Широко известны общие схемы В. И. Вернадского (1933 — 1936), И. К. Зайцева (1945, 1972), Н. И. Толстихина (1961), М. Г. Валяшко (1962), А. В. Щербакова (1962), Е. В. Пин-иекера (1966) и др. по степени минерализации. Приведем одну из последних таких схем классификации Ж. С. Садыкова, К. М. Давлетгалиевой (табл. 5.1.1), которая учитывает в значительной степени содержание ранних классификаций, но бо-- Таблица 5.1.1 Классификация подземных вод по степени минерализации (Ж. С- Садиков, К. М. Давлетгалнева, 1974)
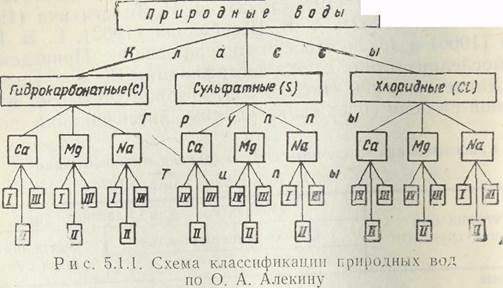
лее детальна по выделяемым типам и подробно обосновывается показателями. 45 По химическим свойствам также имеется много классификаций (В. И. Вернадский, 1933; Г. А. Максимова, 1944; О. А. Алекин, 1945; С. А. Щукарев, 1934; В. А. Приклонскнй, 1949; В. А. Сулин, 1955; М. Г. Валяшко, 1958; и др.). Наиболее часто употребляется классификация О. А. Алекина (рис. 5.1.1). В ее основу положены шесть главных ионои, выраженных в процент-эквивалентной форме. '"! Все природные воды О. А. Алекин делит по преобладающему аниону на три класса: I) гидрокарбонатные, 2) сульфатные, 3) хлоридныс. К г п д р о к а р б о н а т п ы м относится большая часть маломинерализованных вод рек, озер п некоторые подземные. К хлориднын — воды со значительной минерализацией. Это воды океана, морей, соленых озер, некоторые подземные. С у л ь ф а т п ы е но минерализации являются промежуточными между гидрокарбонатными и хло-ридными. Каждый класс О. А. Алекин делит по преобладающему катиону на группы кальциевых, магниевых и натриевых вод, а в пределах группы выделяет четыре тип а:^ I т и п характеризуется соотношением rMg'2++''Ca2f <гНСО3-. Это щелочные, мягкие, образующиеся при растворении продуктов выветривания изверженных пород, содержащих значительное количество Ка ' и К+. Возможно образование вод также за счет обменных реакций между кальцием вол и натрием поглощающего комплекса пород. Чаще всего эти воды маломинерализовапы. II т и п характеризуется соотношением гНСО3~ ОСа2+Н-+rMg2+<rHCO-+rS02!-. Воды этого типа —малой и уме- 46 репной минерализации, они связаны с осадочными породами и продуктами выветривания коренных пород. III тип характеризуется соотношением гНСО3~+гЗО4< <CrCa+rMg:+. Обычно это воды высокой минерализации, генетически они являются смешанными. IV т и п характеризуется простым соотношением гНСО3 —0, то есть воды этого типа кислые. Классы, группы и типы вод графически изображены па рис. 5.1.1, для их обозначения О. Л. Алекии ввел символы: класс обозначается символом соответствующего аниона. Класс гидрокарбонатных вод — символом С, сульфатных --5 я хлоридных вод— символом СУ; группы — символом катиона Са, Mg, Na; тип воды — римской цифрой. К символу добавляется минерализация воды в граммах на литр. Например: гидрокарбонатно-кальциевые воды I типа с минерализацией 0,6 г/л будут обозначены символом С^а—0,6. Существуют классификации, подразделяющие йоды по составу на основе коэффициентов, а также критериев пригодности для определенных целей. Последние отличаются от классификаций по генетическим признакам и максимально учитывают интересы потребителя (технология производства при извлечении и вид минерального сырья, безвредность). Обычно они регламентируются специальными ГОСТами. 5.2. Графические способы выражения результатов химического анализа воды При обобщении большого числа анализов воды для отдельных территорий, а также для изображения их результатов на гидрогеологических картах и разрезах широко применяют графические способы. Их много. Одни иллюстрируют соответствующие классификационные схемы, другие служа-] лишь для наглядного изображения данных анализа. Диаграммы-прямоугольники применяются для изображения состава воды на картах, разрезах. Они могут быть вертикальными и горизонтальными. Обычно в масштабе строят прямоугольник, разделенный па два по длинной стороне, которая изображает 100 % мг-экв. По ней откладывается в масштабе процент миллиграмм-эквивалентов катионов к+4_^а +, Mg2+, Са2*и анионов С1~, SOJ-, HCO^,C02d" в порядке относительной активности.Под диаграммой записывается общая минерализация воды в граммах на литр. На 47 рис. 5.2.1 показан пример вертикальной диаграммы-прямоугольника. Графики-треугольника катионного и анионного состава природных под удобны для систематизации массовых анали- М = 3,3
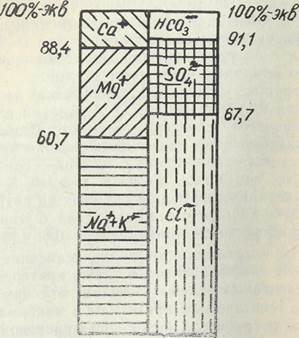
Рис. 5.2.1. Графическое выражение анализа воды способом прямоугольника (М —3,3 г/л) Диаграммы-круги (циклограммы) применяются в тех же случаях, что и диаграммы-прямоугольники, состоят из одного или нескольких концентрических кругов. В первом случае анализ воды изображают в двух половинах круга в виде секторов, соответствующих процентному содержанию анионов С1-, SO*-, НС03-+СО|~(в левой половине) и катионов Na +, К+, Mg2 +, Са2-!- (в правой). Во втором случае круг делится на кольца, внутри которых выделяются секторы, соответствующие процентному содержанию ионов, отсчитываемому с т вертикального или горизонтального радиуса по часовой стрелке в той же последовательности. В любом случае диаметр круга соответствует величин нерализации в граммах на литр. У диаграммы слева указывается общая минерализация, справа — дополнительные сведения (рН, температура, газы, микроэлементы). На рис. Ь.2... показан один из вариантов диаграммы-круга,
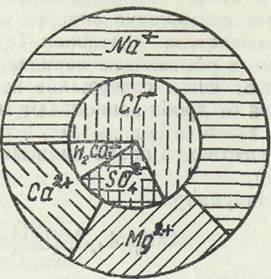
зов (рис. 5.2.3). Процент миллиграмм-эквивалентов катионов и анионов откладывают на соответствующих высотах треугольника. Из точек, отвечающих значениям отдельных катионов и анионов, восстанавливают перпендикуляры до пересечения друг с другом. Точка пересечения и будет отражать кати-онный либо анионный состав воды. Недостаток способа — разделение катионов и анионов па две несвязанные части.
Рис. 5.2.3. Треугольники катионного и анионного состава Наглядным изображением химического состава вод и их изменения в пространстве и времени является гидрохимический профиль и др. Подробно с ними можно ознакомиться в справочнике гидрогеолога и другой литературе [3, 1]. 5.3. Формулы химического состава Формулы представляют собой.краткую условную запись химического состава, выраженного в процент-эквива летной 4. Заказ 261 49 форме. Наиболее часто употребляемая форма записи--по М. Г. Курлову, предложенная им для «курортных вод». Она представляет собой псевдодробь, в числителе которой записывается содержание анионов в процент-эквивалентной форме, в знаменателе— катионов. Тс и другие располагают слева направо в убывающем порядке по содержанию. При этом учитывают ионы, содержание которых в воде превышает 10 %. Слева от дроби записывают минерализацию воды (г/л) и состав газов (л/л воды), если таковые имеются в значительных количествах. Справа записывают температуру (°С) и дебит (л/с). Например: сог м C16IS024,HCO?7 т ^0.2^46 —~-_J:i-_— 1 J - Т18Д0,<2. NaioCa16MgH При записи составов любых вод (исключая минеральные) часто ограничиваются лишь главными компонентами, причем содержание их округляют до целых процентов. Такое выражение называют формулой солевого состава. Существуют и другие формы записи ионного состава.
|
||||||||||||||||||||
|
Последнее изменение этой страницы: 2019-05-20; просмотров: 657; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.01 с.) |

 м=з,з
м=з,з



