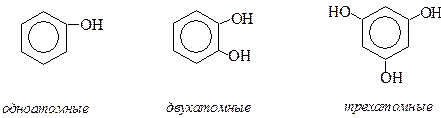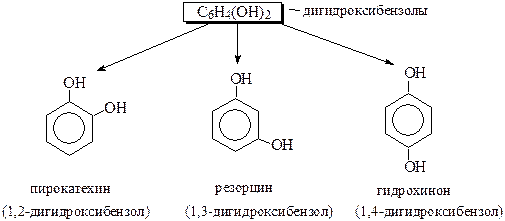Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Многоатомные спирты: химические свойства
Для двух- и трехатомных спиртов характерны основные реакции одноатомных спиртов. В реакциях могут участвовать не одна гидроксильная группа. По аналогии с алкоголятами соли двухатомных спиртов называются гликолятами, а трехатомных – глицератами.
1) Качественная реакция на многоатомные спирты Качественной реакцией на многоатомные спирты, содержащие группы ОН при соседних атомах углерода, является ярко-синее окрашивание при действии свежеосажденного гидроксида меди (II). Голубой осадок Сu(OH)2 растворяется в многоатомных спиртах, образуя раствор сине – фиолетового цвета.
2) Реакции этерификации с органическими и неорганическими кислотами Реакция взаимодействия многоатомных спиртов с карбоновыми кислотами протекает с образованием сложных эфиров.
Реакция взаимодействия глицерина с азотной кислотой протекает с образованием тринитрат глицерина (тривиальное название нитроглицерин) – известное взрывчатое вещество и не менее известное лекарственное (сосудорасширяющее) средство.
Многоатомные спирты: способы получения
Получение гликолей
1) Окисления алкенов перманганатом калия в нейтральной среде (реакция Вагнера):
2) Щелочной гидролиз дигалогеналканов:
Получение глицерина
1) Кислотный гидролиз жиров – обратимая реакция, протекающая с образованием глицерина и карбоновых кислот:
2) Щелочной гидролиз жиров: - необратимая реакция, протекающая с образованием глицерина и солей карбоновых кислот:
Физические свойства многоатомных спиртов
Этиленгликоль и глицерин при комнатной температуре представляют собой бесцветные вязкие жидкости, легко смешивающиеся с водой, сладкие на вкус. Температура кипения этиленгликоля 1970С, глицерина – 2900С. Этиленгликоль ядовит.
Фенолы
Фенолы – это производные ароматических УВ, в которых одна или несколько гидроксильных групп непосредственно связаны с бензольным кольцом.
Номенклатура Названия фенолов составляют с учетом того, что для номенклатуры ИЮПАК сохранено тривиальное название «фенол». Нумерация атомов углерода бензольного кольца начинают с атома, непосредственно связанного с гидроксильной группой, и продолжают в такой последовательности, чтобы имеющиеся заместители получили наименьшие номера.
Классификация
По числу гидроксильных групп фенолы классифицируют на:
Простейшие одноатомные фенолы
(C6Н5ОН) – фенол (гидроксибензол), тривиальное название – карболовая кислота.
Простейшие двухатомные фенолы
Физические свойства
Простейшие фенолы при комнатных температурах представляют собой низкоплавкие бесцветные кристаллические вещества с характерным запахом. Фенолы малорастворимы в воде, но хорошо растворяются в органических растворителях. Фнолы образуют прочные водородные связи и имеют довольно высокие температуры кипения и плавления. Являются токсичными веществами, вызывают ожоги кожи.
Способы получения 1) Сплавление солей ароматических сульфокислот со щелочами При сплавлении натриевой соли ароматической сульфокислоты со щелочью сначала образуется фенолят, который при дальнейшем взаимодействии с кислотой превращается в фенол.
2) Щелочной гидролиз арилгалогенидов При нагревании хлорбензола и гидроксида натрия под давлением получают фенолят натрия, при дальнейшей обработке которого кислотой образуется фенол:
3) Кумольный способ На первой стадии из бензола получают кумол (изопропилбензол), каталитическое окисление которого кислородом приводит к получению гидропероксида кумола. Дальнейшее нагревание гидропероксида кумола с серной кислотой приводит к получению фенола и ацетона, которые разделяют путем ректификакции (фракционной перегонки). Это основной промышленный способ получения фенола:
Химические свойства
|
|||||
|
Последнее изменение этой страницы: 2017-02-22; просмотров: 607; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.144.69 (0.01 с.) |