
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Характеристики основных термодинамических процессов идеального газаСодержание книги
Поиск на нашем сайте
Продолжение табл. 1.3.
где dS – бесконечно малое приращение энтропии системы; dQ – бесконечно малое количество тепла, полученного системой от источника тепла; T – абсолютная температура источника тепла. Знак неравенства соответствует необратимым процессам, а знак равенства – обратимым процессам. Следовательно, аналитическое выражение второго закона термодинамики для бесконечно малого обратимого процесса имеет вид:
а так как согласно первому закону термодинамики:
то уравнение (1.118) принимает следующий вид:
ЭНТРОПИЯ ИДЕАЛЬНОГО ГАЗА Основным уравнением для определения изменения энтропии в обратном процессе является выражение:
Поскольку в технической термодинамике приходится иметь дело не с абсолютным значением энтропии, а с ее изменением, отсчет значений энтропии можно вести от любого состояния. Для газов принято считать значение энтропии равным нулю при нормальных условиях, т. е. при t = 0o C и P = 760 мм. рт. ст. Определение энтропии для любого состояния газа при постоянной теплоемкости, отсчитанной от нормального состояния, производят по следующим формулам:
Изменение энтропии между двумя произвольными состояниями газа 1 и 2 при постоянной теплоемкости определяют по следующим формулам:
Уравнения кривых различных термодинамических процессов в системе координат Ts имеют следующий вид (при постоянной теплоемкости): уравнение изохоры:
уравнение изобары:
Взаимное расположение изохоры и изобары показано на рис. 1.7.
Рис. 1.7. Взаимное расположение изохоры и адиабаты в координатных осях TS
уравнение изотермы:
T = const.
При этом изменение энтропии в изотермическом процессе равно:
Уравнение адиабаты:
s = const. (1.129)
Изображение изотермы и адиабаты в системе координат TS и Pυ дано соответственно на рис. 1.8 и 1.9.
Рис. 1.8. Изображение изотермы в координатных осях TS
Рис. 1.9. Изображение адаибаты в координатных осях Pυ
Уравнение политропы:
где:
Широким распространением при решении термодинамических задач пользуется диаграмма TS. Адиабаты в этой диаграмме изображаются вертикалями, изотермы – горизонталями, изохоры и изобары идеального газа – логарифмическими кривыми. Примеры решения задач Примеры решения задач к разделу 1.1 1. Давление в паровом котле P = 0,4 бар при барометрическом давлении B1 = 725 мм рт. ст. Чему будет равно избыточное давление в котле, если показание барометра повысится до B2 = 785 мм. рт. ст., а состояние пара в котле останется прежним? Барометрическое давление приведено к 00.
Решение Абсолютное давление в котле
Избыточное давление при показании барометра В2 = 785 мм рт. ст.
2. Во сколько раз объем определенной массы газа при -200 С меньше, чем при +200 С, если давление в обоих случаях одинаковое?
Решение При постоянном давлении объем газа изменяется по уравнению (1.9):
следовательно,
3. Баллон с кислородом емкостью 20 л находится под давлением 10 МПа при 150 С. После израсходования части кислорода давление понизилось до 7,6 МН/м2, а температура упала до 100 С. Определить массу израсходованного кислорода.
Решение Из характеристического уравнения:
PV = MRT
Имеем:
Следовательно, до расходования кислорода масса его составляла:
а после израсходования:
Таким образом, расход кислорода: 2,673 – 2,067 = 0,606 кг. 4. Сосуд емкостью V=10 м3 заполнен 25 кг углекислоты. Определить абсолютное давление в сосуде, если температура в нем t = 270 C.
Решение Из характеристического уравнения
PV = MRT
Имеем
Примеры решения задач к разделу 1.2 1. Атмосферный воздух имеет примерно следующий массовый состав: Определить объемный состав воздуха, его газовую постоянную, кажущуюся молекулярную массу и парциальные давления кислорода и азота, если давление воздуха по барометру В =760 мм рт. ст. Решение По уравнению (1.15) получаем
Газовая постоянная воздуха определяется по уравнению (1.23):
Кажущаяся молекулярная масса смеси определяется из уравнения (1.21):
или из уравнения (1.24):
Отсюда:
Парциальные давления определяем из уравнения (1.26):
следовательно,
2. Смесь газов состоит из водорода и окиси углерода. Массовая доля водорода Определить газовую постоянную смеси и ее удельный объем при нормальных условиях.
Решение Из уравнения (1.23):
Удельный объем газовой смеси найдем из характеристического уравнения Pυ = RT:
Примеры решения задач к разделу 1.3 1. Воздух в количестве 6м3 при давлении р1=3 бар и температуре t1 = 25o C нагревается при постоянном давлении до t2= 130о С. Определить количество подведенного к воздуху тепла, считая с = const. Для данного случаяиспользуем формулу (1.69):
Масса газа определится из уравнения (1.5):
а объем газа при нормальных условиях – из уравнения (1.11):
На основании формул (1.27) и (1.28) и табл. 1.3 имеем:
Следовательно,
или:
Примеры решения задач к разделу 1.4 1. В котельной электрической станции за 20 ч работы сожжены 62 т каменного угля, имеющего теплоту сгорания 28900 кДж/кг (6907 ккал/кг). Определить среднюю мощность станции, если в электрическую энергию превращено 18% тепла, полученного при сгорании угля. Решение Количество тепла, превращенного в электрическую энергию за 20 ч работы:
Эквивалентная ему электрическая энергия или работа:
Следовательно, средняя электрическая мощность станции:
2. Паросиловая установка мощностью 4200 кВт имеет к.п.д. Определить часовой расход топлива, если его теплота сгорания:
Решение По формуле (1.54):
отсюда:
Часовой расход топлива составит:
G= Примеры решения задач к разделу 1.5 1. В закрытом сосуде заключен газ при разрежении P1=50 мм. рт. ст. и температуре t1= 70o C. Показание барометра – 760 мм. рт. ст. До какой температуры нужно охладить газ, чтобы разрежение стало равным P2 = 100 мм. рт. ст.?
Решение Так как процесс происходит при V=const, то согласно формуле (1.61):
Подставляя значения, получаем:
отсюда:
2. В закрытом сосуде емкостью Принимая теплоемкость воздуха постоянной, определить, какое давление и какая температура устанавливается после этого в сосуде.
Решение Пользуясь уравнением состояния, определяем массу воздуха в сосуде:
Количество тепла, отводимого от воздуха в процессе, определяется уравнением (1.63):
откуда:
Значение Из соотношения параметров в изохорном процессе:
Имеем:
3. 1 кг воздуха при температуре Определить конечный объем, затрачиваемую работу и количество тепла, отводимого от газа. Решение Определяем начальный объем воздуха из уравнения состояния:
Так как в изотермическом процессе:
то конечный объем
Работа, затрачиваемая на сжатие 1 кг воздуха, получается из уравнения (1.73):
Количество тепла, отводимого от газа, равно работе,
4. 1 кг воздуха при начальной температуре Определить конечный объем, конечную температуру и затрачиваемую работу. Решение Из соотношения параметров в адиабатном процессе по уравнению (1.82) находим:
откуда:
Принимая k = 1,4, получаем:
Затраченная работа по уравнению (1.85):
Конечный объем определяется из уравнения состояния:
5. 1 кг воздуха при P1 = 5 бар и t1 = 111o C расширяется политропно до давления P2 = 1 бар. Определить конечное состояние воздуха, изменение внутренней энергии, количество подведенного тепла и полученную работу, если показатель политропы n = 1,2.
Решение Определяем начальный удельный объем воздуха:
Конечный удельный объем воздуха находим из уравнения (1.96):
Конечную температуру проще всего найти из характеристического уравнения:
Величину работы находим из уравнения (1.102):
Изменение внутренней энергии:
Количество тепла, сообщенного воздуху, по уравнению (1.109):
9. 1,5 кг воздуха сжимают политропно от P1 = 0,9 бар и t1 =18o C до P2 = 10 бар; температура при этом повышается до t2 = 125o C. Определить показатель политропы, конечный объем, затраченную работу и количество отведенного тепла.
Решение По формуле (1.115):
отсюда:
Конечный объем определяем из характеристического уравнения:
Затраченная работа по уравнению (1.107):
Количество отведенного тепла по уравнению (1.110):
Примеры решения задач к разделу 1.6 1. Определить энтропию 1 кг кислорода при P=8 бар и t=250о С. Теплоемкость считать постоянной.
Решение
По формуле (1.121):
Так как для двухатомных газов R = 8,314 кдж/(кмоль
2. 1 кг кислорода при температуре t1 = 127o C расширяется до пятикратного объема; температура его при этом падает до t2 = 27o C. Определить изменение энтропии. Теплоемкость считать постоянной.
Решение По уравнению (1.123):
3. 10 м3 воздуха, находящегося в начальном состоянии при нормальных условиях, сжимают до конечной температуры 400о С. Сжатие проводится: 1) изохорно, 2) изобарно, 3) адиабатно и 4) политропно с показателем политропы n = 2,2. Считая значение энтропии при нормальных условиях равным нулю и принимая теплоемкость воздуха постоянной, определить энтропию воздуха в конце каждого процесса.
Решение Находим массу 10 м3 воздуха при нормальных условиях:
Определяем изменение энтропии в каждом из перечисленных процессов: 1) Изохорное сжатие:
2) Изобарное сжатие:
3) Адиабатное сжатие:
4) политропное сжатие:
1.8. Контрольные задания к разделу 1 Контрольные задания к разделу 1.1-1.2 1*. Разрежение в газоходе парового котла, измеряемое тягомером, равно Р мм вод. ст. Определить абсолютное давление газов, если показание барометра 730 мм рт. ст., и выразить его в МПа. 2*. Объемный состав газообразного топлива следующий: H2, %, CH4, %. Определить среднюю молекулярную массу и газовую постоянную смеси.
3*. Определить массу 5 м3 водорода 5 м3 кислорода и 5 м3 углекислоты при давлении P бар и температуре 1000 С. 4*. Какова будет плотность окиси углерода при t0 С и 710 мм рт. ст., если при 00 C и 760 мм рт. ст. она равна 1,251 кг/м3? 5*. Дымовые газы, образовавшиеся в топке парового котла, охлаждаются с t0 С до 2500 С. Во сколько раз уменьшается их объем, если давление газов в начале и конце газоходов одинаково? 6**.. В цилиндрическом сосуде диаметром d м; и высотой h=2,4 м находится воздух при t 0С, давление воздуха Pmax=0,865 МПа, Рбар=101858 Па. Определить массу воздуха в сосуде и плотность. 7**. В резервуаре объемом 10 м3 находится газовая смесь, состоящая из n1 кг кислорода и n2 кг азота. Температура смеси равна 27 °С. Определить парциальные давления компонентов смеси. 8**. Определить диаметр воздуховода для подачи G кг/ч воздуха при абсолютном давлении 1,15 бар, если температура этого воздуха 22° С. Скорость воздуха в воздуховоде равна 8 м/с. 9***. Поршневой компрессор всасывает в минуту 3 м3 воздуха при t = 17° С и барометрическом давлении Рбар = 750 мм рт. ст. и нагнетает его в резервуар, объем которого равен 8,5 м3. За какое время (в мин) компрессор поднимет давление в резервуаре до значения Р, если температура в резервуаре будет оставаться постоянной? Начальное давление в резервуаре было 750 мм рт. ст., а температура равнялась 17° С.
Контрольные задания к разделу 1.3-1.4 1*. Воздух охлаждается от t1 0C до t2=1000 C в процессе с постоянным давлением. Какое количество теплоты теряет 1 кг воздуха, считая теплоемкость постоянной. 2*. В закрытом сосуде объемом V находится воздух при давлении Р1=0,8 МПа и температуре t1=200 С. Какое количество теплоты необходимо подвести для того, чтобы температура воздуха поднялась до t2=1200 С? 3**. Найти часовой расход топлива, который необходим для работы паровой турбины мощностью 25 МВт, если теплота сгорания топлива 4**. Определить изменение внутренней энергии 2 м3 воздуха, если температура его понижается от 5**. В сосуд, содержащий 5 л воды при температуре 20о С, помещен электронагреватель мощностью N Вт. Определить, сколько времени потребуется, чтобы вода нагрелась до температуры кипения 100о С. Потерями теплоты в окружающую среду пренебречь. 6**. В закрытом сосуде объемом V = 300 л находится воздух при давлении P1 бар и температуре t1 = 20 Какое количество тепла необходимо подвести для того, чтобы температура воздуха поднялась до t2 = 120 Задачу решить, принимая теплоемкость воздуха постоянной. 7***. Продукты сгорания топлива поступают в газоход парового котла при температуре газов tг = 1100° С и покидают газоход при температуре газов tг’ = 700° С. Объемный состав газов следующий: r(CO2) = 11 %, r(O2) = 6%, r(H2O) %, r(N2) %. Определить, какое количество теплоты теряет 1 м3 газовой смеси, взятой при нормальных условиях.
Контрольные задания к разделу 1.4-1.6 1**. Какое количество теплоты необходимо затратить, чтобы нагреть V м3 воздуха при постоянном избыточном давлении P = 2 ат. от t1 = 120° C до t2 = 450° C? Какую работу при этом совершит воздух? Атмосферное давление принять равным 750 мм рт. ст. 2**. В закрытом сосуде заключен газ при разрежении (P1)в = 6,7 кПа и температуре t1 oC. Показания барометра – 742 мм рт. ст. До какой температуры нужно охладить газ при том же атмосферном давлении, что бы разрежение стало (P2)в =13,3 кПа? 3**. В установке воздушного отопления внешний воздух при t1= –15° C нагревается в калорифере при P = const до 60° C. Какое количество теплоты надо затратить для нагревания V м3 наружного воздуха? Давление воздуха считать равным 755 мм рт. ст. Теплоемкость воздуха считать постоянной. 4**. Найти внутреннюю энергию, энтальпию и энтропию 1 кг азота, если температура его равна t °С, а давление (абсолютное) 0,6 МПа. Теплоемкость считать не зависящей от температуры. 5**. Воздух в количестве M кг при температуре t = 27° C изотермически сжимается до тех пор, пока давление не становится равным 4 МПа. На сжатие затрачивается работа L= –6 МДж. Найти начальные давление и объем, конечный объем и теплоту, отведенную от воздуха. 6**. Воздух при температуре t1 = 20° C должен быть охлажден посредством адиабатного расширения до температуры t2 °C. Конечное давление воздуха при этом должно составлять 0,1 МПа. Определить начальное давление воздуха P1 и работу расширения 1 кг воздуха. 7**. В процессе политропного расширения воздуха температура его уменьшилась от t1 °С до t2 = -37° С. Начальное давление воздуха P1 = 4 бар, количество его M = 2 кг. Определить изменение энтропии в этом процессе, если известно, что количество подведенного к воздуху тепла составляет 89,2 кДж. 8**. Какое количество тепла необходимо затратить, чтобы нагреть 2 м3 воздуха при постоянном избыточном давлении P= 2 бар от t1 = 100° С до t2 °С? Какую работу при этом совершит воздух? 9***. Уходящие газы котельной установки проходят через воздухоподогреватель. Начальная температура газов tг1 = 300° C, конечная tг2 = 160° C; расход газов равен G кг/ч. Начальная температура воздуха составляет tв1 = 15 °C, а расход его равен 800 кг/ч. Определить температуру нагретого воздуха tв2, если потери тепла в воздухоподогревателе составляет 4 %. Средние теплоемкости (Cpm) для газов и воздуха принять соответственно равными 1,0467 и 1,0048 кДж/(кгּК). 10***. Рабочим телом газотурбинного двигателя является смесь идеальных газов. Массовый состав смеси m следующий: m(CO2) = 20 %, m(O2) = 8 %, m(H2O) %, m(N2) %. При прохождении через газовую турбину температура потока газовой смеси снижается с t1 = 1200° C до t2 = 400° C. Определить техническую работу газовой турбины в расчете на 1 кг рабочего тела, пренебрегая теплообменом в окружающую среду и зависимостью теплоемкости от температуры.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 790; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.225.156.49 (0.015 с.) |








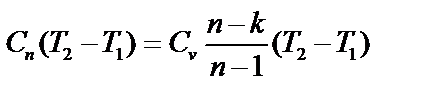




 (1.118)
(1.118)

 (1.119)
(1.119) (1.120)
(1.120)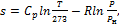 (1.121)
(1.121) (1.122)
(1.122) (1.123)
(1.123)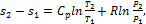 (1.124)
(1.124) (1.125)
(1.125)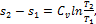 (1.126)
(1.126) (1.127)
(1.127)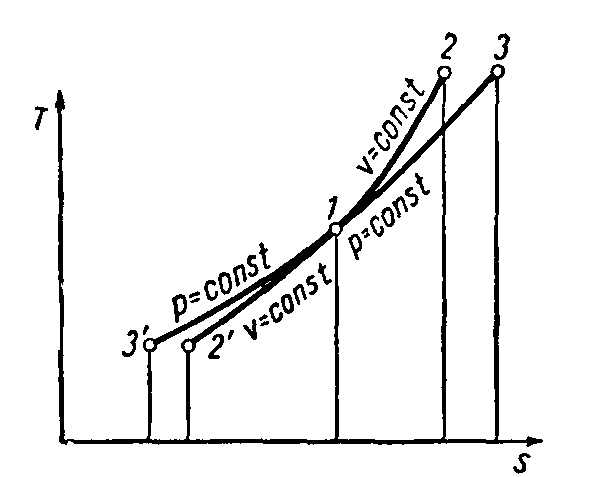
 (1.128)
(1.128)

 (1.130)
(1.130)







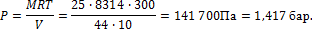
 = 23,2%;
= 23,2%;  = 76,8%.
= 76,8%.


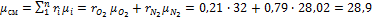 ,
,

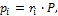




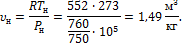





 ,
,

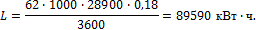

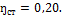

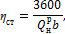





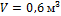 содержится воздух при давлении
содержится воздух при давлении  и температуре
и температуре  В результате охлаждения сосуда воздух, содержащийся в нем, теряет 105 кДж.
В результате охлаждения сосуда воздух, содержащийся в нем, теряет 105 кДж.


 полученно из выражения
полученно из выражения  (для двухатомных газов).
(для двухатомных газов). .
.
 и начальном давлении
и начальном давлении  сжимается изотермически до конечного давления
сжимается изотермически до конечного давления 
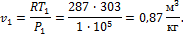

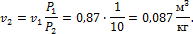



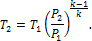





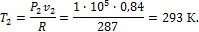





 .
.

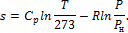
 , а
, а град), то:
град), то: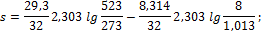
 .
.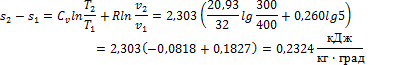


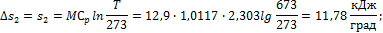

 .
.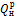 МДж/кг и известно, что на превращение тепловой энергии в электрическую используется только 35% теплоты сожженного топлива.
МДж/кг и известно, что на превращение тепловой энергии в электрическую используется только 35% теплоты сожженного топлива.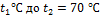 . Начальное давление воздуха абсолютное
. Начальное давление воздуха абсолютное 
 .
. ?
? , МДж/кг
, МДж/кг



