Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение и функции биологических мембран.Содержание книги
Поиск на нашем сайте
29. Роль белков, липидов, гликолипидов и гликопротеинов в структурной организации и функционировании мембран. Значение мембран в поддержании гомеостаза клеток. 30. Роль липидов в организации структуры клеточных мембран. Влияние фазовых состояний и фазовых переходов липидов на функции мембран. 31. Повреждения мембран, связь с развитием болезней. Основные повреждающие факторы. Перекисное окисление липидов. Антиоксидантная защита (ферменты, витамины). 32. Трансмембранный перенос веществ (диффузия, активный транспорт, эндоцитоз, секреция). Значение процесса в образовании секрета слюнных желез. 33. Главные компоненты и этапы трансмембранной передачи сигналов гормонов, медиаторов, цитокинов, эйкозаноидов.
29) Белки отвеч за функ-ть мембр. На долю белков прих-ся от 30-70% массы мембр. Белки мембр разл-ся по своему полож в мембр. Белки могут глубоко проникать в липид бислой или даже пронизывать его, либо разн спос прикр-ся к мембр. *Основ роль липидов в сос мембр закл-ся в стабилиз-ии биослоя. Клетки окр-ны таким слоем липидов кот сформир-н из особ типа липидов, кот облад одновр гидрофиль и гидрофоб св.вом. * Гликолипиды несут разнообр ф-циюони отвеч за рецерпцию нект биолог акт в.в. Они участ в том что опред видов спец-ть ткани. * гликопротеины-в ор-ме чел-ка раз ф-ции и прист во всех классах белков. Предст-ли коллаген и эластин.* Гомеостаз-сов-ть слож приспособит реакций ор-ма. Прониц-ть мембр имеет большое знач-е для саморег-и и поддерж пост-ва состава клетки ее физико-хим гомеостаз Прониц-ть играет важн роль в генерации провед нерв импульса, в энергообесп клетки и др процессах жизнед-ти. 30) Основ роль липидов в сос мембр закл-ся в стабилиз-ии биослоя. Клетки окр-ны таким слоем липидов кот сформир-н из особ типа липидов, кот облад одновр гидрофиль и гидрофоб св.вом* в билог мембр липид слой по всем представлениям явл-ся жидким телом вяз-ти близкой к вязкости подсолнеч масла. текуч мембр огр-на внутр гидрофоб фазой. Эта фаза не всегда быв жидкой. При пониж t мембрана замерзает,т.е. жидкая превр-ся в кристалич-ю. При кристал сост-ии мембрана пропускная сп-ть об-ки сниж-ся и за счет этого сниж-ся жизнедеят. 31.) нар-е тр-та энергии АТФ. нар-е исп-я энергии АТФ. перерастяжение и разрыв мембран набух клеток. дисбаланс ионов и воды в клетке. гипер/гипогидратация клетки. мутации. нар-е митоза и мейоза. *перикис окисл-е- окислит дегидратация липидов происход в основ под дейст своб R. Реак сопр-ся обр-ем своб R
32) это двухстор перем-е в.в из цитоплазмы кл в прост-во и обратно с целью дост-ки кл пит в.в, удаление прод метаболизма. диффузия-одно из явл-й переноса предст собой неравновесн вероятностный пр-сс взаим проникн соприкас-ся в.в в друг друга вслед перем-я частиц в.в, стремл-е к установл-ю равновесн распр-я концентр-ии в.в. актив тр-т-перенос в.в ч/з клет или внутриклет мембр из области низкой концентр в об-ть высокой, т.е. с затратой своб энергии ор-ма. Эндоцитоз-пр-сс поглащ в.в клетками путем втягив-я уч-ка клеточ мембр и обр-я в цит-ме мембр пузыря. Скреция- обр-е и выд-е кл в.в. специф дей-я участ в регуляции процессов жизнедеят. 33) *вз-е р-ра с сигнал молекулой; активация мембр фермента, ответствен за обр-е вторич посредника; обр-е вторич посредника и, АМФ, ц Г М Ф, ИФЗ,ДАТ или Ca 2; актив-я посредниками специф белков в основ протеикиназ кот в свою очередь фосфарилир-ся ферменты, оказ влияние на акт-ть внутриклет про-ов. Энергетический обмен 34.Понятие о катаболизме и анаболизме, их взаимосвязи. Эндергонические и экзергонические реакции метаболизма. Общие пути катаболизма. АТФ и другие макроэргические соединения, их образование и использование. 35. Структурная организация дыхательной цепи митохондрий, ее функции (энергетическая, терморегуляторная) и место в системе дыхания. Дыхательный контроль. 36. Дегидрирование субстратов и окисление водорода как источник энергии для синтеза АТФ. Окислительное фосфорилирование, его механизм, коэффициент эффективности (Р/О). 37.Дыхательная цепь. Условия, обеспечивающие физиологический уровень ее работы. Ингибиторы тканевого дыхания. Разобщение дыхания и окислительного фосфорилирования, последствия. 38. Свободнорадикальное окисление, физиологическое значение. Токсичность кислорода. Условия, активизирующие процесс, последствия активизации (ПОЛ), физиологическое значение. Пероксидаза слюны. 39. Нарушения энергетического обмена. Гипоксия. Гипоэнергетическое состояние и его последствия. 40. Окислительное декарбоксилирование пирувата, связь с цитратным циклом и дыхательной цепью, участие витаминов. Регуляция, физиологическое значение. 41. Цикл лимонной кислоты (цикл Кребса). Последовательность реакций, регуляция процесса, энергетическая функция. Образование цитрата и его роль в процессах минерализации твердых тканей ротовой полости.
34.) анаболизм-синтез новых стр-р или в.в, это пр-сс поддерж обновлен и рост новых тк-й ор-ма, в том числе мышц. Катаболизм- разр-е стр-р или в.в, это необх для обр-я прост в.в. Взаимосвязь пр-сов основ на единстве биохим превр-й, обеспечив энергией всепр-ссы жизнедеят и пост обновл тк-й ор-ма. Энергет р- р, сопр поглощ энергии; для ее протек необх энергия из внеш ср. Экзергонич р-р протек с выд-ем энергии. * Общий путь кат-ма-это путь поставки H орг-х в.в в дыхат цепь. в общем пути кат-ма происх 5 р денатурирования. * Макроэргические соед-я-прир
35) Дыхат цепь митох. мультиферм сис, встроена в кисты. Комп-с отним Н от ссубстратов и ч/з сис переносчиков посл-но передает ей О2 с обр-ем Н2О. Про-сы окисл и фосфорилир м/д собой сопряжены. Окисилит "фосфорил в ЦПЭ"-ист-к АТФ в аэроб кл. имеется межмемб прост-во, сама мембр, матрикс. 36) оксилит фосфорилир-е. дыхат цепь митох, фер-т АТФ-синтаза, А Д Ф+H3PO4→АТФ 37). Дыхат цепь митох. мультиферм сис, встроена в кисты. Комп-с отним Н от ссубстратов и ч/з сис переносчиков посл-но передает еа О2 с обр-ем Н2О. Про-сы окисл и фосфорилир м/д собой сопряжены. Ингибиторы фер-ов ЦПЭ: НАДН2(барбитураты(веронал, гексенал, нембутал), ротенон), QH2-дегидрогеназа(антибиоткик (антимицин А), цитохром-с-оксидаза(цианиды, угарный газ, сероводород) АТФ-синтетаза(олигомицин). Разобщение дых-я и фосфорилирования- ряд хим в.в раствор в липидах, способны транспортировать Н+ в матрикс, минуя пртонные каналы. Рез-т:↓∆μН, синтез АТФ Р/О, ↑t. разобщители: экзогенные(2,4 динитрофенол, антбиотики, токсины) Эндог(жирн к-ты, тирксин, ПОЛ, термогенин) 38) Свободнорадик-е окисл-е-важный и многогранный биохим пр-сс. Превр-ии O2,липидов, белков и др соед под дейст своб R.O2-стабил мол-ла с опр периодом полураспада. ЦНС -симптомы интоксикации прояв-ся беспок-ом, тошнотой, головокруж, судорог. Легкие-пор-е альвеолярно-капилляр мембр. Может встр-ся абсорбционный калапс легкого. Пероксидаза- фермент вы-й защит ф-ю. Фер-т окисл-й субстраты, исп-я H2O2, в кач-ве ок-ля. 39) нар-е мет-ма может прояв-ся на всех ур-ях биолог ор-ции от молекул т клет до организм-го. Гипоксия- сост кислор голодания как всего ор-ма так и отд ор-ов. В след чего в ор-х разв-ся необрат изм-я. Гипоэнерг сост-е-это сост возник вслед-ии нехвата энергии, а нехвата энергии связ с наруш-ем 1поступ-я О2 в кровь, 2. тр-т О2 в ткани,3.ф-ции митох. 40) Окислительное декарбокс пировиногр к-ты(пируват). П В К -центр метаболит углевод обмена, обр-ся из аминк-т. При окисл декарбоксил П В К обр-ся актив форма уксус к-ты-ацетил КоА. общий путь кат-ма как раз и включает окислит декарбоксилир., а ткаже ЦТК, дыхат цепь митох.
41) 41. Цикл Кребса- циклич биохим анаэроб пр-сс, в ходе кот освоб водород окисл-ся до Н2О, принимает уч-е в синтезе АТФ1
. в тв тк зуба ор-ма сод 90% всего цитрата. Нераствор форма адсорбируется на пов-ти кристаллов ГАП и просто связ-ся с ним. Белков ч этого цитрата вкл-ся в эмаль и дентин. Эта форма цитрата играет роль в патогенезе кариеса, т.к. цитрат опр св-ва расворим-ти прониц эмали.
ЩУКа съела ацетат, получается цитрат через цисаконитат будет он изоцитрат водороды отдав НАД, он теряет СО2 этому безмерно рад альфа-кетоглутарат окисление грядет — НАД похитил водород ТДФ, коэнзимА забирают СО2 а энергия едва в сукциниле появилась сразу АТФ родилась и остался сукцинат вот добрался он до ФАДа — водороды тому надо фумарат воды напился, и в малат он превратился тут к малату НАД пришел, водороды приобрел ЩУКа снова объявилась и тихонько затаилась Обмен углеводов 42. Основные углеводы тканей человека, их биологическая роль. Особенности метаболизма фруктозы и галактозы, связь с онтогенезом. Галактоземия, фруктозурия. 43. Углеводы пищи и их биологическая ценность, суточная потребность. Особенности переваривания и всасывания углеводов. Возможные нарушения процессов. 44. Основные углеводы тканей человека, их биологическая роль. Глюкоза, функции, особенности метаболизма в разных тканях. 45.Аэробный гликолиз, последовательность реакций, связь с общими путями катаболизма. Физиологическая роль процесса. Регуляция. 46.Анаэробные окисления глюкозы, последовательность реакций, физиологическое значение, регуляция. Образование молочной кислоты в тканях и ротовой полости. Лактатацидоз. 47.Анаэробный гликолиз и образование молочной кислоты в ротовой полости как пусковой механизм деминерализации тканей. Регуляция кислотно-основного равновесия в ротовой полости. 48.Пентозофосфатный путь катаболизма глюкозы, окислительные реакции. Распространение в организме, физиологическая роль процесса. 49.Глюконеогенез (цикл Кори). Роль лактата, аминокислот, глицерина. Значение процесса, регуляция. Значение биотина. 50. Биосинтез и мобилизация гликогена: последовательность реакций, физиологическое значение. Зависимость от ритма питания, регуляция. 51.Регуляция обмена углеводов и поддержания физиологического уровня глюкозы в крови. Характеристика гормонов и механизм их действия. Гипо- и гипергликемии. Определение толерантности к глюкозе. 42) Глюк, фрук, галак, сахар, лакт, мальтодекстрины, амилаза, пектин. структ-я, пласт-я, энергет-я, запас-я, осмот-я. Мет-м фрук: фосфорелиров-ем фрук с обр-ем фрук-6-фосфат. делее фрукт-6-фосфат расщеп на фрукт-1,6-биофосфат под дей-ем АТФ и А Д Ф далее может подверг-ся дальн превр-ям по путигликолиза. (путь включения фруктозы в мышеч ткан почках жиров тк). в печени др путь Фруитоза-1-фосфат↔диоксиацетонфосфат+D-глицеральдегид. D_глицеральдгид под влиян тиокиназы подв фосфорилир до глицеральдегид-3-фосфата. Мет галактозы Галактоза превр-ся в галактоза-1-фофат(катал галактокиназа), галактоза 1-ф+ У Д Ф- глюк↔(гексозо-1-фосфата-уридилтрансфераза) глюкозо-1-фосфат+ У Д Ф-галактоза, образов Глюк-1-фосфат перех в глюк-6 фосфат а У Д Ф-галактоза ↔У Д Фглюкоза+ пирофосфат ↔(У Д Ф-глюк- пирофосфорилаза) Глюк-1-фосфат + У Т Ф. * Галактоземия- редк генет нар-е обмена в.в. нар-е преобр-я галактозы в глюкозу. (мутация структ гена ответств за синтез фер-та). Фруктозурия- редкий наслед дефект углевод обмена. Недостаточный синтез фруктокиназы. 43) Моносахариды: глюк, фрукт, манноза, дисахариды: сахар, мальт, лакт; плисахар: декстрин, гликоген, крахмал, целлюлоза. структ, запас, пластич, осмотич, рецепто, энергет. суточ потр-ть ор-ма зависит от возраста: от1-1,5г 160г, от 3-4 л-233, от 11-13 л -282, от 14-17 366, сред возраст 616-686. * Переварив-е углев-в нач-ся в ПР. Основ перев просх в тонк к-ке. Углеводы-орг-е в.ва содерж карбонильн группу и неск гидрокс групп. 44). Моносахариды: глюк, фрукт, манноза, дисахариды: сахар, мальт, лакт; плисахар: декстрин, гликоген, крахмал, целлюлоза.* Глюк, бесцвет кристал в.во сладк вкус, растворим в Н2О. В пром-ти глюк получ гидролизм крахмала. в природе глюкоза пол-ся в пр-ссе фотосинтеза. В ор-ме чел-ка явля универс и осн источ энергиидля обесп метабол проц-ов. 45) Аэробн гликолиз- превр глюк в 2 мол-лы П В К. происх в аэроб усл-ях. Энерг выход 8 АТФ. энерг итог гликолиза- 1 глюкозо 6-ф→2 П В К+2НАДН2+ 2 АТФ. 2 НАД-Н2-донор Н для мотихон ЦПЭ, куда перед-ся ч/з мол-лы-посредники. энерг итог: 6 АТФ. 2 П В К могут вступаь в общ путь кат-ма(аэроб окисл глюк), 2 П В К могут прев-ся в анаэроб усл-ях(анаэроб гликолиз). Знач аэроб гликолиза: основ путь кат-ма глюк в бол-ве тк-й(мышцы, почки), наиб инт-но протек в нерв ткани, знач проц в печени-обр-е субстратов и АТФ для синтеза липидов, активация аэроб распада глюк при длит мыш работе в спорте получ назв-е " второе дых-е". 46) 1) Анаэробным гликолизом называют процесс расщепления глюкозы с образованием в качестве конечного продукта лактата(молочной кислоты). Процесс протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи. В цитозоле потекают все 10 реакций, идентичных аэробному гликолизу. 11 реакция является специфической для анаэробного гликолиза, где происходит восстановление ПВК(акцептор водорода) НАДН2 до лактата. 2) физиологическое значение гликолиза: единственный процесс в организме продуцирующий энергию без О2(важно при гипоксии), быстрый короткий процесс, возможен во всех клетках и тканях. Наиболее интенсивно протекает в эритроцитах (нет митохондрий), мышцах (бег до 200 м), опухолевых клетках 3) Образование молочной кислоты (лактата) -Превращение пирувата в лактат обеспечивает регенерацию цитозольного НАДН2→НАД+ -Эта реакция необходима клетке, т.к. НАДН2 образующийся в 6-й реакции, в отсутствии О2 не может окисляться в ЦПЭ. -Реакция обратима -Катализирует процесс лактатдегидрогеназа 3) Значение гликолиза для анаэробной микролоры -Основной источник энергии у анаэробной микрофлоры -Лежит в основе молочнокислого брожения у бактерий, спиртового брожения у дрожжей -Основной источник энергии для анаэробной микрофлоры полости рта, содержащей сахарозу -Следствие: накопление лактата в зубном налете привоит к деминирализаци твердых тканей зуба. -Фактор риска развития кариеса. 4) Лактатцидоз Накопление молочной кислоты (лактата) в клетке, межклеточном пространстве, крови снижает уровень рН и приводит к развитию лактатцидоза. Причины развития: гипоксия, гиповитаминозы В1,В2,РР, интенссивная мышечная работа Последствия лактатцидоза: болевой синдром в мышцах, развитие утомления.
47) 1) Анаэробным гликолизом называют процесс расщепления глюкозы с образованием в качестве конечного продукта лактата(молочной кислоты). Процесс протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи. В цитозоле потекают все 10 реакций, идентичных аэробному гликолизу. 11 реакция является специфической для анаэробного гликолиза, где происходит восстановление ПВК(акцептор водорода) НАДН2 до лактата. 2) физиологическое значение гликолиза: единственный процесс в организме продуцирующий энергию без О2(важно при гипоксии), быстрый короткий процесс, возможен во всех клетках и тканях. Наиболее интенсивно протекает в эритроцитах (нет митохондрий), мышцах (бег до 200 м), опухолевых клетках 3) Образование молочной кислоты (лактата) -Превращение пирувата в лактат обеспечивает регенерацию цитозольного НАДН2→НАД+ -Эта реакция необходима клетке, т.к. НАДН2 образующийся в 6-й реакции, в отсутствии О2 не может окисляться в ЦПЭ. -Реакция обратима -Катализирует процесс лактатдегидрогеназа 3) Значение гликолиза для анаэробной микролоры -Основной источник энергии у анаэробной микрофлоры -Лежит в основе молочнокислого брожения у бактерий, спиртового брожения у дрожжей -Основной источник энергии для анаэробной микрофлоры полости рта, содержащей сахарозу -Следствие: накопление лактата в зубном налете привоит к деминирализаци твердых тканей зуба. -Фактор риска развития кариеса.
4) Регуляция кислотно-основного равновесия полости рта осуществляется ротовой жидкостью за счет ее буферных свойств, которая обеспечивается в большей степени бикарбонатом
48) 1)Пентозофосфатный цикл (шунт) превращение глюкозы (гексо-монофосфатный путь). - Пентозофосфатный цикл-альтернативный путь окисления глюкозы -Апотомический распад (без образования фосфотриоз) -Протекает в 2 стадии без участия О2 -В процесс вступают 6 молекул глюкоз ы -Не приводит к синтезу АТФ -Локализован в цитоплазме клеток: печени, молочной железы, коры надпочечников,эритроцитов, жировой ткани. -Стадии Пентозофосфатного цикла: Окислительная-приводит к обраованию НАДФН2, Неокислительная-приводит к образованию пентоз. 2) Окислительная стадия Пентозофосфатного цикла 1.Глюкозо-6ф-дегидрогеназа (ингибитор-НАДФН2, индуктор-инсулин) 2. Глюколактонгидратаза 3. 6-фосфоглюконатдегидрогеназа (декарбоксилирующаю; индуктор-инсулин) 3) Общее уравнение Пентозофосфатного цикла 6глюкозо-6ф+12НАДФ+→6СО2+12НАДФН2+5 глюкозо-6ф 3)
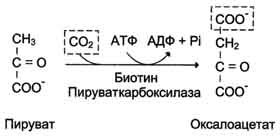
49) Глюконеогенез- то процесс синтеза глюкозы из в.в неуглеводной природы в организме человека и животных. Химизм глюконеогенеза. Процесс активно протекает в печени, менее активно в почках, слизистой кишечника. Контролируетя гормонами коры надпочечников -глюкокортикоидами (кортизол). протекает по тому же пути что и гликолиз (обртимо), за исключением 3-х обходных реакций. Рассмотрим более подробно те реакции глюконеогенеза, которые отличаются от реакций гликолиза и происходят в глюконеогенезе с использованием других ферментов. Рассмотрим процесс синтеза глюкозы из пирувата. 1. Образование фосфоенолпирувата из пирувата - первая из необратимых стадий глюконеогенеза Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций(рис 1 реакции 11,12), первая из которых протекает в митохондриях. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата.(рис 2) Пируват-карбоксилаза, катализирующая данную реакцию, - митохондриальный фермент, коферментом которого является биотин. Реакция протекает с использованием АТФ.
Рис. 1. Гликолиз и глюконеогенез. Ферменты обратимых реакций гликолиза и глюконеогенеза: 2 - фосфоглюкоизоме-раза; 4 - альдолаза; 5 - триозофосфатизомераза; 6 - глицеральдегидфосфатдегидрогеназа; 7 -фосфоглицераткиназа; 8 - фосфоглицератмутаза; 9 - енолаза. Ферменты необратимых реакций глюконеогенеза: 11 - пируваткарбоксилаза; 12 - фосфоенолпируваткарбоксикиназа; 13 - фруктозо-1,6-бисфосфатаза; 14 -глюкозо-6-фосфатаза. I-III -субстратные циклы.
рис 2. Образование оксалоацетата из пирувата.
2. Гидролиз фруктозо-1,6-бисфосфата и глюкоза-6-фосфата
Отщепление фосфатной группы из фруктозо-1,6-бисфосфата и глюкозо-6-фосфата - также необратимые реакции глюконеогенеза. В ходе гликолиза эти реакции катализируют специфические киназы с использованием энергии АТФ
3.Энергетический баланс глюконеогенеза из пирувата
В ходе этого процесса расходуются 6 моль АТФ на синтез 1 моль глюкозы из 2 моль пирувата. Четыре моль АТФ расходуются на стадии синтеза фосфоенолпирувата из оксалоацетата и ещё 2 моль АТФ на стадиях образования 1,3-бисфосфоглицерата из 3-фосфоглицерата.
Суммарный результат глюконеогенеза из пирувата выражается следующим уравнением: 2 Пируват + 4 АТФ + 2 ГТФ + 2 (NADH + Н+)+ 4 Н20 → Глюкоза + 4 АДФ + 2 ГДФ + 6 H3PO4 + 2 NAD+
Биологическое значение глюконеогенеза. Общее уравнение глюконеогенеза. 2 лактата+4 АТФ+2ГТФ+4Н2О→1 глюкоза +4А Д Ф+2 Г Д Ф+6 Фн - Поддержание постоянного уровня глюкзы в крови связано с тем что для многих тканей глюкоза является основным (нервная ткань), а для некоторых единственным (эритроциты) источником энергии - В условиях длительного голодания (24 час)- единственный источник глюкозы в организме (до 80г/сут) предупреждает развитие гипогликемии -Утилизация лактата- предупреждает развитие лактатцидоза
50) 1) Непоседственно синтез гликогена осуществляют следующие ферменты: - Фосфоглюкомутаза- превращает глюкозо-6-фосфат в глюкозо 1- фосфат - Глюкозо 1-фосфат-уридилтрансфераза -ферент, осуществляющий ключевую реакцию синтеза. Необратимость этой реакции обеспечивается гидролизом образующегося дифосфата. - Гликогенсинтаза- образует α1,4-гликозидные связи и удлиняет гликогеновую цепочку -Амило α1,4-α1,6-гликозилтрансфераза (гликоген-ветвящий фермент)-переносит фермент с минимальной длиной в 6 остатков глюкозы на соседнюю с образованием α-1,6-гликозидной цепи. 2) Мобилизация гликогена(гликогенолиз) Резервы гликогена исп-ся по-разному в зависимости от функциональных особенностей клетки. -Гликоген печени расщепляется в интервалах между приемами пищи. Через 12-18 часов голодания запасы гликогена в печени полностью истощаются. - В мышцах кол-во гликогена снижается при физической нагрузке-длительной и/или напряженной -Уровень глюкозы крови поддерживает только печень, в котрой имеется глюкозо-6-фосфатаза. Образуемая в гепатоците свободная глюкоза выходит через плазматическую мембрану в кровь - Остальные органы используют гликоген только для собственных нужд 3) регуляция метаболизма гликогена - Процессы биосинтеза и распада гликогена согласованы с потребностями организма в глюкозе. -Одновременное протекание этих процессов невозможно (бесполезная растрата АТФ) -Изменение направления процессов в метаболизме гликогена обеспечивают регуляторные механизмы (гормоны) Печень-инсулин, глюкагон, адреналин, Мышцы- Инсулин, Адреналин При действии горомонов на клетку происходит активация фермента через аденилатциклазный механизм, который является так называемым каскадным регулирванием. Роль каскада: -Регулирует метаболизм гликогена - Регулирует уровень глюкозы в крови -Усиливает гормональный сигнал на каждом этапе каскада "мобилизация гликогена" 51) 1) Результат регуляции метаболических путей превращения глюкозы - постоянство концентрации глюкозы в крови. Концентрация глюкозы в артериальной крови в течение суток поддерживается на постоянном уровне 60-100 мг/дл (3,3-5,5 ммоль/л). После приёма углеводной пищи уровень глюкозы возрастает в течение примерно 1 ч до 150 мг/дл
Рис. 7-58. Синтез жира из углеводов. 1 - окисление глюкозы до пирувата и окислительное декарбоксилирование пирувата приводят к образованию ацетил-КоА; 2 - ацетил-КоА является строительным блоком для синтеза жирных кислот; 3 - жирные кислоты и а-глицеролфосфат, образующийся в реакции восстановления дигидроксиацетонфосфата, участвуют в синтезе триа-цилглицеролов. (∼8 ммоль/л, алиментарная гипергликемия), а затем возвращается к нормальному уровню (примерно через 2 ч). На рисунке 7-59 представлен график изменений концентрации глюкозы в крови в течение суток при трёхразовом приёме пищи.
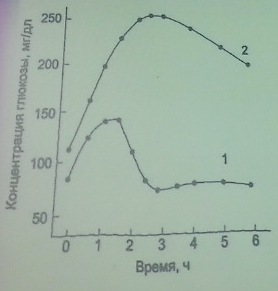
Рис. 7-59. Изменение концентрации глюкозы в крови в течение суток. А, Б - период пищеварения; В, Г - постабсорбтивный период. Стрелкой указано время приёма пищи, пунктиром показана нормальная концентрация глюкозы.
2)- Гипоглиемия-снижение концентрации глюкозы в крови - Избыток глюкозы в крови полсе приема углеводной пищи, снижение потребления глюкозы органами и танями, усиление ее образования в печен приводит к гипергликемии
3) Оценка толерантности организма к глюкозе.Метод "сахарной нагрузки" Обследуемый принимает раствор глюкозы из расчета 1г/кг массы (2сахарная нагрузка") Концентрацию глюкозы в крови измеряют в течение 2-3 ч с интервалом в 30 мин. Результаты представлены в виде графика. 1-норма, 2-нарушение толерантности
Обмен липидов 52. Основные липиды тканей человека, химическое строение, свойства, физиологическое значение. 53. Нормы суточного потребления жиров, особенности переваривания и всасывания. Образование и функции желчных кислот. Переваривание и всасывание, ресинтез жиров в клетках стенки кишечника. Хиломикроны, строение, функции. 54. Ненасыщенные жирные кислоты. Зависимость их концентрации от питания. Физиологическое значение. Простагландины, лейкотриены, их роль в регуляции метаболизма и физиологических функций. 55. Основные фосфолипиды тканей человека, строение и биологические функции. Биосинтез фосфолипидов. Липотропные факторы, их значение, проявление недостаточности. 56. Транспортные липопротеины крови, особенности строения, состава, функций. Липопротеинлипазы. Дислипопротеинемии, гиперлипопротеинемии. 57. Депонирование и мобилизация жиров, биологическая роль процессов, регуляция, зависимость от ритма питания и физической нагрузки. 58. Окисление высших жирных кислот. Последовательность реакций -окисления. Связь окисления жирных кислот с цитратным циклом и дыхательной цепью. Физиологическое значение. 59. Биосинтез и использование кетоновых тел, концентрация их в крови и моче в норме. Факторы, активирующие кетогенез. Кетонемия, кетонурия. 60. Обмен и функции холестерина. Биосинтез холестерина, регуляция процесса. Транспорт и выведение холестерина из организма. 61. Гиперхолестеринемия, причины и последствия. Биохимические основы патогенеза атеросклероза, профилактика и коррекция гиперхолестеринемии. 62. Взаимосвязь обмена жиров и углеводов. Схема образования жиров из глюкозы. Особенности метаболизма жировой ткани. Ожирение.
52) Наиболее распространенные липиды- это нейтральные жиры, структурным компонентом которых, как и большинства липидов, являются жирные кислоты. Жирные кислоты липидов человека представляют собой углеводородную неразветвлённую цепь, на одном конце которой находится карбоксильная группа, а на другом - метальная группа (ω-углеродный атом). Большинство жирных кислот в организме содержат чётное число атомов углерода - от 16 до 20. Жирные кислоты, не содержащие двойных связей, называют насыщенными. Основной насыщенной жирной кислотой в липидах человека является пальмитиновая (до 30-35%). Жирные кислоты, содержащие двойные связи, называют ненасыщенными. Ненасыщенные жирные кислоты представлены моноеновыми (с одной двойной связью) и полиеновыми (с двумя и большим числом двойных связей). Если в составе жирной кислоты содержатся две и более двойных связей, то они располагаются через СН2-группу.
Примечания: Cn:m - число атомов углерода (n) и число двойных связей (m) в молекуле жирной кислоты; w (6,3) - номер углеродного атома, у которого находится первая двойная связь, считая от w- (метильного) атома углерода; D - позиция двойной связи, считая с первого, карбоксильного атома углерода; * - жирные кислоты, которые не синтезируются в организме (незаменимые); ** - арахидоновая кислота может синтезироваться из линолевой кислоты.
Жирные ксилоты, входящие в состав липидов животных и высших растений, имеют много общих свойств. Как уже отмечалось, почти все природные жирные кислоты содержат четное число углеродных атомов, чаще всего 16 или 18. ненасыщенные ЖК животных и человека, участвующие в построении липидов, обычно содержат двойную связь между 9-м и 10-м атомами углерода; дополнительные двойные связи, как правило, бывают на участке между 10-м атомом углерода и метильным концом цепи.
53) 1) Потребность в жирах -80-100г/сут, →ТАГ 1/3-1/2-энергетической ценности пищи: Животные жиры 75%, Растительное масло 25%(ПНЖК). Фосфолипиды, Холестерин 2) особенности переваривания и всасывания - Ассимиляция пищевых жиров *Включает все этапы метаболизмы пищевых ТАГ, начиная с переваривания их с ЖКТ и заканчивая распределения продуктов гидролиза по всем тканям *Все природные липиды хорошо перевариваются *При смешанном питании Так как липиды не растворимы в Н2О их переваривание имеет свои особенности и протекает в неск стадий. *Липиды при механическом воздействии под влиянием желчи смешиваются с пищеварительными соками с образованием эмульсии ("масло в Н2О") Образование эмульсии необходимо для увеличения площади действия ферментов, т.к. они работают только в водной фазе. Липиды жидкой пищи (молоко, бульон) поступают сразу в виде эмульсии * Под действием ферментов происходит гидролиз липидов эмульсии с образованием водорастворимых простых липидов *Выделенные из эмульсии простые липиды соединяясь с компонентами желчи образуют мицеллы *Мицеллы обеспечивают всасывание липиды в клетках эндотелия кишечника. - Основной процесс переваривания липидов происходит в тонком кишечнике 1. Эмульгирование липидов происходит под действием желчных кислот 2. Желчные кислоты синтезируются в печени, концентрируются в желчном пузыре в составе желчи 3. После приема жирной пищи желчь выделяет в просвет 12-перстной кишки (500-1500 мг/сут) 2) Желчные кислоты синтезируются в печени из холестерина. В желче желчные кислоты присутствуют в основном в виде конъюгатов с глицином (66-805) и таурином (20-345), образуя парные желчные кислоты: таурохолевую, гликохолевую Функции желчных кислот: Эмульгирующая располагаясь на поверхности раздела фаз жир-вода, препятствуют их расслаиванию Активация липазы Способствуют всасыванию продуктов переваривания и жирорастворимых витаминов 3) Гидролиз ТАГ в тонком кишечнике осуществляет панкреатическая липаза оптимум рН=8, * гидролизует ТАГ преимущесвено в положениях 1 и 3, с образованием 2 ЖК и моноацилглицерола *часть МАГ гидролизуется до глицерина и ЖК
Ресинтез ТАГ в клетках слизистой кишечника. Большая часть продуктов переваривания вновь превращается в ТАГ. При ресинтезе образуются водоспецифические жиры (более свойственные нашму организму, а не пищевому жиры). Ресинтезированные жиры транспортируюся в лимфу, затем в кровь в составе транспортных форм- хиломикронов. 4) Хиломикроны -надмолекулярные комплексы сферической формы, состоящих из липидов, белков аполипротеинов,-апо *В гидрофильную оболочку входят белки и амфифильные ФЛ, ХС *В гидрофобное ядро входят гидрофобные липиды -85% ТАГ, ЭХС *Созревание хиломикронов в крови при включении в состав апопротеинов
54) 1) В тканях млекопитающих присутствуют ненасыщенные жирные кислоты, различающиеся длиной алифатической цепи между концевой метильной группой и ближайшей двойной связью. Установлено что наиболее распространенные мононенасыщенные жирные кислоты -пальмитоолеиновая и олеиновая-синтезируются из пальмитиновой и стеариновой кислот. Образование двойной связи происходит в микросомах клеток печени и жировой ткани при участии специфической оксигеназы и молекулярного кислорода. В этой реакции одна молекула кислорода используется в качестве акцептора двух пар электронов, одна из которых принадлежит субстрату (Ацил-КоА), а другая -НАДФН2:
Пальмитоил-КоА Пальмитоолеил- КоА С15Н31-СО-S-КоА+НАДФН2+О2→СН3-(СН2)5-СН=СН-(СН2)7-СО-S-КоА+НАДФН2++2Н2О Вместе с тем ткани человека и ряда животных, неспособны синтезировать линолевую и линоленовую кислоты, а долны получать их с пищей. Биологическая роль полиненасыщенных жирных кислот в значительнй мере прояснилась с открытием нового класса актиных соединений - простагландинов.
2) Эйкозаноиды, включающие в себя простагландины, тромбоксаны, лейкотриены и ряд других веществ, - высокоактивные регуляторы клеточных функций
- Структура и номенклатура простагландинов и тромбоксанов
Простагландины (рис. 8-45) обозначают символами, например PG А, где PG обозначает слово "простагландин", а буква А обозначает заместитель в пятичленном кольце в молекуле эйкозаноида.
Каждая из указанных групп простагландинов состоит из 3 типов молекул, отличающихся по числу двойных связей в боковых цепях. Число двойных связей обозначают нижним цифровым индексом, например, PG Е2.
Число двойных связей в боковых цепях простагландинов зависит от структуры предшественника - полистовой кислоты, из которой образовались простагландины. Две двойные связи полиеновой кислоты используются при образовании кольца в молекуле простагландина, а количество оставшихся двойных связей в радикалах, связанных с кольцом, определяет серию простагландина: 1 - если одна двойная связь, 2 - если две двойные связи и 3 - если в радикалах имеются три двойных связи.
PG I - простациклины. Имеют 2 кольца в своей структуре: одно пятичленное, как и другие простагландины, а другое - с участием атома кислорода. Их также подразделяют в зависимости от количества двойных связей в радикалах (PG I2, PG I3).
Структура и синтез лейкотриенов, ГЭТЕ, липоксинов
Лейкотриены также образуются из эйкозаноевых кислот, однако в их структуре отсутствуют циклы, как у простагландинов, и они имеют 3 сопряжённые двойные связи, хотя общее число двойных связей в молекуле больше (рис. 8-49). Лейкотриены С4, D4 и Е4 имеют заместители в виде трипептида глутатиона, дипептида глицилцистеина или цистеина, соответственно.
Липоксигеназный путь синтеза, приводящий к образованию большого количества разных эйкозаноидов, начинается с присоединения молекулы кислорода к одному из атомов углерода у двойной связи, с образованием гидропероксидов - гидропероксидэйкозатетраеноатов (ГПЭ-ТЕ). Далее гидропероксиды превращаются в соответствующие гидроксиэйкозатетроеноаты (ГЭТЕ).
Структура и синтез лейкотриенов и ГЭТЕ
Синтез лейкотриенов идёт по пути, отличному от пути синтеза простагландинов, и начинается с образования гидроксипероксидов - ги
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-17; просмотров: 283; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.235.195 (0.013 с.) |