Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дрібношматкові напівфабрикатиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Рагу. Тушки птиці, кролика розрубують на шматки по 3—4 шт. на порцію, масою 30—40 г кожна. Плов. Тушку птиці, кролика або дичини розрубують на шматки по 1-2 шт. на порцію. Гуска або качка по-домашньому. Тушки качки або гуски розрубують на шматки по 4—5 шт. на порцію. Ч а х о х б і л і. Тушки курки розрубують на порційні шматки. Котлетна маса. М’ясо птиці без шкіри і кісток нарізують шматочками, пропускають через м’ясорубку разом з внутрішнім жиром, з’єднують із замоченим у молоці або воді пшеничним хлібом без скоринок, додають сіль, а для маси з дичини — перець, перемішують, ще раз пропускають через м’ясорубку і вибивають. Для котлетної маси використовують тушки курей, індиків, рябчиків, куріпок, глухарів, фазанів. З тушок сільськогосподарської птиці використовують м’якоть філе і ніжок, а з тушок дичини (крім фазанів і курток) — тільки філе. Готову котлетну масу розподіляють на порції і формують котлети, биточки. Панірують у сухарях або тертому білому хлібі (для лавірування котлет пожарських хліб нарізають кубиками). Кнельна маса. Зачищену м’якоть курячого філе або дичини два рази пропускають через м’ясорубку спочатку з середньою, а потім з густою решіткою, кладуть замочений у молоці або вершках черствий пшеничний хліб без скоринки (можна листкове тісто або холодну рисову кашу), перемішують і знову пропускають через м’ясорубку. Після цього масу розтирають у ступці і протирають крізь сито. Протерту масу охолоджують і збивають, доливаючи невеликими порціями яєчний білок, вершки. В готову кнельну масу додають сіль і обережно перемішують. Добре збита кнельна маса має ніжну пухку консистенцію. На 1 кг м’яса беруть 100 г хліба, 150 г молока, 200 г вершків, 3 г яєчного білка, 15 г солі. Для приготування великої кількості кнельної маси використовують спеціальні машини. З кнельної маси можна приготувати галушки різної форми для супів-пюре. Для кнелів парових масу готують у формочках на парі як окрему страву і подають з різними соусами. Вимоги до якості напівфабрикатів з птиці і дичини Поверхня шкіри тушок птиці повинна бути без колодочок і волосків, без слизу, суха. Колір — блідо-рожевий. М’язова тканина щільна, пружна. При натискуванні пальцями ямка, що утворилася, швидко вирівнюється. Запах специфічний, властивий свіжому м’ясу відповідного виду птиці. Допускаються незначні опіки, два-три прорізи шкіри 2 см завдовжки. Тушки не повинні мати згустків крові і ділянок, в які просочилась жовч. Напівфабрикати повинні мати правильну форму, бути рівномірно запанірованими, без тріщин і ламаних країв. Котлети натуральні — без шкірки і поверхневої плівки, сухожилки перерізані в двох-трьох місцях, плечова кістка зачищена від м’якоті З— 4 см завдовжки з обрубаною частиною гомілки. Маса кісточки — 5 г. Всередині напівфабрикату може бути мале філе або 1—2 шматочки іншого філе. Форма філе овальна. Колір — від біло^рожевого до рожевого, запах — властивий свіжому курячому м’ясу, консистенція — щільна, пружна. Котлети паніровані повинні відповідати тим вимогам, що і котлети натуральні, але їхня поверхня має бути вкрита рівним шаром білої па- ніровки, яка не відстає і незволожена. Дрібношматкові напівфабрикати — акуратно нарубані, однакової форми, шматки необвітрені, без стороннього запаху. Напівфабрикати з котлетної маси повинні зберігати форму. Поверхня рівномірно запанірована, без тріщин, ламаних країв, консистенція — м’яка, однорідна, без шматків хліба і сухожилків, запах — властивий доброякісному м’ясу. Напівфабрикати зберігають при температурі не вищій за 6°С. Оброблені тушки укладають залежно від виду в металеві ящики або лотки в один ряд. Зберігають при температурі від 0 до 4°С не більше як 36 год. Котлети натуральні, паніровані і вироби з котлетної маси укладають під кутом 30°С на ребро, котлети фаршировані — в один ряд, котлетну масу — на лотки шаром 5—7 см. Паніровані котлети зберігають до 24 год., вироби з котлетної маси — 12, субпродукти, супові набори і кістки до 18 год. 5.5. Обробка субпродуктів птиці й дичини До субпродуктів сільськогосподарської птиці відносять голови, гребінці, шийки, крильця, ніжки, серце, шлунок, шкіру і обрізки, які залишилися після приготування напівфабрикатів, а в дичини — шийки (інші відходи мають гіркий смак). Субпродукти обробляють і використовують для приготування страв. Ніжки птиці обсмалюють або обшпарюють. Потім знімають ороговілий шар, відрубують кігті, промивають і використовують для приготування бульйонів і холодців. Голови обшпарюють, зачищають від пір’я і залишків крові, відрізають гребінці, видаляють дзьоб, очі і промивають. Використовують для приготування бульйонів і холодцю. Шиї, крильця обшпарюють, видаляють пір’я, обсушують, натираючи борошном, і обсмалюють. Зачищають від колодочок і промивають, з шиї зчищають згустки крові. Використовують для приготування бульйонів, рагу, холодцю. З гребінців знімають плівку, промивають. Використовують для приготування холодцю, заливних гребінців. У печінки зрізають жовчний міхур разом з частиною протоки так, щоб не порушити його цілісності. Якщо на печінці є сліди жовчі, їх необхідно зрізати. Використовують для приготування паштетів, супів-пюре. З шлунка видаляють залишки їжі разом з оболонкою, добре промивають. Використовують для приготування бульйону, рагу.Серце вивільняють із навколосерцевої сумки, згустків крові, використовують для приготування бульйонів, рагу. 5.6. Напівфабрикати, що надходять із заготівельних фабрик Сировиною для виробництва напівфабрикатів із сільськогосподарської птиці є кури, курчата, індички, качки, їхні тушки, розібрані і підготовлені до кулінарної обробки, надходять заправленими «в кишеньку», «в одну нитку». Для підприємств харчування філе куряче або індиче з кісточкою виробляють порційними шматками масою 90 г, для реалізації в магазинах — ваговими. Грудинка — частина качиної або курячої тушки, яка складається з грудної кісточки з прилеглими до неї м’язами і шкірою. Окісточки курячі, індичі або качині — м’якоть з шкірою і кісточками (стегновою, гомілковою), їх випускають ваговими. Набір для бульйонів — частина однієї тушки з шкірою, яка залишилася після відокремлення філе й окісточків, а також оброблені потрухи. Набір для холодцю — оброблені підготовлені голови, ноги, шиї, крила, шлунки і серце. Надходять розфасованими масою 500 і 1000 г. Напівфабрикати, що випускають фасованими на порції, запаковують у плівку. Кожну порцію перев’язують шпагатом, скріплюють або заклеюють. Напівфабрикати укладають у дерев’яний ящик, полімерний або металевий. Перед відправленням на підприємства харчування їх охолоджують до температури 4—8°С. На упаковці або ярлику, які вкладають у кожну одиницю упаковки, друкарським способом зазначають: назву підприємства-виробни- ка, його підпорядкованість і товарний знак, найменування напівфабрикату, масу і ціну порції, дату і час виготовлення, строки зберігання і реалізації, номер або прізвище пакувальника, стандарт. Напівфабрикати зберігають при температурі від 4 до 8°С, натуральні напівфабрикати із птиці — 48 год. напівфабрикати із субпродуктів — 12 год., котлетної маси — 6 год. Розділ 6 ПРОЦЕСИ, ЯКІ ВІДБУВАЮТЬСЯ ПІД ЧАС КУЛІНАРНОЇ ОБРОБКИ ПРОДУКТІВ У результаті фізико-хімічних змін, які відбуваються під час теплової обробки з білками, жирами, вуглеводами, вітамінами, мінеральними, смаковими і ароматичними речовинами, виникають процеси, які впливають на харчову цінність продуктів, а також на їх засвоюваність, смак, запах і зовнішній вигляд. ДИФУЗІЯ У процесі промивання, замочування, варіння і припускання продукти контактують з водою. У цей час з них можуть виходити поживні речовини. Цей процес називають дифузією. Швидкість дифузії залежить від площі поверхні продукту. Чим більша поверхня продукту, тим швидше проходить дифузія. Швидкість дифузії залежить від концентрації розчинних речовин у продукті і в навколишньому середовищі. Якщо концентрація розчинних речовин у продукті і в навколишньому середовищі зрівнюється, дифузія припиняється. Чим менший об’єм рідини в навколишньому середовищі, тим швидше встановлюється рівновага. Цим пояснюється те, що під час припускання і варіння продуктів парою втрати розчинних речовин менші, ніж під час варіння основним способом. Тому для зменшення втрат поживних речовин під час варіння овочів, м’яса та інших продуктів рідини беруть стільки, щоб вона покривала продукт. І навпаки, якщо потрібно видалити якнайбільше розчинних речовин, то води для варіння беруть більше (варіння нирок). Під час варіння супів, соусів відвар не зливають, тому перехід в нього розчинних речовин суттєвого значення не має. Якщо відвар зливають, то його можна використати, оскільки в ньому знаходиться багато поживних речовин із продуктів (круп, макаронних виробів, риби, м’яса, овочів, птиці). Втрату поживних речовин можна зменшити шляхом вологопере- несення. Якщо класти овочі в гарячу воду, то розчинні речовини з поверхневих шарів переміщаються до центру бульби або коренеплоду, і перехід їх в рідину зменшується. 6.1. Зміни білків ХІМІЧНА ПРИРОДА БІЛКІВ Білки — це основний пластичний матеріал, з якого будується тканина тіла. Це складні речовини; їх молекули складаються із залишків амінокислот, які з’єднані в довгі ланцюжки (поліпептидні ланцюжки). У кожну молекулу білка входять тисячі і десятки тисяч залишків амінокислот. У складі білків їх близько 30-ти видів. Під час харчового травлення білки розкладаються на окремі амінокислоти, які всмоктуються в організм і з яких будуються білки нашого тіла. Окремі амінокислоти можуть в організмі переходити в інші, але вісім із них не можуть синтезуватися в організмі і повинні поступати з їжею, їх називають незамінними. Для повного засвоєння білків в їжі мають бути всі незамінні амінокислоти в тих співвідношеннях, в яких вони входять в білки нашого організму. Такими повноцінними білками є більшість білків м’яса, риби, яєць, молока. У більшості білків рослинного походження не вистачає незамінних амінокислот. Наприклад, у гречаній крупі недостатньо лейцитину, а в рисовій крупі і пшоні — лізину та ін. Один продукт може доповнювати інший за видом незамінних амінокислот. Але таке взаємне збагачення відбувається в тому випадку, коли ці продукти поступають в організм протягом двох годин. БУДОВА МОЛЕКУЛИ БІЛКІВ За формою молекули всі білки поділяються на глобулярні і фібри- лярні. Молекула глобулярних білків за формою близька до кульок (глобули), а фібрилярні молекули мають форму видовжену (ниткоподіб- ну). Молекули білків побудовані з великої кількості амінокислот, які зв’язані між собою в довгі ланцюжки поліпептидів за допомогою по- ліпептидного зв’язку — СО—ІЧН—. У молекулі різних білків амінокислоти з’єднуються у відповідній послідовності, яка називається первинною структурою білка. У глобулярних білках поліпептидні ланцюжки амінокислот згортаються у вигляді колобка. Це вторинна структура. В середині глобули ланцюжки амінокислот розміщені у відповідному порядку і утримуються нестійкими водневими зв’язками. Від того, як розмішені ланцюжки амінокислот, залежать властивості білка гідратація (властивість зв’язувати воду), розчинність (у воді і соляних розчинах); індивідуальні властивості (забарвлення, активність), стійкість проти дії травних ферментів. У фібрилярних білках молекули складаються із довгих поліпептид- них ланцюжків, які мають форму спіралі. ГІДРАТАЦІЯ І ДЕГІДРАТАЦІЯ БІЛКІВ Властивість білків тісно зв’язувати значну кількість вологи називається гідратацією. Вона обумовлена тим, що молекули білка утримують воду за рахунок утворення гідратної оболонки і за рахунок адсорбції (зв’язування молекули води за рахунок водних зв’язків). У розчинах з малою концентрацією білка (молоко, рідке тісто) білки повністю гідратовані і більше зв’язувати воду не можуть. У випадку, коли в продукті мало вологи, білки гідратовані не повністю і можуть зв’язувати деяку кількість її (яйця, борошно). Властивість додаткової гідратації має велике значення в технології приготування їжі. Наприклад, від властивості додаткової гідратації залежить водопог- линаюча властивість борошна, тобто властивість утворювати тісто. Додаткова гідратація проходить при додаванні води до січеної маси м’яса (біфштекси, фрикадельки, фарш для пельменів). Від ступеня гідратації залежить соковитість готових виробів, властивість напівфабрикатів із м’яса і риби втримувати вологу. Дегідратація — це втрата білками зв’язаної води під час сушіння, заморожування і розморожування м’яса та риби, теплової обробки напівфабрикатів. Від ступеня дегідратації залежать такі важливі показники, як вологість готових виробів і їх вихід. ЗМІНИ ГЛОБУЛЯРНИХ І ФІБРИЛЯРНИХ БІЛКІВ При підвищенні температури посилюється тепловий коливний рух окремих залишків амінокислот у ланцюжках, водневі зв’язки між ними розриваються і відбувається перегрупування частини амінокислотних ланцюжків. Поліпептидний ланцюжок розгортається і формується по- новому. Така зміна будови молекули глобулярних білків називається денатурацією (рис. 51).
В результаті денатурації змінюється форма молекули білка, розміщення полярних і неполярних груп, натуральні властивості білка. Таким чином у результаті перегрупування полярних груп знижується здатність білка зв’язувати полярні молекули води і білки частково втрачають здатність набухати; перегрупування активних груп приводить до втрат багатьма білками стійкості проти дії ферментів, і білки легше розкладаються трепсином; білки втрачають здатність розчинятися. Зниження властивості зв’язувати воду є основною причиною зменшення маси м’яса і риби під час варіння і смаження. Втрата стійкості проти дії ферментів підвищує засвоюваність білків багатьох продуктів після їх теплової обробки. Винятком є білок (казеїн сиру), який після теплової обробки важче гідролізується травними ферментами. Денатурацію може викликати не тільки нагрівання, а й дія солей важких металів, дубильні речовини, збивання та ін. В результаті денатурації відбувається згортання білків. Воно полягає в тому, що воднева захисна оболонка на поверхні білкових частин під час денатурації руйнується, частинки легко з’єднуються одна з одною і збільшуються. Згортання буває трьох видів: а) якщо концентрація білків була незначною, то згорнуті білки утворюють пластівці на поверхні м’ясних, рибних і овочевих відварів; б) якщо концентрація білків була великою, то при згортанні вони утворюють щільну студенисту масу — гель (білки яєць); в) якщо білок в продукті знаходиться вже у вигляді гелю, то при згортанні він ущільнюється і виділяється рідина. У фібрилярних білках колаген та ін. викликають зміни іншого характеру. Поліпептидні ланцюжки в них витягнуті і зв’язані один з одним водневими зв’язками. При нагріванні рух поліпептидних ланцюжків посилюється, водневі зв’язки між ними розриваються, і це призводить до двох характерних явищ: а) волокна білка розриваються на окремі ланцюжки амінокислот (дезагрегація); б) амінокислотні ланцюжки скорочуються за рахунок розриву внутрішніх зв’язків (зварювання). БІЛКИ М’ЯСА Будова м’язової тканини м’яса М’язова тканина м’яса складається з м’язових волокон. Довжина їх сягає 10—12 см, а товщина — 0,1—0,15 мм. Поверхня м’язового волокна покрита оболонкою — сарколемою (саркос — м’ясо, лема — шкіра), яка складається з фібрилярного білка колагену і ліпідів (жирів). В середині волокна знаходиться саркоплазма (плазма — рідина). Це розчин мінеральних речовин, водорозчинних білків, вітамінів і інших речовин. Водорозчинні білки саркоплазми — міоген, міоглобін, мю- альбумін, глобулін та ін. У рідкій саркоплазмі знаходиться студне- подібні нитки — міофібрили, які складаються з солерозчинних білків міозину, актину, актоміозину (рис. 52).
Окремі м’язові волокна з’єднуються в первинні пучки, а декілька первинних пучків з допомогою ніжної сполучної тканини — ендомі- зію (ендо — внутрішній) з’єднуються у вторинні пучки. Вторинні пучки з допомогою більш грубішої сполучної тканини — перемізію (про- міжковий) утворюють м’яз, який зверху покритий ще більш грубішою сполучною тканиною — епімізієм (зовнішній). Внутрішня сполучна тканина (ендомізій) складається із тонких колагенових волокон. Проміжкова сполучна тканина (перемізій) складається із колагенових і еластинових волокон (рис. 53).
Зміни білків м’яса під час кулінарної обробки Білки сарколеми дуже стійкі, і навіть під час довгого нагрівання при температурі 120°С структура їх не змінюється. Тому після теплової обробки м’язові волокна зберігаються, і розварене м’ясо можна подрібнити на пучки або окремі м’язові волокна. Білки саркоплазми, які знаходяться в розчиненому стані, денатурують і утворюють щільний гель (студень), оскільки концентрація їх велика. Цей процес починається вже при температурі ЗО—35°С, а при температурі 65°С денатурує близько 90% всіх розчинних білків саркоплазми. Однак навіть при нагріванні м’яса до 95—100°С не відбувається повної денатурації білків і деяка частина їх зберігає властивість розчинятися. Білки міофібрил, які мають вигляд гелю, при нагріванні ущільнюються і від утвореного студня відокремлюється значна частина води разом з розчиненими в ній поживними речовинами. Частина цієї води переходить в простір між волокна, тому діаметр м’язових волокон зменшується, вони стають щільнішими і міцнішими. Під час варіння м’яса і птиці, поки ще продукти не прогрілись, частина водорозчинних білків (міоген) переходить у воду. При дальшому нагріванні вони згортаються і спливають на поверхню бульйону у вигляді піни. Якщо воду, в якій вариться м’ясо або птиця, посолити перш ніж продукти прогріються, то в розчин перейде більше білків за рахунок глобулінів (солерозчинних) і кількість піни збільшиться. Тому при варінні м’яса воду солять після того, як м’ясо прогріється. Одночасно із змінами білків м’язової тканини змінюються також білки сполучної тканини. Ендомізій складається з волокон фібрилярного білка — колагену. У всіх частинах туші ендомізій має однакові властивості. Перемізій складається не тільки з волокон колагену, а й з волокон іншого фібрилярного білка — еластину. Перемізій в окремих частинах туші не однаковий і його властивості визначають кулінарне використання частин м’яса. При нагріванні м’яса в процесі кулінарної обробки еластинові волокна змінюються мало. Колагенові волокна при температурі близько 60°С зварюються, скорочуються майже на половину своєї початкової довжини. В результаті зварювання колагену шматки м’яса під час смаження або варіння деформуються, м’ясний сік разом з розчиненими білками, екстрактивними речовинами і мінеральними солями виходить в навколишнє середовище. Це призводить до зменшення маси напівфабрикатів. Щоб шматки м’яса, особливо при смаженні, не деформувалися, їх відбивають, роблять надрізи, перетинаючи сполучну тканину. Одночасно проходить набухання колагенових волокон. При дальшому нагріванні розриваються водневі зв’язки між окремими амінокислотними ланцюжками. Нерозчинений колаген перетворюється в більш просту розчинну речовину — глютин. Кулінарна готовність м’ясних виробів обумовлена ступенем розкладу колагену і розм’якшенням тканин. Швидкість розкладу колагену залежить від кількох причин. Чим грубіша сполучна тканина, тим повільніше розкладається колаген. Розклад колагенових волокон супроводжується поглинанням значної кількості вологи. Тому для смаження придатні тільки ті частини туші, в яких перемізій достатньо ніжний і значна частина колагену встигає перетворитися в глютин за час, коли основна частина вологи ще не випарувалася. У більшості частин м’яса великої рогатої худоби перемізій настільки міцний, що таке м’ясо непридатне для смаження і його можна використати тільки для варіння і тушкування. Швидкість переходу колагену в глютин залежить від температури: чим вона вища, тим цей процес відбувається скоріше. Особливо швидко він проходить при температурі 100°С. Значно швидше переходить колаген в глютин в присутності кислот. На цьому базується маринування м’яса перед смаженням і застосування кислих соусів для тушіння м’яса. Розчини, в яких є більше 1 % желатину, при охолодженні утворюють студні (гелі). БІЛКИ РИБИ В основі будови м’язової тканини риби також лежать м’язові волокна. Окремі волокна з’єднуються перемізієм у зигзагоподібні міоко- ми. Міокоми за допомогою горизонтальних і вертикальних прошарків (септ) утворюють тіло риби. Септи — це прошарки сполучної тканини між окремими м’язами (рис. 54). Будову м’язової тканини добре видно у звареної риби, в якої після розм’якшення сполучної тканини добре розділяються міокоми. В м’язових волокнах тканини риб немає білка міоглобіну. Більшість білків риби повноцінні і легко засвоюються організмом. Білки м’язової тканини риби змінюються так само, як білки м’яса, але процес згортання білків риби закінчується при температурі 75°С. Сполучна тканина риби майже повністю складається із колагену і не має еластину.
Септи (поздовжні)
Зварювання колагенових волокон шкіри риби викликає деформацію шматків під час теплової обробки. Тому при виготовленні рибних напівфабрикатів шкіру в декількох місцях перерізають. Зварювання колагенових волокон риби відбувається при нижчій температурі (40°С), ніжу м’яса. Зміни ваги м’яса і риби під час теплової обробки Денатурація білків призводить до зміни їх колоїдного стану — згортання. Білки переходять у розчин, згортаються й утворюють піну. Під час варіння м’яса і риби ущільнюється білковий гель міофібрил, що призводить до зменшення ваги і об’єму продукту. Кількість води, яка виділяється м’ясом і рибою, залежить від ряду причин величини шматків, умов нагрівання та ін. Із м’яса і риби переходять в навколишнє середовище разом з водою розчинені білки, мінеральні солі, екстрактивні речовини.
Виділення води при згортанні білків м’яса проходить більш інтенсивно при 45-75°С, але продовжується до 100°С. У риб цей процес закінчується при 75°С. Зменшення ваги продукту обумовлюється також витопленням із нього жиру (табл. 5).
Екстрактивні речовини м’яса і риби обумовлюють смак і сокогінну дію бульйонів, тому важливим є режим варіння, при якому найбільша кількість цих речовин переходить в розчин. Є два основні прийоми варіння м’яса для одержання бульйонів і для других відварних страв. Для бульйону м’ясо заливають холодною водою, нагрівають до кипіння і варять при слабкому кипінні. В цьому випадку в розчин переходить більше екстрактивних речовин. Для других страв м’ясо закладають у гарячу воду, доводять до кипіння і варять при температурі 85-90°С. При цьому білки утримують більше вологи, менше екстрактивних речовин і білків переходить у розчин. М’ясо стає більш ніжним, соковитим, смачним. Втрати сухих речовин м’яса в середньому становлять 1,5—3% від ваги м’яса. Кількість речовин, що переходить у розчин, залежить від величини шматків, виду м’яса, частин туші. Під час смаження втрачається значно менше поживних речовин, ніж під час варіння, оскільки частина води випаровується з поверхні, а розчинені в ній речовини залишаються і частина з них переходить у м’ясний сік. Вироби, поміщені для смаження в добре розігрітий жир, втрачають менше поживних речовин, менше з них виходить соку і вони стають більш соковитими. БІЛКИ МОЛОКА, ЯЄЦЬ, ОВОЧІВ, ЗЕРНОБОБОВИХ Білки молока. В молоці знаходяться основні три білки: казеїн (2,5— 3%), лактоальбумін (0,5—1%) і лактоглобулін (0,1%). Найбільше в молоці казеїну, який належить до групи фосфоровмісних білків і має виражений кислотний характер. У молоці він знаходиться у вигляді кальцієвої солі. Всі білки мають вигляд золю. При підвищенні кислотності молочна кислота, яка виробляється молочнокислими бактеріями, відокремлює кальцій від солей казеїну, підвищує кислотність молока і утворює драглеподібну масу — гель, який під час кип’ятіння згортається. При дальшому нагріванні він ущільнюється і виділяється вода (одержання сиру). Нагрівання молока викликає денатурацію його білків. Денатурований альбумін зсідається у вигляді пластівців на дні посуду. Цей процес починається при 60°С. Протягом 30 хв. при даній температурі осідає близько 1% альбуміну, а за годину — до 5%. При швидкому нагріванні молока початок випадання пластівців починається при 75°С. Денатурація казеїну виявляється у появі плівки на поверхні молока і починається вже при температурі 40—50°С. Білки яєць. В міс білкових речовин у білку і жовтку курячого яйця різний. В білку їх знаходиться 11—12%, у жовтку-т- 15—16%. Основну масу їх складають овоальбуміни (60-л70%), кональбуміни (10—15%), овоглобуліни. Важливе значення мають фосфоропротеїни — вітелін, лівотин і фос- вітин. Вони знаходяться в жовтку яйця, містять різну кількість фосфору і є добрими емульгаторами, що дозволяє використовувати їх під час виготовлення майонезу. Яйця містять також білки, які є антиферментами і гальмують харчове травлення. Під час теплової обробки антиферменти руйнуються й яйця засвоюються краще. І білок і жовток — концентровані золі. Під час нагрівання білки яєць денатурують, а потім зсідаються. Зсідання яєчного білка починається при температурі 50—55°С. Спочатку з’являється поступове помутніння, при 65°С білок густішає і при 75°С перетворюється в непрозору білу студнеподібну масу ніжної консистенції. При температурі 80° С утворюється гель, що зберігає форму, при дальшому нагріванні він стає все більш щільним. Жовток починає густішати при вищій температурі (70°С). Ціле розмішане яйце густішає при тій самій температурі, що і жовток. Для деяких кулінарних виробів (омлетів) яйце розводять водою або молоком. Розведене яйце дає при зсіданні гель більш ніжної консистенції, ніж натуральне. Додавання цукру до яєць підвищує температуру зсідання. Білки овочів. В овочах білків порівняно небагато. Знаходяться вони в ядрі, протоплазмі і клітинному соці. В сирих овочах з внутрішньої сторони оболонки клітини протоплазма утворює захисну мембрану. Вона запобігає проникненню речовин, розчинених у клітинному соці, у навколишнє середовище під час зберігання овочів у воді. У процесі теплової обробки білки протоплазми зсідаються і це сприяє кращому проникненню. Тому з прогрітих овочів у воду переходить більше поживних речовин. Білки зернобобових. Зернобобові характеризуються високим вмістом білкових речовин. У горосі, квасолі кількість білків становить 20—23%. Основну масу становлять альбуміни і глобуліни. Крупи.містять від 6 до 16% білків, головним чином це глобуліни, проламіни і глютеліни. В бобових, крупах, борошні білки знаходяться у вигляді сухих гелів. Під час замочування круп, бобових, а також при замішуванні тіста білки набухають. Під час варіння зернобобових і випікання тіста білки денатурують і зсідаються, при цьому гелі ущільнюються і виділяється значна кількість вологи, яка в них міститься. Але рідина не виходить в навколишнє середовище, як при тепловій обробці м’яса або риби, а залишається в продуктах, оскільки вона зразу поглинається крохмалем на його клейсте- ризацію. 6.2. Зміни вуглеводів Вуглеводи є основною складовою частиною продуктів рослинного походження. В харчових продуктах містяться прості цукри (глюкоза, фруктоза), дисахариди (сахароза, лактоза та ін.), полісахариди (крохмаль, клітковина, пектинові речовини). Прості цукри містяться в ягодах і фруктах, сахароза — в буряку, моркві, лактоза — в молоці. Крохмалем багаті картопля, крупи і борошняні вироби, а клітковиною — всі рослинні продукти. В харчуванні людини вуглеводи відіграють роль джерела енергії. Клітковина сприяє кращому перетравленню, але при захворюванні шлунково-кишкового тракту вміст її в раціоні харчування обмежується. Крохмаль в органах травлення перетворюється в цукор (мальтозу і глюкозу) і засвоюється організмом. ЦУКОР Під час теплової обробки цукор може гідролізуватися, карамелізу- ватися, вступати в реакцію меланоідиноутворення. Під час нагрівання з водою цукри розчиняються. Гідралізуються дисахариди під дією ферментів і кислот з утворенням простих цукрів. Ферментативному гідролізу піддаються сахароза і мальтоза під час бродіння тіста і в початковій стадії його випікання. Сахароза під дією ферменту дріжджів — сахарази, а мальтоза під дією ферменту борошна — мальтази гідролізуються до моносахаридів. Кислотний гідроліз відбувається під час нагрівання дисахаридів з водою в присутності кислот. У таких технологічних процесах, як варіння плодів і ягід у розчині цукру різної концентрації (приготування компотів, фруктово-ягідних начинок, запікання яблук, приготування помадок для кондитерських виробів), відбувається кислотний гідроліз (інверсія) сахарози. Інверт- ний цукор, який утворюється, суттєво впливає на смак готових страв, оскільки ступінь солодкості одержаних простих цукрів вищий, ніж дисахаридів. Різні кислоти володіють різною гідролізуючою властивістю. Найбільша вона у щавлевої кислоти і значно менша у лимонній, яблучній, оцтовій. Карамелізація — це глибоке розщеплення цукрів під час нагрівання їх вище 100°С. При цьому від молекул цукрів відокремлюється молекула води, а ангідридні залишки, з’єднуючись один з одним, утворюють темнокольорові речовини. Під час карамелізації сахарози утворюється спочатку кармелан — речовина світло-жовтого кольору, розчинна у холодній воді. Потім утворюється кармелен — речовина коричневого кольору, теж розчинна у воді, і якщо ще довше нагрівати, то утвориться чорна, нерозчинна у воді речовина — кармелін. Продукти карамелізації використовують як харчові фарби при виготовленні компотів, солодких страв, соусів. Явищем карамелізації значною мірою обумовлене утворення рум’яної шкірочки під час смаження рослинних продуктів, випікання кондитерських виробів. У результаті реакції простих цукрів з азотовмісними речовинами (амінокислотами, амінами) утворюються сполуки — меланоїдини (від грецького кореня «мелано» — темні). Реакція меланощиноутворення має велике значення, її позитивна роль полягає в тому, що вона є причиною утворення апетитної рум’яної шкірочки на смажених, запечених і випечених виробах з м’яса, риби, сирниках, запіканках та ін. Побічні продукти цієї реакції беруть участь в утворенні смаку й аромату готових страв. Негативна роль реакції мелано’ідиноутворення полягає в тому, що зв’язуючи амінокислоти, вона знижує біологічну цінність білків і викликає небажане потемніння очищених овочів, фруктів і інших продуктів. Під час бродіння тіста глибокому розкладу піддаються моносахариди (глюкоза, фруктоза). Під дією ферментів дріжджів вони перетворюються в етиловий спирт і вуглекислий газ, який розпушує тісто, утворюючи пористу структуру. Крім того, під дією молочнокислих бактерій цукри в тісті перетворюються в молочну кислоту, яка затримує гнильні процеси і сприяє набуханню білків клейковини. 6.3. Зміни крохмалю Крохмалем багаті такі продукти, як картопля, кукурудза, бобові, крупи, борошно. Зерна крохмалю мають своєрідну, характерну для кожного продукту форму і величину. У більшості крохмалевмісних продуктів крохмальні зерна складаються із двох полісахаридів — амілози і амілопектину. Це високомоле- кулярні сполуки, які відрізняються величиною і будовою молекули. Молекули цих полісахаридів складаються із залишків глюкози, які з’єднані між собою в довгі ланцюжки. Чим довші ланцюжки амілози, тим вона гірше розчиняється. В молекулі амілози таких залишків у середньому близько 1000. В молекулі амінопектину залишків глюкози набагато більше. Крім цього, в молекулах амілози ланцюжки прямі, а в амінопектину більш розгалужені. Властивості цих полісахаридів різні. Амілоза може давати слабі концентровані розчини, з йодом дає синій колір, а амінопектин під час нагрівання з водою не розчиняється, а набухає, з йодом дає червоно- фіолетове забарвлення. В крохмальному зерні молекули цих полісахаридів розміщені шарами. При цьому верхні шари в основному складаються з амінопектину. Природний крохмаль практично не розчиняється у воді. Нагрівання крохмалю при наявності води викликає клейстериза- цію, тобто руйнування нативної структури крохмальних зерен. Процес цей проходить трьома стадіями. 1. Під час нагрівання суспензії до температури 50—55°С крохмальні зерна набухають, поглинаючи до 50% води від маси крохмалю, але зберігають форму і шарову будову. Порушення внутрішньої структури незначне. 2. При дальшому нагріванні (до температури 60—80°С) відбувається сильне пошкодження нативної структури крохмальних зерен. Зникає шарова будова, зерна збільшуються в об’ємі в декілька десятків разів і перетворюються в пухирці, наповнені розчином амілози і амінопектину, а в’язкість суспензії різко збільшується і вона перетворюється в клейстер. Тому цей процес називається клейстеризацією. Частина розчину переходить у навколишнє середовище. В результаті все більшого набухання крохмальних пухирців кількість води ззовні сильно зменшується, а клейстер стає більш в’язким. Для кожного виду крохмалю характерна своя температура клейсте- ризації, при якій більшість зерен у суспензії поглинає максимальну кількість води. 3. Нагрівання клейстеру вище 80°С надлишком води призводить до розпаду крохмальних зерен — пухирці лопають і в’язкість клейстеру знижується. Наявність у воді солей, цукрів та інших речовин впливає на температуру клейстеризації.Кухонна сіль навіть у дуже малих концентраціях підвищує температуру клейстеризації і зменшує набухання зерен. Цукри і спирти також підвищують температуру клейстеризації. В залежності від співвідношення крохмалю і води одержують клейстер у вигляді гелю або золю. Крохмальні золі різної в’язкості служать основою киселів рідкої і середньої консистенції (вміст крохмал
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-28; просмотров: 426; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.91.111 (0.02 с.) |

 Поліпептидні ланцюжки Водневі зв’язки
Поліпептидні ланцюжки Водневі зв’язки
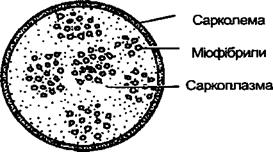 Рис. 52. Схема будови м’язового волокна
Рис. 52. Схема будови м’язового волокна
 Рис. 53. Будова м’язової тканини
Рис. 53. Будова м’язової тканини
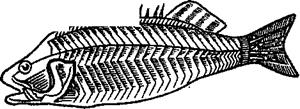



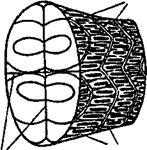 Септи (поперечні) Перемізій
Септи (поперечні) Перемізій