
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Рівняння Гіббса для адсорбції
Припустимо, що в поверхневому шарі рідини, площею F вміщується 1 моль розчиненої речовини. При переході малої кількості розчиненої речовини з об’єму у поверхневий шар, поверхневий натяг зменшується на До розбавленого розчину застосовують закон ідеальних газів. Зменшення вільної поверхневої енергії
і
У випадку ідеального розбавлення розчинів тиск пропорційний концентрації С. Тоді:
Рівняння (4.11) є основним рівнянням Гиббса для адсорбції. Так як спочатку надлишок розбавленої речовини був прийнятий за 1 моль, то Тоді:
Величину З рівняння Гиббса витікає, що при Таким чином, адсорбцію називають позитивною, якщо концентрація розчиненої речовини у поверхневому шарі вище, ніж в об’ємі, й негативною у протилежному випадку. Адсорбція завжди зменшується із збільшенням температури внаслідок теплового руху.
Фізична адсорбція
Сорбційні сили та процеси. Сорбція — це процес поглинання газів або пари твердими чи рідинними тілами. Природа сорбційних сил така ж, як і сил міжмолекулярної взаємодії. Адсорбція відбувається під дією некомпенсованої або міжатомної взаємодії в поверхневому шарі адсорбенту, який притягує молекули адсорбата із приповерхневої області. Адсорбція зменшує поверхневу енергію адсорбента і є початковою стадією процесу взаємодії між твердими речовинами та газом. Розрізняють хімічну і фізичну адсорбції (взаємодію). Фізична взаємодія визначається наступними ефектами: 1. Притягання між молекулою із постійним диполем та молекулою з індуційованим диполем (індукційний ефект);
2. Притягання між молекулами із постійними диполями (орієнтаційний ефект); 3. Притягання між молекулами із флюктуіруючим та індуцірованим диполем (дисперсійний ефект); 4. Відштовхування між ядрами молекул, що зближуються. При хімічній взаємодії розрізняють слідуючи види зв’язків, які забезпечують притягання молекул: ковалентну, металічну, іону. Рідина, яка поглинає газ, називається сорбентом (адсорбентом, абсорбентом). Рідина, що поглинається — сорбат (адсорбат, абсорбат). У випадку фізичної адсорбції між частинкою і поверхнею діють слабкі дальньодіючі сили; енергія зв’язку мала: приблизно 0,1...0,5 еВ.
|
|||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 211; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.20.205.228 (0.006 с.) |
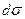 , а вільна енергія поверхні зменшується на
, а вільна енергія поверхні зменшується на  . Це зменшення вільної енергії еквівалентно роботі вилучення з розчину такої самої кількості розчинених речовин. Якщо 1 моль розчиненої речовини знаходиться в об’ємі V, і dP – різниця тисків розчину до і після вилучення малої кількості розчинених речовин, то робота вилучення
. Це зменшення вільної енергії еквівалентно роботі вилучення з розчину такої самої кількості розчинених речовин. Якщо 1 моль розчиненої речовини знаходиться в об’ємі V, і dP – різниця тисків розчину до і після вилучення малої кількості розчинених речовин, то робота вилучення 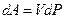 , тоді
, тоді 
 (4.9)
(4.9) (4.10)
(4.10) (4.11)
(4.11) представляє собою адсорбцію в молях на одиницю площі (моль/см2).
представляє собою адсорбцію в молях на одиницю площі (моль/см2). (4.12)
(4.12)
 називають поверхневою активністю речовини, яку вимірюють в гиббсах; 1Гиббс=
називають поверхневою активністю речовини, яку вимірюють в гиббсах; 1Гиббс=  .
. , тобто при зменшені поверхневої енергії
, тобто при зменшені поверхневої енергії  зі збільшенням концентрації С адсорбція позитивна (Г>0), й розчинена речовина вважається поверхнево активною
зі збільшенням концентрації С адсорбція позитивна (Г>0), й розчинена речовина вважається поверхнево активною  . У протилежному випадку має місце зворотна нерівність і розчинену речовину називають інактивною.
. У протилежному випадку має місце зворотна нерівність і розчинену речовину називають інактивною.


