
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Розділ 5. Змочування твердих тіл рідиною
Основні закони капілярності
Сила поверхневого натягу в простих випадках в залежності від різниці тиску по обидві сторони поверхні з кривизною
де R1 і R2 – головні радіуси кривизни поверхні в даній точці. За допомогою цієї фундаментальної формули можна знаходити надмірний тиск для різних випадків.
Змочування і розтікання Змочування – є особливим видом взаємодії рідини з твердим тілом. Воно відбувається раніше розчинення і дифузії. Виявляється на практиці або у формі розтікання краплі рідини по поверхні твердого тіла, або навпаки у формі відтоку (згортання). Нехай крапля рідини поміщена на ідеально гладку однорідну тверду поверхню, крапля має форму тіла обертання. На рис.5.8 точка А є точка торкання тіла обертання. Дотична АВ до поверхні рідини утворює з поверхнею кут θ, який називається крайовим кутом. Крайовий кут завжди відлічується від дотичної убік рідини. Вершина крайового кута знаходиться на лінії змочування – лінії, уздовж якої стикаються всі фази, що беруть участь в змочуванні (тверде тіло – рідина – газ). Необхідно розрізняти рівноважні і нерівноважні крайові кути. Рівноважний крайовий кут залежить тільки від термодинамічних властивостей системи, а саме від поверхневого натягу на межах розділу фаз, що беруть участь в змочуванні. Крайові кути, які виміряні при відхиленні системи від стану термодинамічної рівноваги називаються нерівноважними.
Рис. 5.8. Розтікання краплі по поверхні твердого тіла: 1 – початковий (нерівноважний) стан; 2 –рівноважний стан.
Величина рівноважного крайового кута визначається співвідношенням сил притягання рідини до твердого тіла і сил взаємного притягання між частинками самої рідини. Рівноважний крайовий кут представляє одну з найважливіших характеристик змочування. Основними енергетичними характеристиками поверхні твердих тіл і рідин служать питома вільна поверхнева енергія ƒ і поверхневий натяг σ. Питома вільна поверхнева енергія поверхні розділу двох фаз α і β рівна
Різниця Поверхневий натяг σ визначається як робота зворотного ізотермічного процесу утворення одиниці площі поверхні розділу фаз, за умови, що термодинамічні параметри стану системи (Т і Р, хімічні потенціали
де V – об`єм багатокомпонентної системи; nі – число молів і -го компоненту. Питома вільна поверхнева енергія fαβ і поверхневий натяг
де Для однокомпонентних систем
і при Г = 0 По Гіббсу σ, що входить в рівняння, є поверхневий натяг і воно пов'язано з надмірною вільною поверхневою енергією ƒ виразом.
де Гi, µi – адсорбція і хімічний потенціал i -го (компоненту за умови, що поверхня, яка розділяє вибрана так, що адсорбція першого компоненту рівна нулю. Величина σ визначає роботу утворення поверхні, але не її розтягування. Лише для рідини процеси утворення нової поверхні і розтягування еквівалентні. Тому величина σ, хоча і називається поверхневим натягом, для твердого тіла не є механічним натягом (напругою) його поверхні. Останнє через малу рухливість атомів твердого тіла може приводити, наприклад, до зміни міжатомних відстаней в поверхневому шарі, зміни густини поверхневих частинок тіла. Таким чином, величина поверхневого натягу σ, що входить в рівняння, є робота зворотного утворення одиниці площі даної поверхні.
|
||||||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 181; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.121.242 (0.008 с.) |
 виражається формулою Лапласа
виражається формулою Лапласа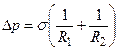 5.1
5.1
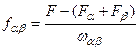 (5.8)
(5.8) – енергія Гельмгольца фази α; F (β) – енергія Гельмгольца фази β; F – загальна енергія Гельмгольца двофазної системи, що має поверхню розділу фаз площею
– енергія Гельмгольца фази α; F (β) – енергія Гельмгольца фази β; F – загальна енергія Гельмгольца двофазної системи, що має поверхню розділу фаз площею  ;
; 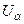 , Tα, Sα – це внутрішня енергія, температура і ентропія фази α.
, Tα, Sα – це внутрішня енергія, температура і ентропія фази α. F – (Fα + Fβ)
F – (Fα + Fβ)  є загальною вільною енергією поверхневого шару Fпш.
є загальною вільною енергією поверхневого шару Fпш.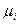 компонентів) не змінюються. Таким чином
компонентів) не змінюються. Таким чином (5.9)
(5.9) зв'язані співвідношенням
зв'язані співвідношенням (5.10)
(5.10) – хімічний потенціал компоненту; Г і – адсорбція цього компоненту на поверхні розділу фаз (надлишок концентрації компоненту i в поверхневому шарі в порівнянні з його концентрацією в об'ємі).
– хімічний потенціал компоненту; Г і – адсорбція цього компоненту на поверхні розділу фаз (надлишок концентрації компоненту i в поверхневому шарі в порівнянні з його концентрацією в об'ємі). (5.11)
(5.11) (5.12)
(5.12) (5.13)
(5.13)


