
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 4. Влияние катализаторов на скорость реакцииСодержание книги
Поиск на нашем сайте а) Гетерогенный катализ. В три пробирки налить по 1 мл раствора перекиси водорода и прибавить одновременно: в одну – щепотку двуокиси марганца, в другую – такое же количество окиси железа, в третью – двуокиси кремния. Наблюдать разложение перекиси водорода с выделением кислорода (проба тлеющей лучиной). Одинаково ли быстро протекает процесс? Напишите уравнения реакций. б) Гомогенный катализ. Раствор роданида железа, оставшийся после опыта 3, разбавить двойным объемом воды и разлить поровну в три пробирки. Отмерить цилиндром 5 мл раствора тиосульфата натрия, влить в первую пробирку, включив в момент вливания секундомер. Отметить время от момента вливания до обесцвечивания раствора. Реакция протекает согласно уравнению 2Fe(CNS)3 + 2Na2S2O3 = 2Fe(CNS)2 + 2 NaCNS + Na2S4O6. Все вещества, образующиеся в результате реакции, бесцветны. Во вторую пробирку добавить 5 капель раствора сульфата меди и влить 5 мл раствора тиосульфата натрия. Определить по секундомеру время от момента сливания растворов до обесцвечивания. Какую роль играют ионы Сu2+? В третью пробирку влить 15 капель сульфата меди и проделать аналогичный опыт. Как влияет количество катализаторов на скорость катализируемой гомогенной реакции?
КОНТРОЛЬНЫЕ ВОПРОСЫ 1 Что называется скоростью химической реакции? В каких единицах она измеряется? 2 В чем различие реакций, происходящих в гомогенных системах и гетерогенных системах? 3 Почему при повышении концентрации реагирующих веществ и температуры скорость реакции увеличивается? 4 Какое состояние реакционной химической системы называется химическим равновесием? Почему химическое равновесие называют подвижным (динамическим)? 5 Какие методы ускорения течения реакций существуют? Что называется катализом? 6 Какова роль катализатора в химической реакции? Влияет ли катализатор на состояние химического равновесия? ГИДРОЛИЗ СОЛЕЙ Обменная реакция веществ с водой, при которой происходит изменение концентрации водородных ионов, т.е. рН раствора, называется гидролизом. Взаимодействие с водой протекает часто ступенчато, с различной глубиной, с образованием комплексов в зависимости от условий и природы реагирующих веществ. Гидролизу подвергаются разные вещества: соли, галогенангидриды, карбиды, углеводы, белки, жиры и т.д. Осахаривание крахмала, гидролиз древесины, получение мыла и другие важные производства основаны на гидролизе. Весьма важное значение имеет гидролиз солей. Он протекает только в тех случаях, когда из ионов соли и ионов воды может образовываться хотя бы одно слабодиссоциирующее или очень мало растворимое вещество. Образование такого вещества сопровождается связыванием одного из ионов воды, смещением равновесия диссоциации воды и изменением рН раствора. В зависимости от характера солей различают три основных вида их гидролиза: 1) гидролиз солей; образованных слабым основание и сильной кислотой: NH4, CuCI2, AI2(SO4)3, SnCI2 и др. гидролиз таких солей идет по катиону (рН<7):
Если катион многозарядный, то в результате гидролиза образуется чаще всего не слабое основание, а основная соль. Гидролиз идет ступенчато:
В растворе накапливаются ионы H+ , которые препятствуют прохождению гидролиза по II и тем более по III ступени; 2) гидролиз солей, образованных слабой кислотой и сильным основанием: Na2CO3, KCN, Na2SO3, KNO2 и др. (рН>7):
Соли, образованные сильным основанием и слабой многоосновной кислотой, гидролизуется ступенчато с образованием кислых солей.
Гидролиз идет, в основном, только по I ступени, т.к. появившиеся гидроксид-ионы препятствуют прохождению гидролиза по II ступени, т.е. смещают равновесие второй реакции влево; 3) гидролиз солей, образованных слабым основанием и слабой кислотой. Соли этого типа легче других подвергается гидролизу, т.к. одновременно связываются ионы Н+ и ОН-. В зависимости от зарядности катиона и аниона при гидролизе таких солей могут образовываться слабое основание и слабая кислота, слабая кислота и основная соль, слабое основание и кислая соль.
При гидролизе солей, образованных слабым основанием и слабой кислотой, рН раствора может быть равен 7, если образуется кислота и основание одинаковые по силе. Некоторые из солей, образованные очень слабым основанием и очень сильной кислотой, подвергаются необратимому гидролизу. Например, полному гидролизу подвергаются сульфиды и карбонаты трехзарядных катионов (AI3+, Fe3+, Cr3+). Поскольку гидролиз принадлежит к числу обратимых процессов, то положение его равновесия может быть смещено в ту или иную сторону изменением концентрации веществ, участвующих в реакции, а также температуры раствора. Так, разбавляя раствор, т.е. увеличивая в нем относительную концентрацию воды, на основании принципа Ле Шателье можно увеличить степень гидролиза. Наоборот, приливая кислоту в растворы, имеющие кислую реакцию, или щелочь в растворы с щелочной реакцией, можно получить степень гидролиза. С повышением температуры раствора степень гидролиза соли увеличивается. Таким образом, для того, чтобы соли не повергались гидролизу, их необходимо хранить при более низкой температуре и в более высокой концентрации. ЛАБОРАТОРНАЯ РАБОТА
|
||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 418; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.134.140 (0.009 с.) |

 NH4NO3 + H2O NH4OH + HNO3
NH4NO3 + H2O NH4OH + HNO3 NH4+ + NO3- + H-OH NH4OH + H+ + NO3-
NH4+ + NO3- + H-OH NH4OH + H+ + NO3- NH4+ + H-OH NH4OH + H+
NH4+ + H-OH NH4OH + H+ AICI3 + H-OH AIOHCI2 + HCI
AICI3 + H-OH AIOHCI2 + HCI AI3+ + H-OH AIOH2+ + H+ (I ступень)
AI3+ + H-OH AIOH2+ + H+ (I ступень)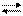 AIOH2+ + H-OH AI(OH)2+ + H+ (II ступень)
AIOH2+ + H-OH AI(OH)2+ + H+ (II ступень) AI(OH)2+ + H2O AI(OH)3 + H+ (III ступень)
AI(OH)2+ + H2O AI(OH)3 + H+ (III ступень) KCN + H-OH HCN + KOH
KCN + H-OH HCN + KOH K+ + CN- + H-OH HCN + K+ + OH-
K+ + CN- + H-OH HCN + K+ + OH- CN- + H-OH HCN + OH-
CN- + H-OH HCN + OH- Na2CO3 + H-OH NaHCO3 + NaOH
Na2CO3 + H-OH NaHCO3 + NaOH CO32- + H-OH HCO3- + OH- (I ступень)
CO32- + H-OH HCO3- + OH- (I ступень)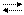 HCO3- + H-OH H2CO3 + OH- (II ступень)
HCO3- + H-OH H2CO3 + OH- (II ступень)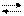 (NH4)2S + H2O NH4OH + NH4HS
(NH4)2S + H2O NH4OH + NH4HS 2NH4+ + S2- + H-OH NH4OH + NH4+ + HS-
2NH4+ + S2- + H-OH NH4OH + NH4+ + HS-


