Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
II. Аминокислоты с полярными (гидрофильными) незаряженнымиСодержание книги
Поиск на нашем сайте
радикалами (7): 1. Глицин (Гли): Не содержит радикала (R=H).
NH2-CH2-COOH
НО -содержащие аминокислоты:
2. Серин (Сер): 3. Треонин (Тре): 4. Тирозин (Тир):
NH2-CH-COOH NH2-CH-COOH ½ ½ CH2 CH-CH3 ½ ½ OH OH
SH -содержащие аминокислоты:
5. NH2-CH-COOH ½ CH2 ½ SH цистеин (Цис)
Cледует отметить, что спиртовые и фенольные ОН-группы и тиоловая SH-группа проявляют в воде очень слабую кислотность по сравнению с карбоксильной –СООН-группой, поэтому их кислотными свойствами можно пренебречь.
Амиды аминокислот, содержащие группу –С=О: ½ NH2
6. Аспарагин (Асн): 7. Глутамин (Глн):
NH2-СH-СOOH NH2-CH-COOH ½ ½ CH2 (CH2)2 ½ ½ C=O C=O ½ ½ NH2 NH2
Амидная группа проявляет, в отличие от аминов, очень слабые основные свойства в силу того, что неподеленная электронная пара азота включена в р,p - сопряжение.
III. Аминокислоты с полярными (гидрофильными) положительно заряженными радикалами (3): 1. Лизин (Лиз):
: NH2-CH-COOH +NH3-CH-COO¾ + ¾OH ½ +H2O ½ (CH2)4 ® (CH2)4 ½ ½ : NH2 +NH3
2. Аргинин (Арг):
NH2-CH-COOH + H2O +NH3-CH-COO- + -OH ½ ® ½ (CH2)3 (CH2)3 ½ ½ : NH NH ½ C=NH C =+NH2
: NH2 NH2 В этом случае протонируется атом азота при двойной связи, так как его неподеленная электронная пара не включена в сопряжение.
3. Гистидин (Гис):
+ H2O + -OH ®
IV. Аминокислоты с полярными (гидрофильными) отрицательно заряженными радикалами (2): 1. Аспарагиновая кислота (Асп): NH2-CH-COOH +NH3-CH-COO¾ + H+ ½ ® ½ CH2 CH2 ½ ½ COOH COO¾
2. Глутаминовая кислота (Глу):
NH2-CH-COOH +NH3-CH-COO¾ + H+ ½ ® ½ (CH2)2 (CH2)2 ½ ½ COOH COO¾ Во всех - a-аминокислотах, за исключением глицина, a - атом углерода связан с четырьмя различными замещающими группами и, следовательно, является асимметрическим, или хиральным. Такие молекулы встречаются в двух стереоизомерных формах и проявляют оптическую активность. Все аминокислоты, входящие в состав молекул белков, являются L-стереоизомерами. Химические свойства аминокислот I. Общие (неспецифические) свойства. 1. Все свойства карбоновых кислот (см. тему № 4). 2. Все свойства аминов. Свойства аминов
Аминами называются органические производные аммиака, в которых один, два или три атома водорода замещены на углеводородные радикалы (первичные, вторичные и третичные амины). Все протеиногенные a-аминокислоты – за исключением пролина – содержат первичную аминогруппу. а) Основные свойства (способность образовывать соли с кислотами) -: обусловлены наличием неподеленной электронной пары на внешнем электронном уровне атома азота: + - (СH3)3N + HCl ® [ (CH3)3NH]Cl триметиламин триметиламмоний хлорид б) Нуклеофильные свойства проявляются в реакциях: - алкилирования аминов (получение аминов из аммиака и алкилгалогенидов):
·· d+ d- + ¾ NH3
этиламмоний -NH4Cl хлорид
Этиламин
Дальнейшее алкилирование приведет ко вторичному амину, затем к третичному амину, который можно превратить в соль четвертичного аммониевого основания (реакция Гофмана).
- ацилирования аминов, например:
½ ½ Cl NH2
Эти реакции встречаются в организме.
Переносчиком ацетильной группы на нуклеофильные субстраты in vivo служит ацетилкофермент А.
½ SKoA
мономер хитина N-ацетилглюкозамин
- взаимодействия аминов с альдегидами и кетонами (обсуждались в теме № 3).
в) Реакция с азотистой кислотой – качественная реакция на класс аминов.
первичный амин + -
вторичный амин -H2O N–нитрозо- диэтиламин (желтый раствор) Третичные амины с азотистой кислотой не реагируют. Первичные ароматические амины дают очень реакционноспособные соли диазония (реакция диазотирования), которые дальше вступают в различные превращения (в том числе реакция азосочетания, например, с b-нафтолом).
3. Амфотерность – способность проявлять как кислотные:
NH 2 – R – COOH + HCI == [ N+H3 – R – COOH] CI
так и основные свойства: NH 2 – R – COOH + NaOH === NH 2 – R – COONa + H2O Амфотерность аминокислот проявляется и внутримолекулярно – в водном растворе все аминокислоты образуют внутренние соли:
NH 2 – R – COOH === + NH 3 – R – COO- II. Специфические свойства обусловлены взаимным влиянием двух функциональных групп.a -, b - и g- Аминокислоты при нагревании вступают в реакции, аналогичные реакциям соответствующих оксикислот. 1. a - Аминокислоты при нагревании образуют дикетопиперазины. Реакция идет межмолекулярно через промежуточное образование дипептидов: дипептидов:
Дикетопиперазин
2. b-Аминокислоты образуют непредельные кислоты: b a t°
½ ½ -NH3 ½ NH2 OH OH
3. g- и d-Аминокислоты образуют циклические амиды, называемые g- и d - лактамами. Для них характерно таутомерное превращение (лактам ® лактим): g b a t° b a
½ ½ -H2O g NH 2 OH
лактам
®
лактим
|
|||||||||||||
|
Последнее изменение этой страницы: 2016-09-19; просмотров: 355; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.54.100 (0.006 с.) |


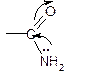 Основностью этой группы тоже можно пренебречь.
Основностью этой группы тоже можно пренебречь. .. ½
.. ½ ½ ½
½ ½
 ˉ
ˉ

 NH3 + CH3 - CH2®Cl [ C2H5NH3]Cl
NH3 + CH3 - CH2®Cl [ C2H5NH3]Cl C2H5NH2
C2H5NH2 СH3-CH2-NH2 + CH3-C=O CH3-C=O + HCl
СH3-CH2-NH2 + CH3-C=O CH3-C=O + HCl

 + СН3-С=О + KoA-SH
+ СН3-С=О + KoA-SH СH3-CH2-NH2 + H-O-N=O N2 + H2O + C2H5OH
СH3-CH2-NH2 + H-O-N=O N2 + H2O + C2H5OH
 (С2H5)2NH + HONO [ (C2H5)2NH2]ONO (C2H5)2N-N=O
(С2H5)2NH + HONO [ (C2H5)2NH2]ONO (C2H5)2N-N=O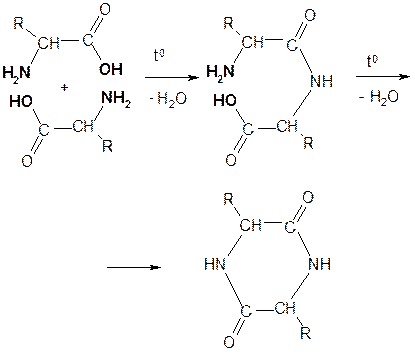
 R-CH-CH2-CH2-C=O ®
R-CH-CH2-CH2-C=O ®