Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Цикло-цепные таутомеры моносахаридовСодержание книги
Поиск на нашем сайте
По мере изучения свойств моносахаридов выяснилось, что открытые (цепные) формулы не описывают полностью химическое поведение сахаров. Например, несмотря на наличие в молекуле глюкозы пяти ОН– групп, только одна из них вступает в реакцию со спиртами в присутствии сухого хлористого водорода с образованием гликозидов. Для объяснения подобных противоречий было высказано предположение (1870 г. А. Колли; 1883 г. Б. Толленс), что истинное строение моноз не описывается лишь открытой (цепной) формулой. Моносахариды образуют в водном растворе таутомерные смеси открытых и циклических форм. В основе их образования лежит внутримолекулярная реакция нуклеофильного присоединения спиртовых групп к альдегидной или кетонной группе:
H+ полуацетальный,
полуацеталь
Такой реакции способствует клешневидноя конформация углеродной цепи углевода:
фуран пиран Пример. Изобразите цикло-цепные таутомеры D-рибозы по Фишеру и Хеуорсу.
Пиранозные формы рибозы образуются путем взаимодействия гидроксильной группы при С5 рибозы с альдегидной группой:
Образование циклической полуацетальной формы приводит к появлению нового хирального центра у первого атома углерода, в результате при такой циклизации получаются два диастереомера, которые отличаются конфигурацией только С1 атома и называются a - и b-аномерами. В a- форме полуацетальный (гликозидный) гидроксил справа от углеродной цепи молекулы; он расположен с той же стороны, что и гидроксил, определяющий принадлежность углевода к D-ряду. В b-форме эта группа с противоположной стороны, слева.
Аналогично, только с участием гидроксила при атоме С4, происходит образование фуранозных форм D-рибозы:
b,D–рибофураноза D–рибоза a,D–рибофураноза
Перспективные формулы Хеуорса
Недостатком проекционных формул Фишера является их несоответствие истинной геометрии молекулы. Поэтому для циклических таутомеров были введены формулы Хеуорса, которые строятся по следующим правилам: 1. Написать формулу Фишера для цепной формы углевода. 2. Написать формулу для циклической таутомерной формы и пронумеровать атомы углерода в ней.
a,D–рибопираноза D–рибоза a,D–рибофураноза (циклическая форма) (открытая форма) (циклическая форма)
3.
Нарисовать необходимый цикл (5- или 6-членный) с атомом кислорода в правом верхнем углу и пронумеровать атомы углерода, связанные с кислородом, по часовой стрелке (см. рисунок) 4. Заместители, стоящие справа от цепи в проекции Фишера, располагают снизу от плоскости цикла, а стоящие слева – сверху.
Исключение составляют заместители у того углеродного атома, при котором происходит циклизация. У такого атома углерода необходимо делать циклическую перестановку заместителей (см. рисунок). a,D –рибопираноза (по Хеуорсу) a, D–рибофураноза (по Хеуорсу)
Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
a,D-рибопираноза a,D-рибофураноза 18 % 16,5 %
D-рибоза 8,5 %
b,D-рибопираноза b,D-рибофураноза 51 % 6 %
Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации. Мутаротация объясняется тем, что кристаллический циклический таутомер, растворяясь в воде, переходит постепенно через открытую форму во все другие таутомерные формы.При этом угол вращения плоскости поляризованного света будет меняться во времени до достижения равновесия между всеми цикло-цепными таутомерами. Это изменение во времени угла вращения плоскости поляризованного света в свежеприготовленных растворах сахаров называется мутаротацией. Конформации моносахаридов Углеводы в циклической форме существуют в виде неплоских конформаций. Так, для пиранозных форм наиболее энергетически выгодной является конформация «кресла».
В равновесной смеси таутомеров D-рибозы преобладает b,D-рибопираноза (51 %), так как этот таутомер существует в конформации кресла с экваториальным расположением большинства гидроксильных групп, что обеспечивает стабильность этой формы:
b, D–рибопираноза Только одна ОН группа в третьем положении кольца занимает аксиальное положение в этой конформации.
В конформации a,D-рибопиранозы таких групп две – в первом и третьем положениях: a, D- рибопираноза
Эта форма менее стабильна; ее содержание составляет всего 18 %. Пятичленные циклы и ациклическая форма содержатся в смеси в меньшей концентрации. Эпимеризация
Под действием щелочей некоторые моносахариды, отличающиеся конфигурацией одного хирального центра, могут превращаться друг в друга через промежуточное образование общей ендиольной формы: D-глюкоза ендиол D-манноза
(63,5%) (2,5%) D-фруктоза (31%) Стереоизомеры, отличающиеся конфигурацией одного хирального центра, называются эпимерами, а процесс их взаимного превращения друг в друга в щелочной среде – эпимеризацией.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-09-19; просмотров: 3312; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.128.79.124 (0.008 с.) |


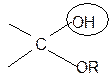





 + HOR или гликозидный
+ HOR или гликозидный гидроксил
гидроксил
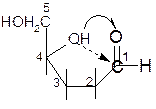

 В 1925–30 гг. У. Хеуорс экспериментально определил размер возможных циклических таутомеров. Он предложил называть пятичленные циклы углеводов фуранозами, а шестичленные – пиранозами как производные фурана и пирана, соответственно:
В 1925–30 гг. У. Хеуорс экспериментально определил размер возможных циклических таутомеров. Он предложил называть пятичленные циклы углеводов фуранозами, а шестичленные – пиранозами как производные фурана и пирана, соответственно:




 b,D–рибопираноза D–рибоза a,D–рибопираноза
b,D–рибопираноза D–рибоза a,D–рибопираноза