Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нанесение вакуумных ионно-плазменных покрытийСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
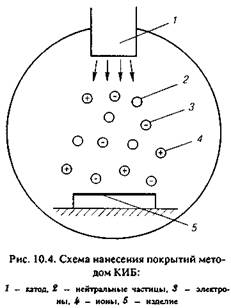
Вакуумная ионно-плазменная технология нанесения покрытий, получившая широкое распространение в различных отраслях машиностроения, главным образом для повышения износостойкости изделий, может с успехом применяться и для деко-рирования отливок. Наиболее перспективным считается электродуговой метод, получивший название конденсация ионной бомбардировкой (КИБ). В вакуумной камере размещен катод (рис. 10.4). Между корпусом камеры и катодом возникает электрическая дуга. Из катодного пятна вылетают ионы, электроны и нейтральные частицы, которые направленным потоком летят к изделию, расположенному внутри камеры. Вначале частицы как бы разрыхляют поверхностный слой изделия, эффективно очищая его и нагревая до 300—500 ° С. Далее происходит насыщение поверхностного слоя ионами того материала, из которого изготовлен катод. Если в камеру вводят различные газы (например, азот- или утлеродсодержащие) на поверхности изделия формируются нитридные или карбидные покрытия. Широкое распространение получили покрытия из нитрида титана, которые удачно имитируют позолоту. Причем, регулируя параметры процесса, можно добиться полного сходства с золотом различных проб. Покрытия из нитрида титана наносят не только на металлы, но и на стекло, и на керамику. Такие покрытия отличаются прочным сцеплением с материалом изделия и высокой износостойкостью. При нанесении покрытий методом КИБ предъявляются очень жесткие требования к качеству поверхности изделий. На поверхности не должно быть посторонних загрязнений (ржавчины, масла, других неметаллических материалов). Особые трудности возникают при нанесении покрытий на отливки, на поверхности которых есть различные дефекты (поры, шлаковые включения, окисленные трещины). В ряде случаев требуется дополнительная подготовка поверхности. Если в состав материала изделия входят легкоиспаряемые элементы (например, цинк в латуни), то перед ионной бомбардировкой на изделие наносят гальваническим способом подслой никеля.
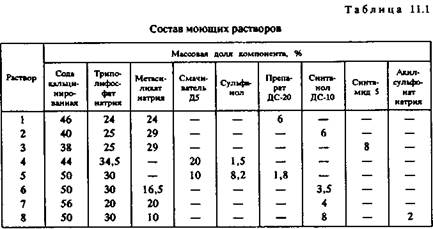
Глава 11 РЕСТАВРАЦИЯ Реставрация (отлат. restauratio — восстановление) охватывает все виды работ, направленные как на сохранение произведения искусства, так и на максимально возможное выявление его первоначального облика. Художественные произведения из металла с течением времени претерпевают различные изменения. В силу различных обстоятельств меняется внешний облик, нарушается сплошность изделий, утрачиваются отдельные элементы. В результате взаимодействия с окружающей средой резко ухудшается качество поверхности, которая в значительной степени определяет эстетическую ценность произведения искусства. Воссоздать первоначальный облик художественного произведения — это ответственная и черезвычайно сложная задача. Кроме художников и искусствоведов в этой работе большое участие принимают специалисты-материаловеды. Реставрация литых изделий имеет некоторые специфические особенности. Известно, что поверхностный слой отливки отличается по своим свойствам и структуре от основного металла из-за взаимодействия с материалом формы. Заделка литейных и других дефектов, появившихся на изделии с течением времени, также требует специального подхода. Реставрационные работы начинаются с очистки изделия. Очистка производится различными органическими и неорганическими материалами. При этом необходимо, чтобы удалялись только инородные наслоения и не происходило никаких изменений с основным металлом. Реставрация, кроме того, может включать воссоздание недостающих элементов и соединение их с оставшимися частями. Завершающим этапом реставрации является консервация изделия. РАЗРУШЕНИЕ МЕТАЛЛОВ Черные металлы. Чугун и сталь активно взаимодействуют с кислородом, влагой и агрессивными газами воздуха, с солями, имеющимися в морской воде и почве. На поверхности образуется химически устойчивая пленка оксидов, гидроксидов, силикатов, карбонатов, хлоридов, сульфидов. Поверхность предметов, обнаруженных при археологических раскопках, содержит и соли кальция. Толщина пленки зависит от условий образования и колеблется от долей микрона до миллиметров, а предметы, которые находят при раскопках, могут вообще не иметь металлического ядра и полностью состоят из продуктов коррозии. Коррозия развивается со временем даже при относительно благоприятных условиях хранения. Многие соли гигроскопичны, а рыхлые оксидные и гидрооксидные образования сорбируют влагу из воздуха. Наличие рыхлых слоев коррозии недопустимо при консервации музейных экспонатов из чугуна и стали. Поэтому удаление продуктов коррозии обязательно при реставрации. Медь и ее сплавы. Они легко окисляются на воздухе кислородом, соединениями серы, оксидами азота. Искусственные и естественные пленки на поверхности изделий — патина — эффективно предохраняют изделие от дальнейшего развития коррозии. При окислении на поверхности медных изделий сначала возникает налет, содержащий сульфид, оксид меди и сажу. Под действием серной кислоты и в результате окисления сульфида появляется сульфат меди. В результате гидролиза сульфата меди образуется однородный, прочно связанный с поверхностью изделия основной сульфат меди, близкий по составу к CuSO4 • Cu(OH)2. Патина не только предохраняет изделие от коррозии, но и придает ему определенную художественную ценность. Олово и свинец. Эти металлы практически не поддаются воздействию воздуха и влаги. Они стойки к воздействию многих кислот и оснований. Очень древние изделия, извлеченные из воды и земли при археологических исследованиях, имеют более прочную поверхностную пленку, чем изделия, которые хранятся столетиями на воздухе. На изделиях из свинца, разрушенных коррозией, чаще всего наблюдаются образования карбоната свинца с включениями оксида и хлорида. Возможно появление сульфида свинца в виде черно-серых мелкокристаллических образований при воздействии сероводорода. Известное в живописи потемнение свинцовых белил также обусловлено' образованием сульфида свинца. На старинных весах из свинца налет сульфида создает сероватую патину, которая обычно не требует удаления. Серебро. Серебро при комнатной температуре во влажном чистом воздухе адсорбирует кислород. При этом образуется пленка оксида толщиной до 1,2 нм. Воздействие галогенов при комнатной температуре приводит к образованию на серебре защитной пленки галогенида. Из-за диффузии ионов серебра от металла к поверхности возможен рост пленки гало-генидов. ОБЕЗЖИРИВАНИЕ Бронзовая скульптура, стоящая на открытом воздухе, часто бывает покрыта различными восковыми составами. Кроме того, поверхность металла нередко загрязнена жировыми и смолистыми веществами. Их удаляют органическими растворителями или специально подобранными водными обезжиривающими составами. Органические растворители делят на две группы — горючие и негорючие. К первой относятся ацетон, керосин, ксилол, толуол, эфиры, уайт-спирит; ко второй — хлорированные и фторированные углеводороды (четыреххлористый углерод, трихлорэтилен, тетрахлорэтилен, хлороформ, хладон-113). Растворяющую способность различных растворителей по отношению к маслам (в порядке убывания) характеризует следующий ряд: хладон-113 (4,45) -* трихлорэтан (3,10) •* ксилол (2,20) -• тетрахлорэтилен (1,70) •* бензин (1,30) -> уайт-спирит (0,90) -• -» керосин (0,65). Токсичность и пожароопасное» являются серьезными недостатками большинства органических растворителей. Обезжиривание органическими растворителями не всегда обеспечивает полное удаление жировых загрязнений. В частности, в углублениях микрорельефа может оставаться нерасгворившаяся жировая пленка. Для удаления этих остатков, а также загрязнений, не растворяемых органическими растворителями, применяют щелочные растворы, которые подогревают. Продолжительность обработки при температуре раствора 50—60 ° С составляет от 5 до 30 мин. Повышение температуры до 100° С сокращает время обработки до 3—10 мин. Время обработки зависит от степени загрязненности и профиля поверхности. Содержание щелочи в водном растворе составляет 10—20 г/л. Более эффективное обезжиривание изделий из медных сплавов обеспечивает электрохимическая обработка. Примерный состав электролита (на 1 л воды): едкий натр (NaOH) — 15—25 г; углекислый натрий (NajCOs) — 15 г; тринатрийфосфат (Na3PC>4 • 12Н2О) — 15 г; жидкое стекло (Na2SiO3) — Зг. Изделие крепят на катоде, анодом служит лист нержавеющей стали. Поверхности анода и катода должны быть примерно равными по площади. Примерный режим электрохимического обезжиривания: напряжение 6—9 В, плотность тока 3—10 А/дм2. Время обработки 3—5 мин, из них 2—4 мин на катоде и 0,5—1 мин на аноде. Переключение с катода на анод производится для удаления водорода из металла. Щелочные растворы для обезжиривания изделий из черных металлов имеют несколько иной состав: едкие щелочи (NaOH, КОН) — 5—15 г/л; тринатрийфосфат (Na3PO4 • 12Н2О) — 15—35 г/л; углекислый натрий (Ыа2СОз) — 15—35 г/л; эмульгатор — 3—10 г/л. В качестве эмульгаторов рекомендуются синтанолы и сульфанолы. Обезжиривание меди и ее сплавов производят в холодном растворе, а стали — в нагретом до 90—45 °С. Кроме того, обезжиривание стали ведут при высокой плотности тока (20—100 А/дм2). Активным компонентом водных обезжиривающих составов является сода, которая обеспечивает щелочность среды и оказывает омыляющее действие на растительные и животные жиры. Эффективно очистить поверхность от масел и красок можно в водных растворах синтетических моющих средств (табл. 11.1). Их вводят в горячую воду в количестве 10—20 г/л.
Высокую эффективность моющих растворов обеспечивают поверхностно-активные вещества (ПАВ) и смачиватели. В растворах для обезжиривания металлов используют анионоактивные (акилсульфо-нат, сульфонолы НП-3, НП-1, ДС-РАС) и неионогенные (синтанол ДО 10, синтамид-5, препараты ОП, контакт Петрова) ПАВ. Содержание ПАВ в обезжиривающих растворах обычно составляет 3—5 г/л, но в некоторых случаях может быть и ниже. Золотые изделия обезжиривают в кипящем 10—20 %-ном растворе каустика. Золотые изделия, имеющие паянные оловянистыми припоями соединения, обезжиривают в растворе, содержащим 1 л азотной кислоты, 1 л серной кислоты и 5—10 г/л хлористого натрия. Обработку проводят при температуре 15—20 ° С в течение 5—10 с. Изделия из серебра сначала обезжиривают в органическом растворе (четыреххлористом углероде или бензине) в течение 3—20 мин. Затем для полного удаления жировой пленки изделие подвергают электрохимической обработке в электролите следующего состава: едкий натр — 20—30 г/л; кальцинированная сода — 20—30 г/л; тринатрийфосфат — 50—60 г/л; жидкое стекло — 5—10 г/л. Рабочая температура 70—80°С. Плотность тока 3—10 А/дм2, продолжительность обработки от 2 до 15 мин. ОЧИСТКА Очистка меди и медных сплавов. Изделия из меди и медных сплавов можно очищать в 30%-ном растворе муравьиной кислоты. При обработке необходимо следить, чтобы с поверхности изделия удалялись только солевые и оксидные загрязнения и новообразования и не происходило бы растравливания меди. Преимуществом муравьиной кислоты перед другими реагентами является ее летучесть, благодаря которой обеспечивается сохранность реставрируемого изделия. Хорошо очищают медные сплавы 5—10%-ные растворы лимонной и уксусной кислот, но после такой очистки изделия необходимо тщательно промывать. Бронзовые изделия можно очищать от оксидно-солевых загрязнений и неравномерной патины в 10— 15 % -ных растворах аммиака и карбоната аммония. Высокой способностью очищать медные сплавы от оксидно-солевых и карбонатно-кальциевых загрязнений обладают растворы динатрие-вой соли этилендиаминтетрауксусной кислоты (трилон Б). Обычно пользуются 10%-ным раствором трилона Б. Очистка происходит медленно и ее необходимо контролировать во избежание растравливания отдельных участков металла. Специфическим «мягким» растворителем продуктов коррозии меди и бронзы является 10—15%-ный раствор гексаметафосфата натрия, который действует также на известковые новообразования, землю, глину. Размягченные наслоения постепенно удаляют с поверхности изделий щетинной кистью и водой, обработка ускоряется, если применять горячий 20%-ный раствор гексаметафосфата натрия с температурой 40— 50° С. В настоящее время все более широкое применение получают пастообразные и пленкообразные очищающие составы. В качестве пленко-образователей применяют поливиниловый спирт и различные дисперсии, модифицированные глицерином или другим многоатомным спиртом для снижения адгезии. В качестве очищающего средства в состав включают этилендиамин или полимеры, содержащие карбоксильные группы. К последним относятся метакриловая кислота и гидролизованный сополимер стирола с малеиновым ангидридом (старомаль). Кислотность раствора устанавливается на уровне 4,5—5,5 рН добавлением аммония. Очистка черных металлов. Одними из составляющих продуктов коррозии черных металлов являются хлоридные соли. Их можно удалять промывкой в струе дистиллированной воды или вывариванием. Оба процесса очень длительные. Эффективное удаление хлоридов происходит при обработке изделия в насыщенном растворе углекислого аммония в нашатырном спирте. Соли аммония из корки продуктов коррозии удаляют нагреванием до 300 ° С. Возможно электрохимическое давление иона хлора в 2—3%-ном растворе едких щелочей. Хлориды можно удалять, обрабатывая изделие раствором гидрокси-да лития в этаноле. Для очистки железа от продуктов коррозии применяют растворы минеральных и органических кислот, обычно с добавлением 1—2% пирокатехина, гидрохинона, ментола. Наиболее активной смесью является раствор, содержащий ортофосфорную (35%) и соляную (5—10%) кислоты с добавлением ингибиторов. Эффективными очищающими средствами являются растворы органических кислот: тиогликолевой, лимонной, муравьиной, щавелевой. Эти кислоты, так же как и динатриевая соль этилендиаминтетрауксусной кислоты (трилон Б), достаточно хорошо растворяют оксиды и гидроксиды железа и достаточно медленно реагируют с компактным металлом. Введение в раствор органических кислот и трилона Б, ингибиторов коррозии (например, уротропина) полностью подавляет рас-травливание металла. Особое место в реставрации изделий из железа занимает удаление отдельных очагов коррозии. Для этого участок корродированного металла обрабатывают пастой из порошка цинка и 15%-ного раствора едкого натра или загущенными очищающими растворами. Для послойного удаления солевых и оксидных образований можно применять растворы пленкообразующих полимеров — полиэлектролитов, сополимеров акрилового и винилового ряда, содержащих карбоксильные группы. Представляет известный интерес обработка металла низкотемпературной газовой плазмой, которая содержит значительное количество химически активных ионов, радикалов атомов и молекул в возбужденном состоянии. С помощью кислород-аргоновой плазмы без нагревания можно полностью удалить с поверхности изделия органические загрязнения. Затем, используя смесь «водород—аргон», удаляют большинство солей и полностью восстанавливают оксиды до металла. Полностью и почти полностью восстановить корродированное железо, в частности сильно окисленные археологические находки, позволяет использование оксида углерода или водород. В первом случае восстановление производят в электрической печи над слоем древесного угля при температуре 800 °С. Восстановления металла из оксида железа заканчивают при снижении содержания СОг в отходящих газах до определенного уровня. Термическое восстановление железа с помощью водорода осуществляют в трубчатых печах при температуре 400—600 ° С. После термического восстановления поверхность изделий имеет так называемую губчатую структуру, поэтому их необходимо тщательно промыть в кипящем растворе едкого натра, а затем в дистиллированной воде, высушить и обработать защитным средством. Очистка олова и свинца. Очистка этих металлов от обычных загрязнений не вызывает особых затруднений. Достаточно горячей воды, мыла, мягкой щетки и фланели. При очистке свинца от органических загрязнений (масел, лаков, красок) органическими растворителями ограничивают использование хлорированных углеводородов и сложных эфиров. Очистка серебра. Серебряные изделия лучше очищать растворами трилона Б (105) в сочетании с неионогенными ПАВ, в частности с ОП-7 илиОП-10 (0,5—1,0%). Сульфидную пленку с поверхности серебряных изделий удаляют раствором следующего состава (г/л): тиомочевина — 80—85; ортофос-форная кислота — 10—20; этиловый спирт — 60—65; ОП-7 — 5—10; вода — до 1000 мл. После удаления сульфидных пленок изделие промывают в воде и сушат.
|
||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 740; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.185.207 (0.009 с.) |