
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Билет № 46: Седиментационое равновесие. Факторы, определяющие седиментационную устойчивость дисп. системы.Содержание книги
Поиск на нашем сайте
Седиментация – осаждение ч-ц в гравитационном поле Способность к седиментации выражают ч/з константу седиментации, которая связана со скоростью оседания (u): Sсед = u/g, где g – ускорение своб. падения Для сферических ч-ц: Sсед = 2r2 (ρ – ρ0) / 9η [Сб], где ρ и ρ0 – плотность вещ-ва дисп. фазы и дисп. среды соотв.; Особенности седиментационного равновесия: При седиментационном равновесии действие гравитационных сил полностью компенсируется силами диффузии. В поле действия гравитационных сил это равновесие хар-ся опред. распределением ч-ц по высоте. Тяжёлые ч-цы находятся в осадке; лёгкие частицы обл. высокой кинетич. энергией и поэтому всплывают. Ч-цы золей занимают промежуточное место. Устойчивость системы к оседанию называют кинетической, или седиментационной. Мерой устойчивости служит гипсометрическая высота (высота от некоторого уровня, при подъёме на кот. концентрация коллоидных ч-ц уменьшается в 2 р. Гипсометрический з-н: lnνh/ν0 = -(Vч g(ρ – ρ0)h)/ (kT), где h – гипсометрическая высота; νh и ν0 – частичные конц-ии на высоте h и на начальном уровне соотв.; Vч – объём отд. колл. ч-цы Факторы сед. устойчивости: 1) структурно- мех. фактор – заключается в формировании на пов-ти ч-ц дисп. фазы упругой и механически прочной защитной плёнки. Разрушение этой плёнки требует затрат энергии и времени. Часто мех. плёнку обр-ют ПАВы 2) Гидродинамический фактор – объясняют изменением вязкости среды и плотностей дисп. фазы и дисп. среды. Благодаря этим изменениям снижается скорость движения коагулирующих ч-ц и вытекания дисп. среды из прослоек м/у ними, а значит, и коагуляции в целом. Билет № 47: Возникновение объёмно-пористых стр-р. Структурообразование по теории ДЛФО. Коагуляционно- тиксотропные и конденсационно- кристаллизационные стр-ры. Структурообразование – включает в себя процессы объединения частиц дисп. фазы, в рез-те кот. обр-ся тело, характеризуемое некоторым пространственным каркасом и непосредственной связью м/у частицами. Классификация по Ребиндеру:
Билет №48: Адсорбция на пов-ти тв. тел. Теория адсорбции, Ур-е Ленгмюра и его анализ. Адсорбция – самопроизвольное концентрирование газообразного или раств. в воде вещ-ва на пов-ти раздела фаз. Адсорбат – вещ-во, адсорбированное адсорбентом. Адсорбент – конденсированная фаза, на пов-ти кот. происходит адсорбция. Адсорбтив – адсорбирующееся вещ-во. А. на границе тв. тело-газ исслед. Ленгмюр. В его теории адсорбцион. спос-ть в-в хар-ся абсолют. кол-вом адсорбир. в-ва А.Теория опис. идеал. сис-мы, часто не вып-ся на практике, служит базой для др. теорий. А. мол-л происх. на актив.адсорбцион.центрах-дефекты на пов-ти крист.решетки.Актив.центр удерж.одну адсорбир.мол-лу =>при полном заполнении пов-ти обр-ся монослой из адсорбир.мол-л,а теорию Ленгмюра наз-ют теорией монослойной А. Ур-ие Ленгмюра:А=Аmax·Kp/(1+Kp)(1). Исп. рав-во p=cRT, ур-ие м. выразить ч/з конц-ию газа:A=Amax·KRTc/(1+KRTc).Константа K показывает соотнош-ие констант скоростей адсорбции и десорбции: K=kад/kдес.
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 849; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.22.41.80 (0.008 с.) |

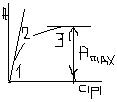 1) конц-ия адсорбтива оч.мала: с→0,KRTc→0,1>>KRTc.=> A=Amax·KRTc. А. опис-ся линейным нач.участком изотермы. 2) конц-ия адсорбтива им.промежут.знач-ие-вып-ся ур-ие A=Amax·KRTc/(1+KRTc).А.опис-ся переход.участком изотермы. 3) конц-ия адсорбтива оч.велика,с→∞.В ур-ии A=Amax·KRTc/(1+KRTc) единицей м.пренебречь и получить: A=Amax. А. опис-ся графиком, || оси абсцисс, что соотв.макс.заполнению пов-ти слоем адсорбир. в-ва. Это предел.мономолек. А. Т.о., на нач. этапе А. газа ↑ пропорц. ↑ р(c) адсорбтива, затем рост замедляется и при высоких р(c) пов-ть адсорбента покрывается мономолек. слоем адсорбата. Постоянные K и Amax м. опред-ть из графика линейной зав-ти р/А от р.Из(1) следует,что А+АKp= Amax Ap.Разделим на KА Amax лев. и прав. части ур-ия (1),в итоге:1/(K Amax)+p/ Amax=p/A.
1) конц-ия адсорбтива оч.мала: с→0,KRTc→0,1>>KRTc.=> A=Amax·KRTc. А. опис-ся линейным нач.участком изотермы. 2) конц-ия адсорбтива им.промежут.знач-ие-вып-ся ур-ие A=Amax·KRTc/(1+KRTc).А.опис-ся переход.участком изотермы. 3) конц-ия адсорбтива оч.велика,с→∞.В ур-ии A=Amax·KRTc/(1+KRTc) единицей м.пренебречь и получить: A=Amax. А. опис-ся графиком, || оси абсцисс, что соотв.макс.заполнению пов-ти слоем адсорбир. в-ва. Это предел.мономолек. А. Т.о., на нач. этапе А. газа ↑ пропорц. ↑ р(c) адсорбтива, затем рост замедляется и при высоких р(c) пов-ть адсорбента покрывается мономолек. слоем адсорбата. Постоянные K и Amax м. опред-ть из графика линейной зав-ти р/А от р.Из(1) следует,что А+АKp= Amax Ap.Разделим на KА Amax лев. и прав. части ур-ия (1),в итоге:1/(K Amax)+p/ Amax=p/A.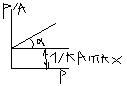 tgα=1/ Amax, величина К опред-ся из отрезка, отсекаемого графиком на оси ординат.
tgα=1/ Amax, величина К опред-ся из отрезка, отсекаемого графиком на оси ординат.


