Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Несмотря на простоту строения, глицин и серин являются весьма востребован-ными аминокислотами в клетках. Они могут превращаться друг в друга.Содержание книги
Поиск на нашем сайте Роль реакции превращения серина в глицин состоит в образовании активной Формы ТГФК-N5,N10-метилен-ТГФК.
ВЗАИМОСВЯЗЬ ОБМЕНА ГЛИЦИНА, СЕРИНА И МЕТИОНИНА Реакции метилирования являются распространенными в организме. Они необхо-димы для синтеза ряда веществ – креатина, холина, карнитина, адреналина, фос-фатидилхолина, нуклеотидов в ДНК и РНК, гистонов, чужеродных веществ, в том числе лекарственных соединений. Источником метильной группы для этих реакций является S-аденозилметионин и производные тетрагидрофолиевой кислоты (ТГФК). Образованный в реакции распада серина до глицина N5,N10-метилен-ТГФК пре-вращается в N5-метил-ТГФК. N5-Метил-ТГФК участвует в реакции реметилирования гомоцистеина в метионин. Последний впоследствии присоединяет аденозильный ос-таток и превращается в активную форму метионина – S-аденозилметионин, участ-вующий во многих реакциях метилирования.
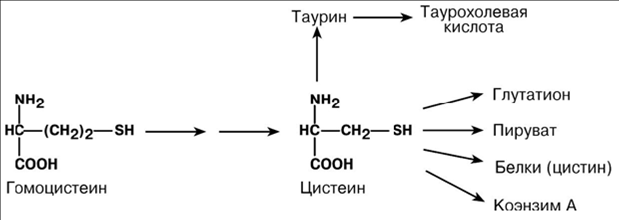
ПУТИ ИСПОЛЬЗОВАНИЯ ЦИСТЕИНА
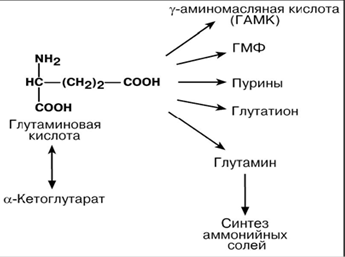
ПУТИ ИСПОЛЬЗОВАНИЯ ГЛУТАМИНОВОЙ И АСПАРАГИНОВОЙ КИСЛОТ
Деградация аминокислот: общие сведения Углеродные скелеты 20 белковых аминокислот (см. с. 66) превращаются в итоге в семь различныхпродуктов деградации (на схеме окрашены в розовый и светло-голубой цвета). Пять метаболитов (2-оксоглутарат, сукцинил-КоА, фумарат, оксалоацетат и пируват) служат предшественниками в процессе глюконеогенеза (см. с. 156). Первые четыре являются еще и промежуточными продуктами цитратного цикла, в то время как пируват может быть переведен пируватдекарбоксилазой в оксалоацетат и тем самым стать участником глюконеогенеза (зеленая стрелка). Аминокислоты, деградация которых поставляет один из пяти упомянутых метаболитов, называются глюкогенными аминокислотами. За двумя исключениями (лизин и лейцин, см. ниже) глюкогенными являются все белковые аминокислоты. Два других продукта распада (ацетоацетат и ацетил-КоА) не могут включаться в глюконеогенез в организме животных. Они используются для синтеза кетоновых тел, жирных кислот и изопреноидов (см. сс. 174, 304). Поэтому аминокислоты, которые разрушаются с образованием ацетил-КоА или ацетоацетата, называются кетогенными аминокислотами. Фактически кетогенными являются только лейцин и лизин. Некоторые аминокислоты поставляют продукты деградации, являющиеся глюкогенами и кетогенами. К этой группе принадлежат фенилаланин, тирозин, триптофан и изолейцин. Существует несколько путей удаления аминогруппы во время распада аминокислоты (дезаминирования). Обычно NH2-группа переносится путем трансаминирования на 2-оксоглутарат (см. с. 180, желтые метки на схеме). Образующийся глутамат в дальнейшем вновь превращается в 2-оксоглутарат с помощью глутаматдегидрогеназы (окислительное дезаминирование, зеленая метка). В этой реакции образуется свободный аммиак (NH3), который у высших животных превращается в мочевину и выводится из организма (см. с. 184). Аммиак освобождается также при гидролизе амидных групп аспарагина и глутамина (гидролитическое дезаминирование, оранжевая метка). Другим превращением, при котором образуется NH3, является элиминирующее дезаминированиесерина в пируват (голубая метка, см. с. 402). ДЕКАРБОКСИЛАЗА АМИНОКИСЛОТ фермент, катализирующий декарбоксилирование (отщепление СО2 от карбоксильной группы) аминокислот. Ко-ферментом Д. а. является пиридоксаль-5-фосфат — производное витамина B6 (пиридоксина). Г И С Т А М И Н Реакция образования гистамина наиболее активно идет в тучных клетках, Филах и эозинофилах. В них гистамин синтезируется и накапливается в секреторных Гранулах.
В кровь гистамин выделяется при повреждении ткани, при ударе, электрическом Раздражении. В клинической практике секреция гистамина обычно связана с аллер- Гиями – при повторном попадании антигена в ранее сенсибилизированный организм Развивается аллергическая реакция. Физиологические эффекты Расширение артериол и капилляров. Как следствие – покраснение кожи, сни- жение артериального давления;
|
||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 648; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.01 с.) |