
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Використання карбонових кислот у медициніСодержание книги Поиск на нашем сайте
ацетилен → оцтовий альдегід → етанол → етилен → ацетилен → бензол → → хлорбензол → фенол → пікринова кислота
Зміст теми: · 3%, 6%, 9% розчини – оцет, використовується для обтирання та компресів. · Ацетат калію СН3СООК – діуретичний засіб при набряках серцевого походження. · Мурашина кислота НСООН – 1% спиртовий розчин (мурашиний спирт) використовується для розтирання при невралгіях, міозитах. · Валер’янова кислота С4Н9СООН – входить до складу крапель і таблеток валер’яни та валідолу, має заспокійливу дію. · Акрилова кислота СН2 = СН – СООН – полімери на основі акрилової кислоти використовують для виготовлення зубних протезів. · Бензойна кислота С6Н5СООН – антисептичний засіб, використовується зовнішньо. · Бензоат натрію С6Н5СООNa – відхаркуючий засіб. · Фенолфталеїн – проносний засіб (пурген). Самостійна робота №8 Дикарбонові кислоти 1. Скласти рівняння реакцій, що підтверджують хімічні властивості: – малонової кислоти; – янтарної кислоти; – малеїнової кислоти; – мета-фталевої кислоти.
2. Здійснити перетворення: етан → етилен → етанол → оцтова кислота → натрій ацетат → метан → → ацетилен → бензол → толуол → бензойна кислота → натрій бензоат
Самостійна робота №9 Гідроксикислоти, фенолокислоти 1. Скласти рівняння реакцій, що підтверджують хімічні властивості:
– яблучної кислоти; – винної кислоти; – лимонної кислоти; – саліцилової кислоти.
Використання карбонових кислот у медицині
Використання карбонових кислот в аналітичній хімії
Якісні реакції на карбонові кислоти
Зміст теми:
Використання карбонових кислот у медицині
· Молочна кислота – має бактерицидну дію, використовується зовнішньо для припікання (80% сироп). · Кальцій лактат – використовують при недостачі Са2+ в організмі (препарат кальцію). · Ферум (ІІ) лактат – використовують при анеміях (препарат заліза). · Винна кислота – м’який проносний засіб. · Натрій цитрат – консервант крові (1: 9). · Ферум (ІІІ) цитрат – при анеміях.
Використання карбонових кислот в аналітичній хімії
· Мурашина кислота – використовується як неводний розчинник для кислотно – основного титрування. · Щавлева кислота – використовується в якісному аналізі для відкриття іонів кальцію. · Винна кислота – використовується в якісному аналізі для відкриття іонів калію:
׀ ׀ СН – ОН СН – ОН ׀ + КОН → ׀ + Н2О СН – ОН СН – ОН ׀ ׀ СООН СООК калію гідротартрат · Сегнетова сіль (натрій – калій виннокислий) – використовується в якісному аналізі для виготовлення реактиву Фелінга: CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
СООNa СООNa ׀ ׀
СН – ОН СН – О ׀ ׀ СООK СООK · Реактив Фелінга – використовують для відкриття альдегідів.
Самостійна робота №10 Естери. Жири. 1. Скласти конспект з питань: – естери: визначення, загальна формула, номенклатура, хімічні властивості, добування; – жири: визначення, класифікація, хімічні властивості, добування, біологічна
роль; – воски: тваринні та рослинні; м’які та тверді. 2. Скласти рівняння добування з саліцилової кислоти: – метилсаліцилату; – фенілсаліцилату.
3. Здійснити перетворення: а) етан → етанол → оцтова кислота → метилацетат → етилацетат → калій ацетат → → ферум (ІІІ) ацетат
б) ацетилен → бензол → толуол → бензойна кислота → метилбензоат → натрій → → бензойна кислота → амід бензойної кислоти бензоат
Зміст теми: Естери · це похідні карбонових кислот, у яких група ОН заміщена залишком спирту.
Номенклатура
O – С2Н5 етиловий естер мурашиної кислоти
O – СН3 метиловий естер оцтової кислоти
Ізомерія: ·
O – СН3 О – С2Н5
· міжкласова
O – СН3 ОН
Хімічні властивості:
· О – С2Н5
· СН3 – С + NaОН → СН3СООNa + С2Н5ОН
·
·
Добування – реакція естерифікації:
О – С2Н5
Використання у медицині: метилсаліцилат, фенілсаліцилат (фармакологічну дію дивись в темі „Саліцилати”)
Жири · це естери спирту гліцерину та вищих жирних кислот. Класифікація жирів: · змішані · рідкі (олії) · рослинні Хімічні властивості: · гідроліз СН2 – О – СО – С15Н31 СН2 – ОН СН – О – СО – С15Н31 + 3НОН → СН – ОН + 3С15Н31СООН СН2 – О – СО – С15Н31 СН2 – ОН
· лужний гідроліз (омилення) СН2 – О – СО – С15Н31 СН2 – ОН СН – О – СО – С15Н31 + 3NaОН → СН – ОН + 3С15Н31СООNa СН2 – О – СО – С15Н31 СН2 – ОН мило
· гідрогенізація рідких жирів СН2 – О – СО – С17Н33 СН2 – О – СО – С17Н35 СН – О – СО – С17Н33 + 3Н2 → СН – О – СО – С17Н35 СН2 – О – СО – С17Н33 СН2 – О – СО – С17Н35
Добування жирів:
СН2 – ОН СН2 – О – СО – С15Н31 СН – ОН + 3С15Н31СООН → СН – О – СО – С15Н31 + 3Н2О СН2 – ОН СН2 – О – СО – С15Н31
Біологічна роль жирів:
· енергетична функція; · поживна функція; · захисна функція; · терморегуляція. Воски
· це естери вищіх карбонових кислот та вищіх спиртів.
Воски поділяють на тваринні (спермацет, бджолиний віск, ланолін) та рослинні (воски з листів рослин). Температура плавлення восків зростає зі зростанням карбонових радикалів кислот та спиртів. У зв'язку з цим воски бувають м’які та тверді.
М’які воски: · ланолін – виробляється шкірними залозами вівець. Використовують як основу лікарських мазей. · спермацет – добувають з голови кашалоту. Використовують як основу лікарських мазей. Тверді воски: · бджолиний віск – добувають з бджолиних сотів. Використовують як основу лікарських мазей та косметичних препаратів. Самостійна робота №11 Вуглеводи 1. Скласти конспект з питань: – класифікація дисахаридів; – сахароза: добування, гідроліз; – мальтоза: добування, окислення, гідроліз; – лактоза: добування, окислення, гідроліз; – крохмаль: будова, фотосинтез, властивості, біологічна роль;
– целюлоза: будова, властивості, ефіри целюлози, біологічна роль; – використання вуглеводів у медицині.
Сахароза · Добування: СН2ОН
+ + →
Н ОН ОН Н α – глюкоза β – фруктоза СН2ОН
+ Н2О
Н ОН сахароза ОН Н · Гідроліз: С12Н22О11 + Н2О → С6Н12О6 + С6Н12О6 глюкоза фруктоза Мальтоза · Добування: СН2ОН СН2ОН
Н ОН Н ОН α – глюкоза α – глюкоза СН2ОН СН2ОН
Н ОН Н ОН мальтоза
· Реакція „срібного дзеркала”: СН2ОН СН2ОН
Н ОН Н ОН
СН2ОН СН2ОН
Н ОН Н ОН
· Гідроліз: С12Н22О11 + Н2О → 2С6Н12О6
Лактоза · Добування: СН2ОН СН2ОН
Н ОН Н ОН β – галактоза α – глюкоза СН2ОН СН2ОН
Н ОН Н ОН лактоза
· Реакція „срібного дзеркала”: СН2ОН СН2ОН
Н ОН Н ОН
СН2ОН СН2ОН
→
Н ОН Н ОН
· Гідроліз: С12Н22О11 + Н2О → С6Н12О6 + С6Н12О6 галактоза глюкоза Крохмаль · Будова молекули: СН2ОН СН2ОН
Н ОН Н ОН Складається з залишків α – глюкози: – амілоза (25%) – лінійна форма; – амілопектин (75%) – розгалужена форма. • Фотосинтез: 6n CO2 + 5n H2O → (C6H10O5)n + 6n O2
· Властивості:
1 – в гарячій воді утворює колоїдний розчин (клейстер); 2 – якісна реакція – з йодом дає синє забарвлення; 3 – гідроліз (ферментативний або кислотний): (C6H10O5)n → (C6H10O5)m → С12Н22О11 → С6Н12О6 крохмаль декстрини мальтоза глюкоза
· Біологічна роль:
1 – рослини накопичують крохмаль в процесі фотосинтезу; 2 – до організму тварин та людини крохмаль надходить з їжею, гідролізується частково в ротовій порожнині під дією ферментів слини та повністю в тонкому кишечнику (фермент – амілаза); 3 – глюкоза всмоктується в кров, переноситься до різних органів і тканин, окислюється в клітинах з виділенням енергії;
4 – надлишок глюкози накопичується у вигляді глікогену в м’язах та печінці. При необхідності глікоген знов розкладається до глюкози.
Целюлоза (клітковина) · Будова молекули: СН2ОН СН2ОН
Н ОН Н ОН
Складається з залишків β – глюкози, має тільки лінійну форму.
• Властивості: 1 – не розчиняється у воді; 2 – не дає якісну реакцію з йодом; 3 – гідроліз (ферментативний або кислотний): (C6H10O5)n + nH2O → С6Н12О6 4 – утворює ефіри, що мають практичне значення.
· Ефіри целюлози: Нітрати целюлози [C6H7O2(OH)3]n + 3n HNO3 → [C6H7O2(ONO2)3]n + 3n H2O тринітрат целюлози (піроксилін) Тринітрат целюлози – вибухова речовина. Моно –, динітрати целюлози – використовують для виготовлення фото –, кіно –, рентгенівських плівок.
Ацетати целюлози [C6H7O2(OH)3]n + 3n СН3СООН → [C6H7O2(OСОСН3)3]n + 3n H2O триацетат целюлози Ацетати целюлози – штучне волокно. · Біологічна роль: 1 – стимулює моторику шлунку та кишечнику, виділення травних соків, створює відчуття ситості; 2 – виводить з кишково – шлункового тракту барвники, важкі метали та радіоактивні елементи, що попадають туди з їжею; 3 – переварювання клітковини відбувається в товстому кишечнику під дією ферменту целюлаза, але цей процес йде тільки на 10%, тому клітковина приймає участь в утворенні калу.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 876; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.140.12 (0.011 с.) |

 СООН СООК
СООН СООК СН – ОН СН – О
СН – ОН СН – О ׀ + Cu(OH)2 → ׀ Cu + 2Н2О
׀ + Cu(OH)2 → ׀ Cu + 2Н2О Загальна формула
Загальна формула


 O
O Н – C мурашино–етиловий естер або
Н – C мурашино–етиловий естер або
 O
O СН3 – C оцтово–метиловий естер або
СН3 – C оцтово–метиловий естер або


 О
О


 за складом прості
за складом прості
 за фізичними властивостями тверді
за фізичними властивостями тверді
 за походженням тваринні
за походженням тваринні
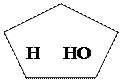
 О О
О О




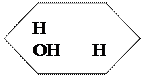 О О
О О






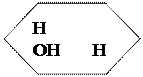
 → + Н2О
→ + Н2О









 глюкоза
глюкоза

 → О + Н2О
→ О + Н2О









